名校
解题方法
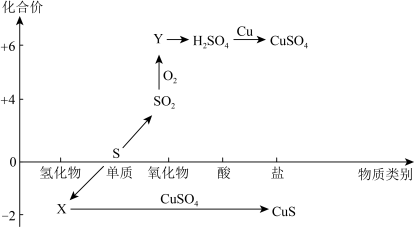
1 . 硫及其化合物的“价-类”二维图如下图所示,回答下列问题:___________ ,Y的化学式是___________ 。
(2)检验 时,取少量待测液于试管中,先加入
时,取少量待测液于试管中,先加入___________ ,无明显现象,再加入___________ 溶液,若产生白色沉淀,则溶液中含有 。
。
(3)CuS与足量浓硫酸反应也可制得SO2,该反应的化学方程式为:CuS+4H2SO4(浓) CuSO4+4SO2↑+4H2O。
CuSO4+4SO2↑+4H2O。
①请用“双线桥”法标明该反应电子转移的方向和数目___________ 。
②当有1.5NA电子发生转移时,理论上生成SO2的体积(标准状况)为___________ L。
(2)检验
 时,取少量待测液于试管中,先加入
时,取少量待测液于试管中,先加入 。
。(3)CuS与足量浓硫酸反应也可制得SO2,该反应的化学方程式为:CuS+4H2SO4(浓)
 CuSO4+4SO2↑+4H2O。
CuSO4+4SO2↑+4H2O。①请用“双线桥”法标明该反应电子转移的方向和数目
②当有1.5NA电子发生转移时,理论上生成SO2的体积(标准状况)为
您最近一年使用:0次
名校
解题方法
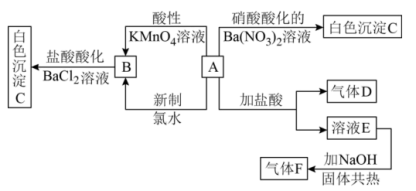
2 . 一种白色晶体A极易溶于水,将A配成溶液进行如下框图所示的实验,实验现象及转化关系如下列框图所示。其中A为正盐,气体D能使品红溶液褪色,气体F能使湿润的红色石蕊试纸变蓝。
(1)写出下列物质化学式:A___________ ;C___________ ;
(2)写出F的电子式:___________ ;
(3)写出溶液E与 共热反应的离子方程式:
共热反应的离子方程式:___________ ;
(4)写出A和新制氯水反应的离子方程式:___________ 。
(1)写出下列物质化学式:A
(2)写出F的电子式:
(3)写出溶液E与
 共热反应的离子方程式:
共热反应的离子方程式:(4)写出A和新制氯水反应的离子方程式:
您最近一年使用:0次
名校
解题方法
3 . 绿矾(FeSO4·7H2O)是治疗缺铁性贫血药品的重要成分,某化学兴趣小组利用工厂的废铁屑(主要成分为Fe,此外还含有少量Cu、Al,Al2O3和Fe2O3)制备磁性Fe3O4胶体粒子、绿矾和净水剂Na2FeO4的实验流程如图:
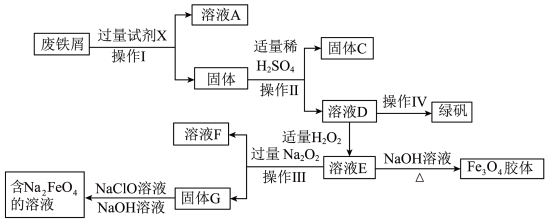
请回答下列问题:
(1)试剂X化学式为______ 。
(2)铁元素在元素周期表的位置为______ 。
(3)固体C化学名称为______ 。溶液D中加入 溶液,无红色产生,原因是
溶液,无红色产生,原因是______ (用离子方程式表示)。
(4)为得到绿矾晶体需要将溶液D倒入______ (填仪器名称)中进行浓缩,结晶。
(5)D中加入适量H2O2生成E的离子方程式______ 。若D中含3amolFe2+,则理论上加入______  H2O2可使溶液E中铁元素恰好转化为Fe3O4胶体。
H2O2可使溶液E中铁元素恰好转化为Fe3O4胶体。
(6)由固体G生成Na2FeO4的离子方程式为______ 。

请回答下列问题:
(1)试剂X化学式为
(2)铁元素在元素周期表的位置为
(3)固体C化学名称为
 溶液,无红色产生,原因是
溶液,无红色产生,原因是(4)为得到绿矾晶体需要将溶液D倒入
(5)D中加入适量H2O2生成E的离子方程式
 H2O2可使溶液E中铁元素恰好转化为Fe3O4胶体。
H2O2可使溶液E中铁元素恰好转化为Fe3O4胶体。(6)由固体G生成Na2FeO4的离子方程式为
您最近一年使用:0次
名校
4 . 已知反应Ⅰ~反应Ⅳ为单质与单质在一定条件下的化合反应。
①图中涉及的物质中除甲和B外均由短周期元素组成。
②乙与B在高温下反应能放出大量的热,生成C和甲,该反应能用于焊接钢轨。
③甲在A中燃烧生成B,丁在D中燃烧生成E和丙。
④D是一种常见的温室气体,且E中丁元素的质量分数为60%。

回答下列问题:
(1)写出下列物质的化学式:A___________ 、B___________ 。
(2)组成丁的元素在元素周期表的位置是___________ ,物质D的电子式为___________ 。
(3)写出丁在D中燃烧的化学方程式:___________ 。
(4)C与足量 溶液反应的离子方程式为
溶液反应的离子方程式为___________ 。
(5) 溶于足量盐酸,得到的溶液与铜粉完全反应,至少需要铜粉的质量为
溶于足量盐酸,得到的溶液与铜粉完全反应,至少需要铜粉的质量为___________ 。
①图中涉及的物质中除甲和B外均由短周期元素组成。
②乙与B在高温下反应能放出大量的热,生成C和甲,该反应能用于焊接钢轨。
③甲在A中燃烧生成B,丁在D中燃烧生成E和丙。
④D是一种常见的温室气体,且E中丁元素的质量分数为60%。

回答下列问题:
(1)写出下列物质的化学式:A
(2)组成丁的元素在元素周期表的位置是
(3)写出丁在D中燃烧的化学方程式:
(4)C与足量
 溶液反应的离子方程式为
溶液反应的离子方程式为(5)
 溶于足量盐酸,得到的溶液与铜粉完全反应,至少需要铜粉的质量为
溶于足量盐酸,得到的溶液与铜粉完全反应,至少需要铜粉的质量为
您最近一年使用:0次
名校
5 . 化合物X是一种由三种元素组成的重要化工原料,其相对分子质量小于200,已知B、D含有一种相同的元素且在常温下均为气体化合物,其中气体B可使品红溶液褪色,C可通过单质间的化合反应得到。(部分反应条件省略)请回答:
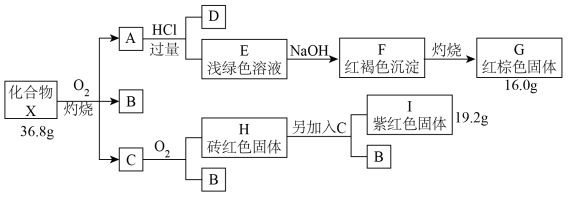
(1)写出X与 反应生成A、B、C的化学方程式
反应生成A、B、C的化学方程式______ 。
(2)检验溶液E中金属阳离子的实验操作是______ 。
(3)B和D两种气体混合发生的反应中,氧化产物与还原产物的质量之比为______ 。
(4)F溶于适量的盐酸中得到J,将5∼6滴J滴入 沸腾的蒸馏水中加热可得到K,区别J和K的方法是
沸腾的蒸馏水中加热可得到K,区别J和K的方法是______ 。
(5)如图中所示,生成 紫红色固体I,吸收
紫红色固体I,吸收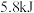 热量,写出该反应的热化学方程式
热量,写出该反应的热化学方程式______ 。
(6)将固体I溶于 与
与 的混合溶液,向其中滴加
的混合溶液,向其中滴加 的氨水直至沉淀溶解,写出沉淀溶解的离子方程式
的氨水直至沉淀溶解,写出沉淀溶解的离子方程式______ ,再加入 95%的乙醇后得到深蓝色晶体,该晶体的化学式为
95%的乙醇后得到深蓝色晶体,该晶体的化学式为______ 。

(1)写出X与
 反应生成A、B、C的化学方程式
反应生成A、B、C的化学方程式(2)检验溶液E中金属阳离子的实验操作是
(3)B和D两种气体混合发生的反应中,氧化产物与还原产物的质量之比为
(4)F溶于适量的盐酸中得到J,将5∼6滴J滴入
 沸腾的蒸馏水中加热可得到K,区别J和K的方法是
沸腾的蒸馏水中加热可得到K,区别J和K的方法是(5)如图中所示,生成
 紫红色固体I,吸收
紫红色固体I,吸收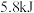 热量,写出该反应的热化学方程式
热量,写出该反应的热化学方程式(6)将固体I溶于
 与
与 的混合溶液,向其中滴加
的混合溶液,向其中滴加 的氨水直至沉淀溶解,写出沉淀溶解的离子方程式
的氨水直至沉淀溶解,写出沉淀溶解的离子方程式 95%的乙醇后得到深蓝色晶体,该晶体的化学式为
95%的乙醇后得到深蓝色晶体,该晶体的化学式为
您最近一年使用:0次
名校
解题方法
6 . 物质之间的转化关系如图,部分生成物省略。A是由四种元素组成的化合物。C、D是由元素X、Y、Z中两种组成的化合物,X、Y、Z的原子序数依次增大,在周期表中X的原子半径最小,Y、Z原子最外层电子数之和为10。D为无色非可燃性气体,G为黄绿色单质气体,J、M为金属,I有漂白作用。
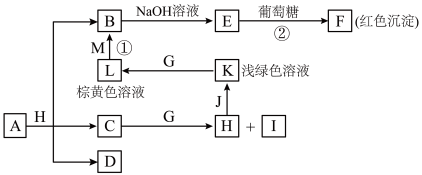
请回答下列问题:
(1)C的电子式____ 。
(2)写出反应①的离子反应方程式____ ,反应②中体现葡萄糖的____ 性。
(3)比较Y与Z的原子半径大小_____>_____(填写元素符号)。____
(4)写出A的化学式____ 。
(5)已知F溶于稀硝酸,溶液变成蓝色,并放出无色气体;请写出该反应的化学方程式____ 。
(6)研究表明:气体D在480℃、800大气压条件下可被活泼金属钠还原为晶莹透明的晶体N,其结构中原子的排列为正四面体,请写出该反应的化学方程式____ ,N的一种同素异形体的名称为____ 。

请回答下列问题:
(1)C的电子式
(2)写出反应①的离子反应方程式
(3)比较Y与Z的原子半径大小_____>_____(填写元素符号)。
(4)写出A的化学式
(5)已知F溶于稀硝酸,溶液变成蓝色,并放出无色气体;请写出该反应的化学方程式
(6)研究表明:气体D在480℃、800大气压条件下可被活泼金属钠还原为晶莹透明的晶体N,其结构中原子的排列为正四面体,请写出该反应的化学方程式
您最近一年使用:0次
2022-09-20更新
|
343次组卷
|
5卷引用:黑龙江省哈尔滨市第三中学校2022-2023学年高三上学期第一次验收考试化学试题
名校
7 . 某混合物的无色溶液中,可能含有以下离子中的若干种:K+、Ca2+、Fe3+、NH 、Cl-、CO
、Cl-、CO 和SO
和SO 。现每次取10.00mL进行实验:
。现每次取10.00mL进行实验:
①第一份加入AgNO3溶液有沉淀产生;
②第二份加入足量NaOH后加热,收集到气体448mL(标准状况下);
③第三份加入足量BaCl2溶液后,生成白色沉淀,过滤、干燥,得到固体4.30g,该固体经足量盐酸洗涤,干燥后剩余2.33g。
(1)c(CO )=
)=_______ mol·L−1;
(2)某同学认为该溶液中一定存在K+,浓度范围是_______ ;
(3)根据以上实验,某离子可能存在。检验该离子是否存在的方法是:_______ ;
(4)写出③中固体加入足量盐酸洗涤的离子方程式为_______ 。
(5)以NaIO3为原料制备I2的方法是:先向NaIO3溶液中加入计量的NaHSO3,生成碘化物;再向混合溶液中加入NaIO3溶液,反应得到I2,上述制备I2的总反应的离子方程式为_______ 。
(6)KI溶液和CuSO4溶液混合可生成CuI沉淀和I2,若生成1mol I2,消耗的KI至少为_______ mol。I2在溶液中可发生反应I2+I- I
I 。实验室中使用过量的KI与CuSO4溶液反应后,过滤,滤液经水蒸气蒸馏可制得高纯碘。反应中加入过量KI的原因是
。实验室中使用过量的KI与CuSO4溶液反应后,过滤,滤液经水蒸气蒸馏可制得高纯碘。反应中加入过量KI的原因是_______ 。
 、Cl-、CO
、Cl-、CO 和SO
和SO 。现每次取10.00mL进行实验:
。现每次取10.00mL进行实验:①第一份加入AgNO3溶液有沉淀产生;
②第二份加入足量NaOH后加热,收集到气体448mL(标准状况下);
③第三份加入足量BaCl2溶液后,生成白色沉淀,过滤、干燥,得到固体4.30g,该固体经足量盐酸洗涤,干燥后剩余2.33g。
(1)c(CO
 )=
)=(2)某同学认为该溶液中一定存在K+,浓度范围是
(3)根据以上实验,某离子可能存在。检验该离子是否存在的方法是:
(4)写出③中固体加入足量盐酸洗涤的离子方程式为
(5)以NaIO3为原料制备I2的方法是:先向NaIO3溶液中加入计量的NaHSO3,生成碘化物;再向混合溶液中加入NaIO3溶液,反应得到I2,上述制备I2的总反应的离子方程式为
(6)KI溶液和CuSO4溶液混合可生成CuI沉淀和I2,若生成1mol I2,消耗的KI至少为
 I
I 。实验室中使用过量的KI与CuSO4溶液反应后,过滤,滤液经水蒸气蒸馏可制得高纯碘。反应中加入过量KI的原因是
。实验室中使用过量的KI与CuSO4溶液反应后,过滤,滤液经水蒸气蒸馏可制得高纯碘。反应中加入过量KI的原因是
您最近一年使用:0次
名校
8 . A、B、C为中学常见单质。通常状况下,A为固体,B为黄绿色气体,C为无色气体。D、E、F、G、H、X均为化合物,其中X常温下是无色气体,其水溶液是一种强酸,E为黑色固体,H在常温下为液体。它们之间转化关系如图所示(其中某些反应条件和部分反应物已略去)。已知:二价铁离子与铁氰化钾溶液生成蓝色沉淀,三价铁离子与铁氰化钾溶液无明显现象,请回答下列问题:

(1)写出下列物质的化学式:A___ 、X___ 。
(2)反应⑦的化学方程式是___ 。
(3)检验D的溶液中是否含有G中阳离子的方法是___ 。
(4)A的一种含氧酸根AO 具有强氧化性,在其钠盐溶液中加入稀硫酸,溶液变为黄色,并有可使带火星的木条复燃的无色气体生成。该反应的离子方程式是
具有强氧化性,在其钠盐溶液中加入稀硫酸,溶液变为黄色,并有可使带火星的木条复燃的无色气体生成。该反应的离子方程式是___ 。
(5)向0.02molA的氧化物中加入45mL4mol/L硫酸溶液恰好完全反应,所得溶液中A2+能恰好被标准状况下672mL氯气氧化。则该铁的氧化物与酸反应的离子方程式为:___ 。
(6)向G溶液中加入氢氧化钠溶液的现象是___ 。

(1)写出下列物质的化学式:A
(2)反应⑦的化学方程式是
(3)检验D的溶液中是否含有G中阳离子的方法是
(4)A的一种含氧酸根AO
 具有强氧化性,在其钠盐溶液中加入稀硫酸,溶液变为黄色,并有可使带火星的木条复燃的无色气体生成。该反应的离子方程式是
具有强氧化性,在其钠盐溶液中加入稀硫酸,溶液变为黄色,并有可使带火星的木条复燃的无色气体生成。该反应的离子方程式是(5)向0.02molA的氧化物中加入45mL4mol/L硫酸溶液恰好完全反应,所得溶液中A2+能恰好被标准状况下672mL氯气氧化。则该铁的氧化物与酸反应的离子方程式为:
(6)向G溶液中加入氢氧化钠溶液的现象是
您最近一年使用:0次
2021-11-26更新
|
440次组卷
|
3卷引用:黑龙江省大庆铁人中学2021-2022学年高一上学期期中考试化学试题
名校
9 . 回答下列问题:
(1)甲、乙、丙、丁四种易溶于水的物质,分别由NH 、Ba2+、Mg2+、H+、OH-、Cl-、HCO
、Ba2+、Mg2+、H+、OH-、Cl-、HCO 、SO
、SO 中的不同阳离子和阴离子各一种组成,已知:
中的不同阳离子和阴离子各一种组成,已知:
①将甲溶液分别与其他三种物质的溶液混合,均有白色沉淀生成;
②0.1 mol·L-1乙溶液中pH<1;
③向丙溶液中滴入AgNO3溶液有不溶于稀HNO3的白色沉淀生成。推断甲、乙、丙、丁的化学式:甲___________ ,乙___________ ,丙___________ ,丁___________ 。写出过量的甲与丁的稀溶液反应的离子方程式:___________ 。
(2)一定条件下,向FeSO4溶液中滴加碱性NaBH4溶液,溶液中BH (B元素的化合价为+3价)与Fe2+反应生成纳米铁粉、H2和B(OH)
(B元素的化合价为+3价)与Fe2+反应生成纳米铁粉、H2和B(OH) ,其离子方程式为
,其离子方程式为___________ 。
(3)无水条件下制备高铁酸钠的主要反应为2FeSO4+aNa2O2=2Na2FeO4+bX+2Na2SO4+cO2↑,该反应中物质X的化学式为___________ ,b与c的关系是___________ 。
(1)甲、乙、丙、丁四种易溶于水的物质,分别由NH
 、Ba2+、Mg2+、H+、OH-、Cl-、HCO
、Ba2+、Mg2+、H+、OH-、Cl-、HCO 、SO
、SO 中的不同阳离子和阴离子各一种组成,已知:
中的不同阳离子和阴离子各一种组成,已知:①将甲溶液分别与其他三种物质的溶液混合,均有白色沉淀生成;
②0.1 mol·L-1乙溶液中pH<1;
③向丙溶液中滴入AgNO3溶液有不溶于稀HNO3的白色沉淀生成。推断甲、乙、丙、丁的化学式:甲
(2)一定条件下,向FeSO4溶液中滴加碱性NaBH4溶液,溶液中BH
 (B元素的化合价为+3价)与Fe2+反应生成纳米铁粉、H2和B(OH)
(B元素的化合价为+3价)与Fe2+反应生成纳米铁粉、H2和B(OH) ,其离子方程式为
,其离子方程式为(3)无水条件下制备高铁酸钠的主要反应为2FeSO4+aNa2O2=2Na2FeO4+bX+2Na2SO4+cO2↑,该反应中物质X的化学式为
您最近一年使用:0次
2021-10-22更新
|
109次组卷
|
2卷引用:黑龙江省佳木斯市第一中学2021-2022学年高三上学期第四次调研考试化学试题
解题方法
10 . 形成酸雨的原理之一可简单表示如图:

请回答下列问题:
(1)酸雨的pH___________ (填“>”“<”或“=”)5.6;
(2)D物质的化学式为___________ ;C物质的化学式为___________ ;
(3)反应b的化学方程式为___________ 。
(4)写出汽车尾气中CO、NO相互作用生成可参与大气循环的两种气体的化学方程式___________ :反应中氧化剂是___________ 。

请回答下列问题:
(1)酸雨的pH
(2)D物质的化学式为
(3)反应b的化学方程式为
(4)写出汽车尾气中CO、NO相互作用生成可参与大气循环的两种气体的化学方程式
您最近一年使用:0次



