名校
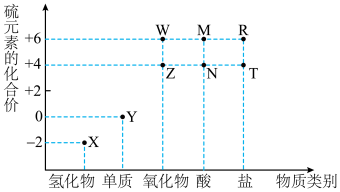
1 . 利用元素的化合价物质类别的坐标系,可以对含某元素的各物质性质有整体的认识。如图是硫元素的常见化合价与部分物质类别的对应关系。______ ;检验其阴离子的方法是______ 。
(2)化石燃料的燃烧可产生 ,在上述图表中它是
,在上述图表中它是______ (图中的字母),为避免过多 进入大气造成酸雨,沿海的火电站可利用天然海水(显弱碱性的微粒主要是
进入大气造成酸雨,沿海的火电站可利用天然海水(显弱碱性的微粒主要是 )吸收该物质,成本低廉。其过程如下。
)吸收该物质,成本低廉。其过程如下。 时,发生的主要反应的离子方程式为
时,发生的主要反应的离子方程式为______ 。
②氧化的目的是将硫元素全部转化为 ,该过程中溶液pH
,该过程中溶液pH______ (填“升高”“不变”或“降低”)。
③排放海水与原海水相比,减少的 与增加的
与增加的 的物质的量之比的为
的物质的量之比的为______ 。
(3)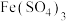 溶液脱除空气污染物X并再生的原理如图所示。反应I的离子方程式为
溶液脱除空气污染物X并再生的原理如图所示。反应I的离子方程式为______ ;每脱除170kg X,消耗标准状况下 的体积为
的体积为______ L。
(2)化石燃料的燃烧可产生
 ,在上述图表中它是
,在上述图表中它是 进入大气造成酸雨,沿海的火电站可利用天然海水(显弱碱性的微粒主要是
进入大气造成酸雨,沿海的火电站可利用天然海水(显弱碱性的微粒主要是 )吸收该物质,成本低廉。其过程如下。
)吸收该物质,成本低廉。其过程如下。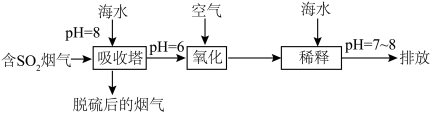
 时,发生的主要反应的离子方程式为
时,发生的主要反应的离子方程式为②氧化的目的是将硫元素全部转化为
 ,该过程中溶液pH
,该过程中溶液pH③排放海水与原海水相比,减少的
 与增加的
与增加的 的物质的量之比的为
的物质的量之比的为(3)
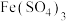 溶液脱除空气污染物X并再生的原理如图所示。反应I的离子方程式为
溶液脱除空气污染物X并再生的原理如图所示。反应I的离子方程式为 的体积为
的体积为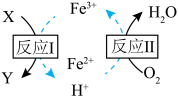
您最近一年使用:0次
2 . 在研究前18号元素时发现,随原子序数递增可以将它们排成如图所示的蜗牛形状。图中每个点代表一种元素,其中①代表氢元素。___________ 键(填“离子”或“共价”);
(2)写出由元素①、②、③形成的化合物的电子式___________ 。
(3)Li和元素③在同一族,现代航天工业中选择用 做供氧剂的原因是
做供氧剂的原因是___________ 。
(4)元素④在元素周期表中的位置是___________ 。
(5)自然界磷元素只存在一种稳定的核素 。约里奧-居里夫妇在核反应中用α粒子轰击
。约里奧-居里夫妇在核反应中用α粒子轰击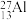 ,得到另一种核素
,得到另一种核素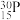 。
。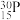 与
与 的关系是
的关系是___________ 。
(6)请设计实验验证元素④的非金属性弱于元素⑤的非金属性___________ (用离子方程式表示)。
(7)向由元素②、③、⑤按原子个数比1∶1∶1组成的化合物水溶液中滴入石蕊试液,溶液变成蓝色,一段时间后溶液颜色褪去,请解释原因___________ 。

(2)写出由元素①、②、③形成的化合物的电子式
(3)Li和元素③在同一族,现代航天工业中选择用
 做供氧剂的原因是
做供氧剂的原因是(4)元素④在元素周期表中的位置是
(5)自然界磷元素只存在一种稳定的核素
 。约里奧-居里夫妇在核反应中用α粒子轰击
。约里奧-居里夫妇在核反应中用α粒子轰击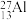 ,得到另一种核素
,得到另一种核素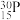 。
。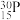 与
与 的关系是
的关系是(6)请设计实验验证元素④的非金属性弱于元素⑤的非金属性
(7)向由元素②、③、⑤按原子个数比1∶1∶1组成的化合物水溶液中滴入石蕊试液,溶液变成蓝色,一段时间后溶液颜色褪去,请解释原因
您最近一年使用:0次
名校
解题方法
3 . 已知A、B、C、D、E、F、G是原子序数依次增大的短周期主族元素,A是原子半径最小的元素,A与B形成的一种化合物能使湿润的红色石蕊试纸变蓝,C与G同主族,D与A同主族,B、D、E最外层电子数之和为8,F是地壳中含量最高的金属元素,G的单质常出现在火山喷口。
(1)C在元素周期表中的位置是_______ 。
(2)D的单质与水反应的离子方程式为_______ 。
(3)E、F分别形成的简单离子中,半径较大的是_______ (填离子符号)。
(4)D、F的最高价氧化物对应的水化物相互反应的化学方程式为_______ 。
(5)B和E形成的一种化合物可与水剧烈反应,产生沉淀与气体,该反应的化学方程式为_______ 。
(6)A和C形成的一种化合物,该化合物的一个分子中电子总数为18,并能与G的氢化物水溶液反应产生浑浊,其化学方程式为_______ 。
(1)C在元素周期表中的位置是
(2)D的单质与水反应的离子方程式为
(3)E、F分别形成的简单离子中,半径较大的是
(4)D、F的最高价氧化物对应的水化物相互反应的化学方程式为
(5)B和E形成的一种化合物可与水剧烈反应,产生沉淀与气体,该反应的化学方程式为
(6)A和C形成的一种化合物,该化合物的一个分子中电子总数为18,并能与G的氢化物水溶液反应产生浑浊,其化学方程式为
您最近一年使用:0次
2023-02-16更新
|
249次组卷
|
2卷引用:江苏省苏州市木渎高级中学2022-2023学年高一下学期期初调研化学试题
名校
解题方法
4 . 图所示的是一些常见单质、化合物之间的转化关系图,有些反应中的部分物质和反应条件被略去。已知:B是实验室中最常用的溶剂,X、Y是日常生活中常见金属单质,D、E是常见气态非金属单质,其中D呈黄绿色。A的焰色反应呈紫色(透过蓝色钻玻璃),F的稀溶液呈蓝色。
请回答下列问题:

(1)A的化学式______ ,X的化学式为______ ,I的化学式为______ 。
(2)J与Y反应的离子方程式为______ 。
(3)Y与水蒸气反应的化学方程式为______ 。
(4)向H的水溶液中加入氨水,并通入空气,得到红褐色沉淀,写出该过程中总反应的离子方程式:____________ 。
请回答下列问题:

(1)A的化学式
(2)J与Y反应的离子方程式为
(3)Y与水蒸气反应的化学方程式为
(4)向H的水溶液中加入氨水,并通入空气,得到红褐色沉淀,写出该过程中总反应的离子方程式:
您最近一年使用:0次
5 . 下表为元素周期表的一部分,表中所列的字母分别代表一种化学元素,回答(1)(2)两小问
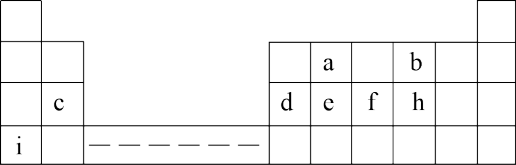
(1)a、b、c三种元素的原子半径由大到小的顺序是___________ (填元素符号);
(2)c、d、e三种元素最高价氧化物对应水化物中碱性最强的是_____ (填水化物的化学式)。
(3)配平下列离子方程式___ __MnO + ____Cl- + ____H+= ______Mn2+ + _____Cl2 + ___H2O
+ ____Cl- + ____H+= ______Mn2+ + _____Cl2 + ___H2O
(4)保持洁净安全的生存环境已成为全人类的共识。二氧化硫是引起酸雨的一种主要物质,必须严格控制排放。酸雨降落到地面后,其中的亚硫酸在空气中被氧气逐渐氧化生成硫酸,使酸性进一步增强,写出这一过程的化学方程式:___________ 。

(1)a、b、c三种元素的原子半径由大到小的顺序是
(2)c、d、e三种元素最高价氧化物对应水化物中碱性最强的是
(3)配平下列离子方程式
 + ____Cl- + ____H+= ______Mn2+ + _____Cl2 + ___H2O
+ ____Cl- + ____H+= ______Mn2+ + _____Cl2 + ___H2O(4)保持洁净安全的生存环境已成为全人类的共识。二氧化硫是引起酸雨的一种主要物质,必须严格控制排放。酸雨降落到地面后,其中的亚硫酸在空气中被氧气逐渐氧化生成硫酸,使酸性进一步增强,写出这一过程的化学方程式:
您最近一年使用:0次
名校
6 . X、Y、Z、Q、W、R是常见的短周期主族元素,其相关信息如下表:
(1)元素X在元素周期表中的位置是_______ ,其氢化物X2H4使Br2/CCl4溶液褪色的反应方程式为_______ 。
(2)上述六种元素中有2种元素能形成一种淡黄色的固体化合物,该化合物的电子式是_______ 。
(3)汽车尾气净化器可使XO与YO两种有毒气体催化转化后排放,化学反应方程式为_______ 。
(4)上述六种元素原子半径与主要化合价的关系如图,其中X的单质与④最高价氧化物对应水化物浓溶液共热反应的还原产物为_______ 。
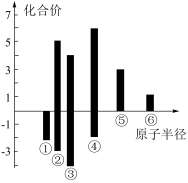
(5)为消除水体中含量过高的YQ ,可向水体中先加足量NaOH溶液再加W单质共热(有YH3生成),该反应的离子方程式为
,可向水体中先加足量NaOH溶液再加W单质共热(有YH3生成),该反应的离子方程式为_______ 。
元素 | 相关信息 |
X | 它的一种同位素被用作相对原子质量的标准 |
Y | 常温下单质为双原子分子,分子中含有3对共用电子对 |
Z | 是短周期中原子半径最大的主族元素 |
Q | 最外层电子数是次外层电子数的3倍 |
W | 原子序数等于X、Y原子序数之和 |
R | 与Q同族,且最高价氧化物的水化物的浓溶液常温下使W单质钝化 |
(2)上述六种元素中有2种元素能形成一种淡黄色的固体化合物,该化合物的电子式是
(3)汽车尾气净化器可使XO与YO两种有毒气体催化转化后排放,化学反应方程式为
(4)上述六种元素原子半径与主要化合价的关系如图,其中X的单质与④最高价氧化物对应水化物浓溶液共热反应的还原产物为

(5)为消除水体中含量过高的YQ
 ,可向水体中先加足量NaOH溶液再加W单质共热(有YH3生成),该反应的离子方程式为
,可向水体中先加足量NaOH溶液再加W单质共热(有YH3生成),该反应的离子方程式为
您最近一年使用:0次
名校
7 . 氮及其化合物是科学家们一直在探究的问题,它们在工农业生产和生命活动中起着重要的作用。回答下列问题:
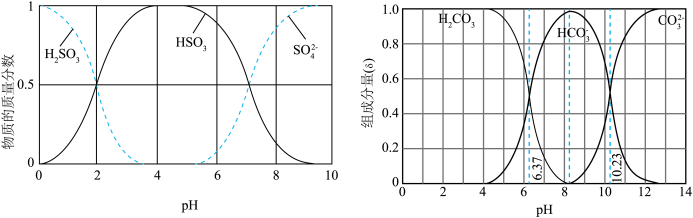
(1) 也是造成水体富营养化的重要原因之一,用
也是造成水体富营养化的重要原因之一,用 溶液氧化可除去氨气。其反应机理如左下图所示(其中
溶液氧化可除去氨气。其反应机理如左下图所示(其中 和
和 略去)。
略去)。 氧化
氧化 的总反应化学方程式为
的总反应化学方程式为_______ 。

(2)改变 对溶液中
对溶液中 去除氨气效果与余氯(溶液中
去除氨气效果与余氯(溶液中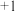 价氯元素的含量)的影响如右上图所示,则除氨气过程中最佳的
价氯元素的含量)的影响如右上图所示,则除氨气过程中最佳的 值约为
值约为_______ 。
(3)非金属单质A经如图所示的过程转化为含氧酸D,已知D为强酸,请回答下列问题:
Ⅰ.若A在常温下为气体单质,将装满气体C的试管倒扣在水槽中,溶液最终充满试管容积的 写出
写出 的化学方程式
的化学方程式_______ 。
Ⅱ.若A在常温下为非金属气态氢化物,B遇到空气变成红棕色。
①写出A到B的化学方程式_______ 。
②将 铜粉与一定量的D的稀溶液反应,当完全反应时收集到气体(全部为
铜粉与一定量的D的稀溶液反应,当完全反应时收集到气体(全部为 )
) (标准状况),向所得溶液中继续加稀硫酸至反应不能再进行,需加入
(标准状况),向所得溶液中继续加稀硫酸至反应不能再进行,需加入
_______  。
。
Ⅲ.若A为淡黄色晶体:将B直接通入 溶液不会产生白色沉淀。但与另一种气体X一起通入时则会产生白色沉淀,则气体X可能是
溶液不会产生白色沉淀。但与另一种气体X一起通入时则会产生白色沉淀,则气体X可能是_______ (写分子式)
(1)
 也是造成水体富营养化的重要原因之一,用
也是造成水体富营养化的重要原因之一,用 溶液氧化可除去氨气。其反应机理如左下图所示(其中
溶液氧化可除去氨气。其反应机理如左下图所示(其中 和
和 略去)。
略去)。 氧化
氧化 的总反应化学方程式为
的总反应化学方程式为
(2)改变
 对溶液中
对溶液中 去除氨气效果与余氯(溶液中
去除氨气效果与余氯(溶液中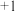 价氯元素的含量)的影响如右上图所示,则除氨气过程中最佳的
价氯元素的含量)的影响如右上图所示,则除氨气过程中最佳的 值约为
值约为(3)非金属单质A经如图所示的过程转化为含氧酸D,已知D为强酸,请回答下列问题:
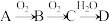
Ⅰ.若A在常温下为气体单质,将装满气体C的试管倒扣在水槽中,溶液最终充满试管容积的
 写出
写出 的化学方程式
的化学方程式Ⅱ.若A在常温下为非金属气态氢化物,B遇到空气变成红棕色。
①写出A到B的化学方程式
②将
 铜粉与一定量的D的稀溶液反应,当完全反应时收集到气体(全部为
铜粉与一定量的D的稀溶液反应,当完全反应时收集到气体(全部为 )
) (标准状况),向所得溶液中继续加稀硫酸至反应不能再进行,需加入
(标准状况),向所得溶液中继续加稀硫酸至反应不能再进行,需加入
 。
。Ⅲ.若A为淡黄色晶体:将B直接通入
 溶液不会产生白色沉淀。但与另一种气体X一起通入时则会产生白色沉淀,则气体X可能是
溶液不会产生白色沉淀。但与另一种气体X一起通入时则会产生白色沉淀,则气体X可能是
您最近一年使用:0次
2022-04-20更新
|
227次组卷
|
3卷引用:江苏省响水中学2021-2022学年高一下学期第三次学情分析考试化学试题
名校
解题方法
8 . 已知A、B、C、D、E都是周期表中前四周期的元素,它们的核电荷数依次增大。其中A、B、C是同一周期的非金属元素。A的最外层电子数是次外层的2倍,C为地壳中含量最高的元素,D的二价阳离子与C的阴离子具有相同的电子层结构。E的原子序数为24,请用化学用语回答下列问题:
(1)A、B、C的第一电离能由小到大的顺序为___________ ,电负性由大到小的顺序为___________ 。
(2)C的核外电子的轨道排布式为___________ ,E的核外电子排布式是___________ 。
(3)写出化合物AC2的电子式___________ ,单质B2的结构式___________ 。
(4)B的最高价氧化物对应的水化物的稀溶液与D的单质反应时,B被还原到最低价,该反应的化学方程式是___________ 。
(1)A、B、C的第一电离能由小到大的顺序为
(2)C的核外电子的轨道排布式为
(3)写出化合物AC2的电子式
(4)B的最高价氧化物对应的水化物的稀溶液与D的单质反应时,B被还原到最低价,该反应的化学方程式是
您最近一年使用:0次
名校
解题方法
9 . 利用元素的化合价推测物质的性质是化学研究的重要手段。如图是硫元素的常见化合价与部分物质类别的对应关系:
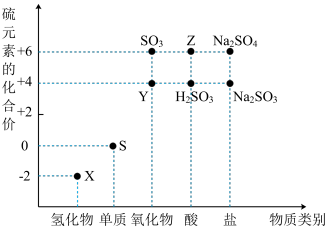
(1)从硫元素化合价变化的角度分析,图中既有氧化性又有还原性的化合物有_______ (填化学式)。
(2)将X与Y混合,可生成淡黄色固体,该反应中氧化剂与还原剂的物质的量之比为_______ 。
(3)Z的浓溶液与铜单质在一定条件下可以发生化学反应,该反应的化学方程式为_______ 。
(4)Na2S2O3是重要的化工原料。从氧化还原反应的角度分析,下列制备Na2S2O3的方案理论上可行的是_______ (填字母)。
a.Na2S+S b.Na2SO3+S c.SO2+Na2SO4 d.Na2SO3+Na2SO4
(5)已知Na2SO3能被K2Cr2O7氧化为Na2SO4,则24 mL 0.05 mol·L-1的Na2SO3溶液与20 mL 0.02 mol·L-1的K2Cr2O7溶液恰好反应时,Cr元素在还原产物中的化合价为_______ 。

(1)从硫元素化合价变化的角度分析,图中既有氧化性又有还原性的化合物有
(2)将X与Y混合,可生成淡黄色固体,该反应中氧化剂与还原剂的物质的量之比为
(3)Z的浓溶液与铜单质在一定条件下可以发生化学反应,该反应的化学方程式为
(4)Na2S2O3是重要的化工原料。从氧化还原反应的角度分析,下列制备Na2S2O3的方案理论上可行的是
a.Na2S+S b.Na2SO3+S c.SO2+Na2SO4 d.Na2SO3+Na2SO4
(5)已知Na2SO3能被K2Cr2O7氧化为Na2SO4,则24 mL 0.05 mol·L-1的Na2SO3溶液与20 mL 0.02 mol·L-1的K2Cr2O7溶液恰好反应时,Cr元素在还原产物中的化合价为
您最近一年使用:0次
2021-04-25更新
|
418次组卷
|
14卷引用:江苏省盱眙中学2022-2023学年高一下学期6月阶段测试化学试题
江苏省盱眙中学2022-2023学年高一下学期6月阶段测试化学试题【全国百强校】黑龙江省牡丹江市第一高级中学2018-2019学年高一上学期期末考试化学试题【全国百强校】内蒙古自治区杭锦后旗奋斗中学2018-2019学年高一下学期第一次月考化学试题沪科版高中化学拓展课程第4章《离子互换反应和氧化还原反应》检测题2贵州省岑巩县第四中学2019-2020学年高一上学期期末考试化学试题贵州省施秉县一中2019-2020学年高一上学期期末考试化学试题辽宁省大连市辽宁师范大学附属中学2019-2020学年高一下学期期末考试化学试题鲁科版(2019)高一必修第一册第三章第2节 硫的转化 课时4 不同价态硫元素之间的转化酸雨及其防治高一必修第一册(苏教2019版)专题4 第二单元 硫及其化合物的相互转化 课时2 含硫物质之间的转化 氧化还原反应方程式的配平河北省安平中学2020-2021学年高一上学期12月月考化学试题山西省长治市第二中学校2020-2021学年高一下学期期中考试化学试题河北省张家口市第一中学2020-2021学年高一下学期4月月考化学试题湖南省衡阳县四中2022-2023学年高二上学期开学摸底考试化学试题(A卷)黑龙江省双鸭山市第一中学2023-2024学年高二上学期开学考试化学试题
解题方法
10 . 有关物质的转化关系如下图所示,A为常见调味品,B为常见液体,C、E是金属。D、F为气态单质,其中D为黄绿色。J为红褐色固体,A、C、G、I、K的焰色反应均为黄色。已知:K是 ;
;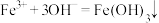 ;
;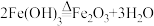 。
。
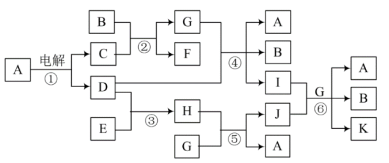
(1)物质B的电子式为___________ ;
(2)写出反应④的化学方程式,并用双线桥表示电子转移的方向和数目:___________ ;
(3)写出反应⑥的化学方程式:___________ ;
(4)聚合硫酸铁 (铁元素化合价为
(铁元素化合价为 )是一种高效的混凝剂,常用于净水,它的组成可以通过以下实验测定:
)是一种高效的混凝剂,常用于净水,它的组成可以通过以下实验测定:
①称取一定质量的聚合硫酸铁溶于水配成 的溶液。
的溶液。
②准确量取 溶液,加入盐酸酸化的
溶液,加入盐酸酸化的 溶液至沉淀完全,过滤、洗涤、干燥至恒重,得到白色固体
溶液至沉淀完全,过滤、洗涤、干燥至恒重,得到白色固体 。
。
③准确量取 溶液,加入足量的
溶液,加入足量的 溶液至沉淀完全,过滤、洗涤、干燥、灼烧至恒重,得到红棕色固体
溶液至沉淀完全,过滤、洗涤、干燥、灼烧至恒重,得到红棕色固体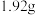 。
。
请通过计算确定该聚合硫酸铁组成中x:y:z的值为________ 。(没有计算过程不得分)
 ;
;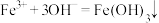 ;
;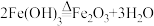 。
。
(1)物质B的电子式为
(2)写出反应④的化学方程式,并用双线桥表示电子转移的方向和数目:
(3)写出反应⑥的化学方程式:
(4)聚合硫酸铁
 (铁元素化合价为
(铁元素化合价为 )是一种高效的混凝剂,常用于净水,它的组成可以通过以下实验测定:
)是一种高效的混凝剂,常用于净水,它的组成可以通过以下实验测定:①称取一定质量的聚合硫酸铁溶于水配成
 的溶液。
的溶液。②准确量取
 溶液,加入盐酸酸化的
溶液,加入盐酸酸化的 溶液至沉淀完全,过滤、洗涤、干燥至恒重,得到白色固体
溶液至沉淀完全,过滤、洗涤、干燥至恒重,得到白色固体 。
。③准确量取
 溶液,加入足量的
溶液,加入足量的 溶液至沉淀完全,过滤、洗涤、干燥、灼烧至恒重,得到红棕色固体
溶液至沉淀完全,过滤、洗涤、干燥、灼烧至恒重,得到红棕色固体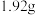 。
。请通过计算确定该聚合硫酸铁组成中x:y:z的值为
您最近一年使用:0次



