解题方法
1 . 三氯化锑 用于红外光谱分析以及显像管生产等。工业生产中,以辉锑矿(主要成分为
用于红外光谱分析以及显像管生产等。工业生产中,以辉锑矿(主要成分为 ,还含有
,还含有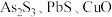 和
和 等)为原料制备
等)为原料制备 的工艺流程如图:
的工艺流程如图:
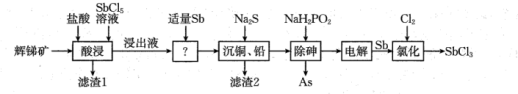
已知:① 具有强氧化性,“浸出液”主要含盐酸和
具有强氧化性,“浸出液”主要含盐酸和 ,还含
,还含 和
和 等杂质;
等杂质;
②常温下,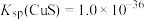 、
、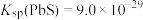 ;
;
③溶液中离子浓度小于或等于 时,认为该离子沉淀完全。
时,认为该离子沉淀完全。
回答下列问题:
(1)除将辉锑矿粉碎外,还能加快辉锑矿“酸浸”速率的措施有_____ (填两条)。
(2)“滤渣1”的主要成分有_____ (填化学式);若在实验室模拟分离“滤渣1”和“浸出液”,需要使用到的硅酸盐仪器有_____ 。
(3)“浸出液”中加入适量 的目的是
的目的是_____ (填化学方程式)。
(4)当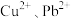 共沉淀时,溶液中
共沉淀时,溶液中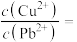
_____ (保留两位有效数字)。
(5)“除砷”时,氧化产物为 ,则
,则 (可溶于水)与
(可溶于水)与 反应的离子方程式为
反应的离子方程式为_____ 。
(6)已知:“电解” 溶液时有
溶液时有 生成。则上述流程中可循环利用的物质有
生成。则上述流程中可循环利用的物质有_____ 。
 用于红外光谱分析以及显像管生产等。工业生产中,以辉锑矿(主要成分为
用于红外光谱分析以及显像管生产等。工业生产中,以辉锑矿(主要成分为 ,还含有
,还含有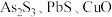 和
和 等)为原料制备
等)为原料制备 的工艺流程如图:
的工艺流程如图:
已知:①
 具有强氧化性,“浸出液”主要含盐酸和
具有强氧化性,“浸出液”主要含盐酸和 ,还含
,还含 和
和 等杂质;
等杂质;②常温下,
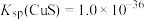 、
、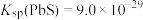 ;
;③溶液中离子浓度小于或等于
 时,认为该离子沉淀完全。
时,认为该离子沉淀完全。回答下列问题:
(1)除将辉锑矿粉碎外,还能加快辉锑矿“酸浸”速率的措施有
(2)“滤渣1”的主要成分有
(3)“浸出液”中加入适量
 的目的是
的目的是(4)当
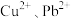 共沉淀时,溶液中
共沉淀时,溶液中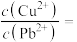
(5)“除砷”时,氧化产物为
 ,则
,则 (可溶于水)与
(可溶于水)与 反应的离子方程式为
反应的离子方程式为(6)已知:“电解”
 溶液时有
溶液时有 生成。则上述流程中可循环利用的物质有
生成。则上述流程中可循环利用的物质有
您最近一年使用:0次
解题方法
2 . 在室温下,Ti不与O2、H2O、强碱、强酸反应,在高温下可与O2反应。Hunter法是最早研究用来制取金属钛的方法,其流程如下图所示。回答下列问题:
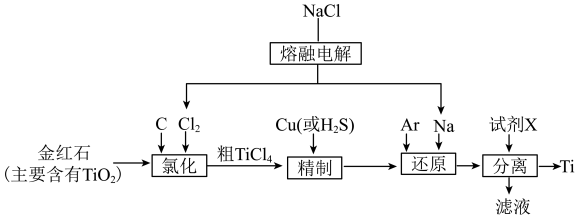
(1)“氯化”是在1000~1050℃下进行,碳被氧化为CO,该反应的化学方程式为___________ 。
(2)“精制”时,粗 中含有大量杂质,可用精馏的方法提纯,对于沸点相近的
中含有大量杂质,可用精馏的方法提纯,对于沸点相近的 杂质可用铜(或
杂质可用铜(或 )将其转化为
)将其转化为 沉淀,反应机理为
沉淀,反应机理为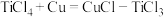 ,
,
 。从总反应看,
。从总反应看, 是该反应的
是该反应的___________ ; 可与
可与 直接反应生成
直接反应生成 ,写出
,写出 与
与 发生反应的化学方程式:
发生反应的化学方程式:___________ 。
(3)“钠还原”是用液态钠还原气态 得到Ti,Ar的作用是
得到Ti,Ar的作用是___________ ;若发生 、
、 等副反应,其原因可能是
等副反应,其原因可能是___________ 。
(4)“分离”时,固体混合物需经取出、破碎、酸浸、过滤、洗涤及干燥等步骤,试剂X为___________ (填名称),滤液循环使用的方法是___________ 。

(1)“氯化”是在1000~1050℃下进行,碳被氧化为CO,该反应的化学方程式为
(2)“精制”时,粗
 中含有大量杂质,可用精馏的方法提纯,对于沸点相近的
中含有大量杂质,可用精馏的方法提纯,对于沸点相近的 杂质可用铜(或
杂质可用铜(或 )将其转化为
)将其转化为 沉淀,反应机理为
沉淀,反应机理为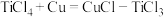 ,
,
 。从总反应看,
。从总反应看, 是该反应的
是该反应的 可与
可与 直接反应生成
直接反应生成 ,写出
,写出 与
与 发生反应的化学方程式:
发生反应的化学方程式:(3)“钠还原”是用液态钠还原气态
 得到Ti,Ar的作用是
得到Ti,Ar的作用是 、
、 等副反应,其原因可能是
等副反应,其原因可能是(4)“分离”时,固体混合物需经取出、破碎、酸浸、过滤、洗涤及干燥等步骤,试剂X为
您最近一年使用:0次
解题方法
3 . 锂离子电池在我们日常生活中随处可见,随之而来的是废旧电池的合理处理,否则会造成新的环境污染。从废旧锂离子电池正极材料(主要含LiCoO2、Al等)中回收Co并制取CoC2O4·2H2O的工艺流程如图所示:
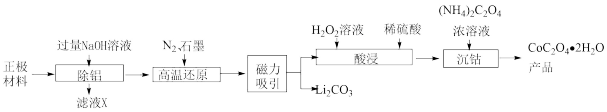
已知:①LiCoO2与NaOH溶液不反应;
②金属Co易被磁铁吸引,与稀硫酸反应生成大量氢气。
回答下列问题:
(1)“除铝”前需将废旧锂离子电池经过放电、破碎处理,其中破碎的目的是______ ,滤液X的主要溶质是______ (填化学式)。
(2)“高温还原”时,有CO生成,发生反应的化学方程式为______ ;“高温还原”时,通入N2的目的是______ 。
(3)从安全性角度考虑,“酸浸”时先加入过氧化氢溶液,再加入稀硫酸的原因是______ ,“酸浸”发生的总离子反应方程式为_______ 。
(4)“沉钴”时,检验钴离子已沉淀完全的方法是______ ,已知钴离子恰好完全沉淀(离子浓度等于10-5mol•L-1)时,c(C2O )=2.0×10-5mol•L-1,则该温度下Ksp(CoC2O4)=
)=2.0×10-5mol•L-1,则该温度下Ksp(CoC2O4)=______ 。

已知:①LiCoO2与NaOH溶液不反应;
②金属Co易被磁铁吸引,与稀硫酸反应生成大量氢气。
回答下列问题:
(1)“除铝”前需将废旧锂离子电池经过放电、破碎处理,其中破碎的目的是
(2)“高温还原”时,有CO生成,发生反应的化学方程式为
(3)从安全性角度考虑,“酸浸”时先加入过氧化氢溶液,再加入稀硫酸的原因是
(4)“沉钴”时,检验钴离子已沉淀完全的方法是
 )=2.0×10-5mol•L-1,则该温度下Ksp(CoC2O4)=
)=2.0×10-5mol•L-1,则该温度下Ksp(CoC2O4)=
您最近一年使用:0次
2023-02-17更新
|
205次组卷
|
2卷引用:青海省西宁市大通回族土族自治县2022-2023学年高三下学期开学摸底考试化学试题



