名校
1 . 氢氧化铬是一种两性氢氧化物,主要用于制备三价铬盐及三氧化二铬,也可用于油漆、颜料生产及羊毛处理等。利用铬渣(铬以低价态含氧酸盐的形式存在,主要杂质为铁、铝、硅、磷等的化合物)制备氢氧化铬的流程如图。已知:最高价铬酸根离子在酸性介质中以 形式存在,在碱性介质中以
形式存在,在碱性介质中以 形式存在,
形式存在, 在pH>12时开始溶解。下列说法错误的是
在pH>12时开始溶解。下列说法错误的是
 形式存在,在碱性介质中以
形式存在,在碱性介质中以 形式存在,
形式存在, 在pH>12时开始溶解。下列说法错误的是
在pH>12时开始溶解。下列说法错误的是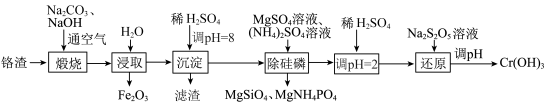
A. 常用作红色涂料 常用作红色涂料 |
B.滤渣中含有 |
C.“煅烧”后铬被氧化为 |
D.“还原”工序发生的反应为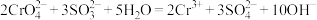 |
您最近一年使用:0次
2 . 以废料铅膏( 、
、 、
、 、
、 等)为原料,制备超细
等)为原料,制备超细 ,实现铅循环再利用的流程如下:
,实现铅循环再利用的流程如下: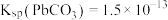 ,
,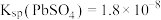 。②
。② 溶解在
溶解在 溶液中(杂质不溶于
溶液中(杂质不溶于 )的溶解度曲线如图所示:
)的溶解度曲线如图所示:
 、
、 、
、 、
、 等)为原料,制备超细
等)为原料,制备超细 ,实现铅循环再利用的流程如下:
,实现铅循环再利用的流程如下: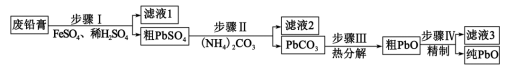
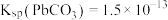 ,
,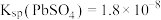 。②
。② 溶解在
溶解在 溶液中(杂质不溶于
溶液中(杂质不溶于 )的溶解度曲线如图所示:
)的溶解度曲线如图所示:
A.步骤Ⅰ发生的主要反应有 |
B.步骤Ⅱ,若滤出的 沉淀中混有 沉淀中混有 ,该滤液中 ,该滤液中 |
| C.过程中为提高产品产率,滤液3应循环使用 |
D.精制的操作是在 用碱溶解,然后趁热过滤、洗涤、干燥 用碱溶解,然后趁热过滤、洗涤、干燥 |
您最近一年使用:0次
3 . 近日,中科院上海硅酸盐研究所施剑林团队报道了MnOOH催化谷胱甘肽自氧化产生活性氧。某小组以菱锰矿(主要成分为 ,含少量
,含少量 、FeO、CoO、
、FeO、CoO、 、
、 等)为原料制备高纯度MnOOH,流程如下:
等)为原料制备高纯度MnOOH,流程如下:
②几种金属离子沉淀的pH如表所示:
下列叙述正确的是
 ,含少量
,含少量 、FeO、CoO、
、FeO、CoO、 、
、 等)为原料制备高纯度MnOOH,流程如下:
等)为原料制备高纯度MnOOH,流程如下: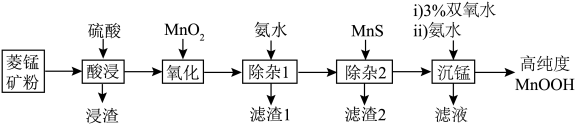
②几种金属离子沉淀的pH如表所示:
| 金属氢氧化物 |  |  |  |  |  |
| 开始沉淀的pH | 2.7 | 7.6 | 4.0 | 7.6 | 8.1 |
| 完全沉淀的pH | 3.7 | 9.6 | 5.2 | 9.2 | 10.1 |
A.滤渣1的成分是 和 和 |
B.“氧化”反应的离子方程式为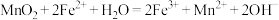 |
C.“除杂2”的原理是 |
D.双氧水氧化 ,滤液一定显酸性 ,滤液一定显酸性 |
您最近一年使用:0次
名校
解题方法
4 . ⅤA族元素及其化合物应用广泛。 催化氧化生成NO,NO继续被氧化为
催化氧化生成NO,NO继续被氧化为 ,将
,将 通入水中制取
通入水中制取 。工业上用白磷
。工业上用白磷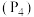 与
与 反应生成
反应生成 和一种盐,该盐可与
和一种盐,该盐可与 反应制备一元弱酸
反应制备一元弱酸 。雌黄
。雌黄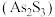 和
和 在盐酸中反应转化为雄黄
在盐酸中反应转化为雄黄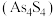 和
和 (沸点114℃)并放出
(沸点114℃)并放出 气体。砷化镓(GaAs)是第三代半导体材料,熔点高,硬度大。下列反应的化学或离子方程式错误的是
气体。砷化镓(GaAs)是第三代半导体材料,熔点高,硬度大。下列反应的化学或离子方程式错误的是
 催化氧化生成NO,NO继续被氧化为
催化氧化生成NO,NO继续被氧化为 ,将
,将 通入水中制取
通入水中制取 。工业上用白磷
。工业上用白磷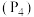 与
与 反应生成
反应生成 和一种盐,该盐可与
和一种盐,该盐可与 反应制备一元弱酸
反应制备一元弱酸 。雌黄
。雌黄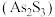 和
和 在盐酸中反应转化为雄黄
在盐酸中反应转化为雄黄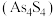 和
和 (沸点114℃)并放出
(沸点114℃)并放出 气体。砷化镓(GaAs)是第三代半导体材料,熔点高,硬度大。下列反应的化学或离子方程式错误的是
气体。砷化镓(GaAs)是第三代半导体材料,熔点高,硬度大。下列反应的化学或离子方程式错误的是A. 制 制 的离子方程式: 的离子方程式: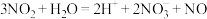 |
B.白磷与 溶液反应: 溶液反应: |
C. 与足量的 与足量的 溶液反应的离子方程式: 溶液反应的离子方程式: |
D.雌黄制备雄黄的方程式: |
您最近一年使用:0次
2024-02-20更新
|
333次组卷
|
2卷引用:河北省部分高中2023-2024学年高三上学期1月期末化学试题
名校
5 . 油画创作通常需要用到多种无机颜料。研究发现,在不同的空气湿度和光照条件下,颜料雌黄( )褪色的主要原因是发生了以下两种化学反应:
)褪色的主要原因是发生了以下两种化学反应:
 )褪色的主要原因是发生了以下两种化学反应:
)褪色的主要原因是发生了以下两种化学反应:
| A.反应Ⅰ和反应Ⅱ的还原产物均只有1种 |
| B.反应Ⅰ和Ⅱ中,元素As和S都被氧化 |
C.反应Ⅰ和Ⅱ中,参加反应的 ∶Ⅰ<Ⅱ ∶Ⅰ<Ⅱ |
D.反应Ⅰ和Ⅱ中,氧化1 mol  转移的电子数之比为3∶7 转移的电子数之比为3∶7 |
您最近一年使用:0次
2024-02-16更新
|
171次组卷
|
2卷引用:湖北省武汉市华中师范大学第一附属中学2023-2024学年高一上学期1月期末化学试题
解题方法
6 . 工业上可用次氯酸盐将氨氮废水转化为 实现绿色处理。实验室模拟如下:取等量氨水分别和不同量的
实现绿色处理。实验室模拟如下:取等量氨水分别和不同量的 混合(混合溶液体积为
混合(混合溶液体积为 ),测得溶液中氨氮(氨、
),测得溶液中氨氮(氨、 )和总氮(氨氮和
)和总氮(氨氮和 的总和)的去除率及
的总和)的去除率及 的浓度与
的浓度与 的加入量关系如图所示。
的加入量关系如图所示。
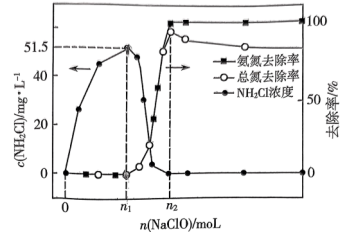
在此过程中发生的反应为:
①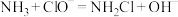
②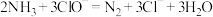
③
已知: 中氮元素为
中氮元素为 价。下列说法正确的是
价。下列说法正确的是
 实现绿色处理。实验室模拟如下:取等量氨水分别和不同量的
实现绿色处理。实验室模拟如下:取等量氨水分别和不同量的 混合(混合溶液体积为
混合(混合溶液体积为 ),测得溶液中氨氮(氨、
),测得溶液中氨氮(氨、 )和总氮(氨氮和
)和总氮(氨氮和 的总和)的去除率及
的总和)的去除率及 的浓度与
的浓度与 的加入量关系如图所示。
的加入量关系如图所示。
在此过程中发生的反应为:
①
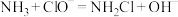
②
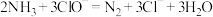
③

已知:
 中氮元素为
中氮元素为 价。下列说法正确的是
价。下列说法正确的是A.当 时,反应①中转移电子的物质的量为 时,反应①中转移电子的物质的量为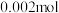 |
B.当 时, 时, |
C. |
D.当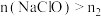 时, 时,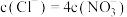 |
您最近一年使用:0次
名校
解题方法
7 . 向 和
和 的混合溶液中不断通入
的混合溶液中不断通入 ,溶液中n(含碘的某微粒)和n(含铁的某微粒)随
,溶液中n(含碘的某微粒)和n(含铁的某微粒)随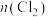 的变化曲线如图所示。(已知:
的变化曲线如图所示。(已知: 与
与 的水溶液生成
的水溶液生成 和
和 ,
, 为强酸)下列说法中不正确的是
为强酸)下列说法中不正确的是

 和
和 的混合溶液中不断通入
的混合溶液中不断通入 ,溶液中n(含碘的某微粒)和n(含铁的某微粒)随
,溶液中n(含碘的某微粒)和n(含铁的某微粒)随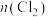 的变化曲线如图所示。(已知:
的变化曲线如图所示。(已知: 与
与 的水溶液生成
的水溶液生成 和
和 ,
, 为强酸)下列说法中不正确的是
为强酸)下列说法中不正确的是
A.a点溶液中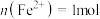 |
B.b点时已通入氯气的总体积为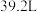 (标况) (标况) |
C.c点的总反应离子方程式为 |
D.d点溶液中阴离子的个数为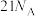 |
您最近一年使用:0次
2024-02-08更新
|
163次组卷
|
2卷引用:重庆市巴蜀中学校2023-2024学年高一上学期1月期末化学试题
8 . 某离子反应中涉及 、
、 、
、 、
、 、
、 、
、 六种微粒。其中
六种微粒。其中 的数目随时间变化的曲线如图所示。下列判断正确的是
的数目随时间变化的曲线如图所示。下列判断正确的是

 、
、 、
、 、
、 、
、 、
、 六种微粒。其中
六种微粒。其中 的数目随时间变化的曲线如图所示。下列判断正确的是
的数目随时间变化的曲线如图所示。下列判断正确的是
A.该反应的还原剂是 |
B.消耗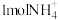 ,转移6mol电子 ,转移6mol电子 |
C. 是氧化产物 是氧化产物 |
| D.氧化剂与还原剂的物质的量之比为3:2 |
您最近一年使用:0次
2024-01-21更新
|
340次组卷
|
2卷引用:黑龙江省大庆实验中学实验一部2023-2024学年高一上学期期末考试化学试题
9 . Cu2S可用于钾离子电池的负极材料。冶炼铜时可使Cu2S在高温下与O2反应转化为Cu2O,生成的Cu2O与Cu2S进一步反应得到Cu。Cu2O在酸性溶液中会转化为Cu和Cu2+;Cu2S能被浓硝酸氧化为Cu(NO3)2。Cu在O2存在下能与氨水反应生成[Cu(NH3)4]2+;Cu(OH)2能与NaOH反应生成Na2[Cu(OH)4]。O3、O2的沸点分别为-111℃、-182℃。下列化学反应表示正确的是
A.Cu2S在高温下与O2反应:2Cu2S+4O2 2Cu2O+2SO3 2Cu2O+2SO3 |
B.Cu2S与浓硝酸反应:Cu2S+6HNO3(浓) 2Cu(NO3)2+2NO2↑+H2S↑+2H2O 2Cu(NO3)2+2NO2↑+H2S↑+2H2O |
| C.Cu2O溶于稀硝酸:Cu2O+2H+=Cu+Cu2++H2O |
| D.Cu在O2存在下与氨水反应:2Cu+8NH3·H2O+O2=2[Cu(NH3)4]2++4OH-+6H2O |
您最近一年使用:0次
名校
10 . 工业生产中除去电石渣浆(含 )中的
)中的 并制取硫酸盐的一种常用流程如图所示。下列说法正确的是
并制取硫酸盐的一种常用流程如图所示。下列说法正确的是
 )中的
)中的 并制取硫酸盐的一种常用流程如图所示。下列说法正确的是
并制取硫酸盐的一种常用流程如图所示。下列说法正确的是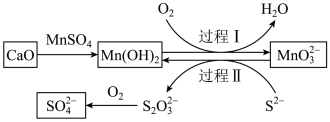
A.碱性条件下,氧化性: |
B.过程Ⅱ中,反应的离子方程式为 |
C.将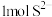 转化为 转化为 理论上需要 理论上需要 的体积为 的体积为 (标准状况) (标准状况) |
| D.该过程中涉及的化学反应均是氧化还原反应 |
您最近一年使用:0次
2024-01-14更新
|
919次组卷
|
2卷引用:云南师范大学附属中学2023-2024学年高一上学期1月教学测评期末化学试题



