名校
1 . 下列用于解释事实的方程式书写不正确的是
A.新切开的钠的光亮表面在空气中很快变暗: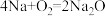 |
B.Fe3O4溶于过量稀硝酸中: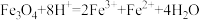 |
C.向AlC13溶液中滴加氨水产生白色沉淀: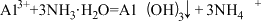 |
D.向AgCl悬浊液中滴加KI溶液产生黄色沉淀: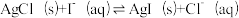 |
您最近一年使用:0次
名校
解题方法
2 . 过氧化氢(H2O2)是重要的化工产品,广泛应用于绿色化学合成。医疗消毒等领域。回答下列问题:
(1)已知: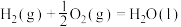
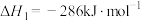
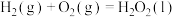
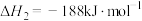
过氧化氢分解反应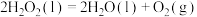 的
的
___________  。
。
(2)早期制备方法: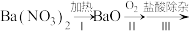 滤液
滤液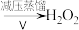
①I为分解反应,产物除BaO、 外,还有一种红棕色气体。该反应的化学方程式是
外,还有一种红棕色气体。该反应的化学方程式是___________ 。
②Ⅱ为可逆反应,写出一条促进该反应正向进行的措施是___________ 。
③Ⅲ中生成 ,反应的化学方程式是
,反应的化学方程式是___________ 。
④减压能够降低蒸馏温度,从 的化学性质角度说明V中采用减压蒸馏的原因:
的化学性质角度说明V中采用减压蒸馏的原因:________ 。
(1)已知:
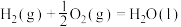
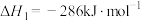
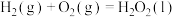
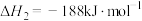
过氧化氢分解反应
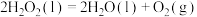 的
的
 。
。(2)早期制备方法:
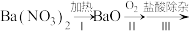 滤液
滤液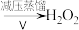
①I为分解反应,产物除BaO、
 外,还有一种红棕色气体。该反应的化学方程式是
外,还有一种红棕色气体。该反应的化学方程式是②Ⅱ为可逆反应,写出一条促进该反应正向进行的措施是
③Ⅲ中生成
 ,反应的化学方程式是
,反应的化学方程式是④减压能够降低蒸馏温度,从
 的化学性质角度说明V中采用减压蒸馏的原因:
的化学性质角度说明V中采用减压蒸馏的原因:
您最近一年使用:0次
名校
解题方法
3 . 氮及其化合物是科学家们一直在探究的问题,它们在工农业生产和生命活动中起着重要的作用。回答下列问题:
(1)N2和H2合成氨的化学方程式:________ ,该反应的
_______ 0(填“大于”、“小于”或“等于”)。
(2)氮循环是指氮在自然界中的循环转化过程,是生物圈内基本的物质循环之一,存在较多蓝、绿藻类的酸性水体中存在如下图所示的氮循环,请回答相关问题:
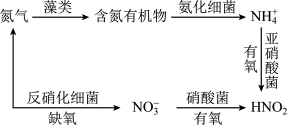
① 在亚硝酸菌作用下的硝化过程的离子方程式是
在亚硝酸菌作用下的硝化过程的离子方程式是___________ 。
②恒温时在亚硝酸菌的作用下发生该反应,能说明体系达到平衡状态的是___________ (填标号)。
A.溶液的pH不再改变
B. 的消耗速率和
的消耗速率和 的生成速率相等
的生成速率相等
C.溶液中 、
、 、
、 、
、 的总物质的量保持不变
的总物质的量保持不变
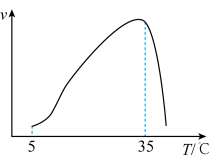
③实验测得在其它条件一定时, 硝化反应的速率随温度变化曲线如下图所示,温度高于35℃时反应速率迅速下降的原因可能是
硝化反应的速率随温度变化曲线如下图所示,温度高于35℃时反应速率迅速下降的原因可能是___________ 。
(3)硝酸工业的尾气成分主要是 ,通常利用
,通常利用 处理,将其转化为无毒物质后排放,该反应的化学方程式为
处理,将其转化为无毒物质后排放,该反应的化学方程式为___________ 。
(1)N2和H2合成氨的化学方程式:

(2)氮循环是指氮在自然界中的循环转化过程,是生物圈内基本的物质循环之一,存在较多蓝、绿藻类的酸性水体中存在如下图所示的氮循环,请回答相关问题:

①
 在亚硝酸菌作用下的硝化过程的离子方程式是
在亚硝酸菌作用下的硝化过程的离子方程式是②恒温时在亚硝酸菌的作用下发生该反应,能说明体系达到平衡状态的是
A.溶液的pH不再改变
B.
 的消耗速率和
的消耗速率和 的生成速率相等
的生成速率相等C.溶液中
 、
、 、
、 、
、 的总物质的量保持不变
的总物质的量保持不变③实验测得在其它条件一定时,
 硝化反应的速率随温度变化曲线如下图所示,温度高于35℃时反应速率迅速下降的原因可能是
硝化反应的速率随温度变化曲线如下图所示,温度高于35℃时反应速率迅速下降的原因可能是
(3)硝酸工业的尾气成分主要是
 ,通常利用
,通常利用 处理,将其转化为无毒物质后排放,该反应的化学方程式为
处理,将其转化为无毒物质后排放,该反应的化学方程式为
您最近一年使用:0次
2023-12-15更新
|
29次组卷
|
2卷引用:海南省海口市第四中学2023-2024学年高二上学期11月期中考试化学试题
名校
解题方法
4 . CuCl是一种重要化工原料,常用作催化剂、杀菌剂。化学小组利用下图装置(部分夹持装置略去)制备CuCl。

已知:①CuCl为白色固体,微溶于水,不溶于酒精,在空气中能被迅速氧化。
②CuCl能溶于氨水, 为无色。
为无色。
实验步骤:
Ⅰ.连接好仪器,检查装置气密性后加入药品。
Ⅱ.打开活塞K,通入一段时间 后,关闭活塞K。
后,关闭活塞K。
Ⅲ.打开仪器a的活塞,向三颈瓶中加盐酸调pH至2~3。
Ⅳ.打开活塞K,通入 ,溶液中产生白色沉淀,待反应完全后,再通一段时间的气体。
,溶液中产生白色沉淀,待反应完全后,再通一段时间的气体。
Ⅴ.将A中混合液过滤、洗涤、干燥得CuCl粗产品,纯化后得CuCl产品。
回答下列问题:
(1)步骤Ⅱ中反应前通入 的目的是
的目的是_______ 。
(2)仪器a的名称是_______ ,装置C的作用是_______ 。
(3)步骤Ⅳ中通入 发生反应的离子方程式
发生反应的离子方程式_______ 。
(4)步骤Ⅴ中用95%的乙醇代替蒸馏水洗涤的优点是_______ 。
(5)CuCl溶于氨水后的溶液遇到空气被氧化为深蓝色,深蓝色溶液中阳离子为_______ 。

已知:①CuCl为白色固体,微溶于水,不溶于酒精,在空气中能被迅速氧化。
②CuCl能溶于氨水,
 为无色。
为无色。实验步骤:
Ⅰ.连接好仪器,检查装置气密性后加入药品。
Ⅱ.打开活塞K,通入一段时间
 后,关闭活塞K。
后,关闭活塞K。Ⅲ.打开仪器a的活塞,向三颈瓶中加盐酸调pH至2~3。
Ⅳ.打开活塞K,通入
 ,溶液中产生白色沉淀,待反应完全后,再通一段时间的气体。
,溶液中产生白色沉淀,待反应完全后,再通一段时间的气体。Ⅴ.将A中混合液过滤、洗涤、干燥得CuCl粗产品,纯化后得CuCl产品。
回答下列问题:
(1)步骤Ⅱ中反应前通入
 的目的是
的目的是(2)仪器a的名称是
(3)步骤Ⅳ中通入
 发生反应的离子方程式
发生反应的离子方程式(4)步骤Ⅴ中用95%的乙醇代替蒸馏水洗涤的优点是
(5)CuCl溶于氨水后的溶液遇到空气被氧化为深蓝色,深蓝色溶液中阳离子为
您最近一年使用:0次
2023-12-14更新
|
45次组卷
|
2卷引用:海南省海口市第一中学2023-2024学年高二上学期11月期中考试化学试题
名校
解题方法
5 . SiCl4是生产多品硅的副产物。利用SiC14对废弃的锂电池正极材料LiCoO2进行氯化处理以回收Li、Co等金属,工艺路线如下:
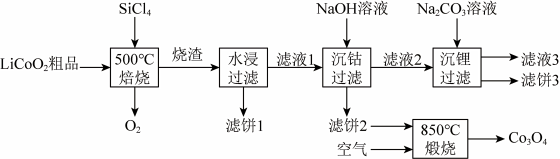
回答下列问题:
(1)Co位于元素周期表第__________ 周期第_________ 族。
(2)烧渣是LiC1、CoC12和SiO2的混合物,“500°C焙烧”后剩余的SiC14应先除去,否则水浸时会产生大量烟雾,用化学方程式表示其原因___________ 。
(3)鉴别洗净的“滤饼3”和固体Na2CO3常用方法的名称是___________ 。
(4)已知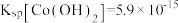 ,若“沉钻过滤”的pH控制为10.0,则溶液中Co2+浓度为
,若“沉钻过滤”的pH控制为10.0,则溶液中Co2+浓度为___________ mol·L-1。“850℃煅烧”时的化学方程式为___________ 。

回答下列问题:
(1)Co位于元素周期表第
(2)烧渣是LiC1、CoC12和SiO2的混合物,“500°C焙烧”后剩余的SiC14应先除去,否则水浸时会产生大量烟雾,用化学方程式表示其原因
(3)鉴别洗净的“滤饼3”和固体Na2CO3常用方法的名称是
(4)已知
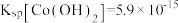 ,若“沉钻过滤”的pH控制为10.0,则溶液中Co2+浓度为
,若“沉钻过滤”的pH控制为10.0,则溶液中Co2+浓度为
您最近一年使用:0次
解题方法
6 . 用主要成分为 的矿石(杂质为
的矿石(杂质为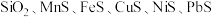 等)制取锰的流程如图所示。
等)制取锰的流程如图所示。

已知:流程中相关金属离子开始沉淀和完全沉淀的 如下:
如下:
(1)焙烧中 参与反应的化学方程式为
参与反应的化学方程式为___________ 。
(2)氧化过程中反应的离子方程式为___________ 。
(3)调 的目的是除去
的目的是除去 ,则
,则 的调控范围是
的调控范围是___________ ;加入 的目的是除去
的目的是除去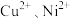 ,则除
,则除 转化的离子方程式为
转化的离子方程式为___________ 。
(4)电解中生成 的电极反应式为
的电极反应式为___________ 。
 的矿石(杂质为
的矿石(杂质为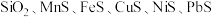 等)制取锰的流程如图所示。
等)制取锰的流程如图所示。
已知:流程中相关金属离子开始沉淀和完全沉淀的
 如下:
如下:| 金属离子 |  |  |  |  |  |
开始沉淀的 | 2.2 | 7.5 | 7.9 | 7.8 | 4.4 |
完全沉淀的 | 3.5 | 9.5 | 9.0 | 10.4 | 5.8 |
 参与反应的化学方程式为
参与反应的化学方程式为(2)氧化过程中反应的离子方程式为
(3)调
 的目的是除去
的目的是除去 ,则
,则 的调控范围是
的调控范围是 的目的是除去
的目的是除去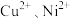 ,则除
,则除 转化的离子方程式为
转化的离子方程式为(4)电解中生成
 的电极反应式为
的电极反应式为
您最近一年使用:0次
解题方法
7 . 酸性条件下, 与过硫酸铵
与过硫酸铵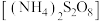 混合后可发生反应:
混合后可发生反应: 。下列有关说法错误的是
。下列有关说法错误的是
 与过硫酸铵
与过硫酸铵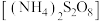 混合后可发生反应:
混合后可发生反应: 。下列有关说法错误的是
。下列有关说法错误的是| A.过硫酸铵发生还原反应,反应中硫元素得电子 |
B. |
C. 分别是“ 分别是“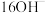 ”、“ ”、“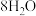 ” ” |
| D.过硫酸铵中硫元素显+6价 |
您最近一年使用:0次



