1 . 已知工业上制备氧缺位铁酸盐[ZnFe2Ox(3<x<4)]部分流程如图,该方法可实现硫、氮氧化合物的废气利用。

下列有关说法错误的是

下列有关说法错误的是
| A.ZnFe2O4中铁的价态为+3价 |
| B.除去SO2、NO2时,ZnFe2Ox在反应中表现了氧化性 |
| C.若使1molZnFe2Ox完全转化为ZnFe2O4,需失去(8-2x)mol电子 |
| D.ZnFe2O4与H2的反应要在无氧条件下进行 |
您最近一年使用:0次
2022-09-23更新
|
1821次组卷
|
10卷引用:宁夏石嘴山市平罗中学2022-2023学年高三上学期期中考试(重点班)化学试题
宁夏石嘴山市平罗中学2022-2023学年高三上学期期中考试(重点班)化学试题百师联盟2023届高三上学期一轮复习联考(全国卷)化学试题江苏省徐州市王杰中学2022-2023学年高三上学期10月阶段检测化学试题重庆市礼嘉中学校2022-2023学年高一上学期第一次月考化学试题浙江省杭州第二中学2022-2023学年高一上学期期中考试化学试题(已下线)热点情景汇编-专题三 氧化还原中的化学山东省菏泽第一中学2022-2023学年高一上学期期末考试化学试题(已下线)【2022】【高一化学】【期中考】-181(已下线)【2022】【高一上】【期中考】【杭二东河】【高中化学】【徐外兰收集】江苏省灌南高级中学2023-2024学年高三上学期暑期检测(二)化学试题
2 . 阅读下面一段材料并回答问题。
(1) 中铁元素的化合价为
中铁元素的化合价为_______ 。
(2)制备 需要在
需要在_______ (填“酸性”、“碱性”或“中性”)环境中进行。
(3)下列关于 的说法中,不正确的是
的说法中,不正确的是_______ 。
a.是强氧化性的盐 b.固体保存需要防潮
c.其消毒和净化水的原理相同 d.其净水优点有:作用快、安全性好、无异味
(4)消毒净化 水,至少需要
水,至少需要 的质量为
的质量为_______ kg。
(5)高铁酸钠 是一种新型的净水剂,可以通过下述反应制取:
是一种新型的净水剂,可以通过下述反应制取:
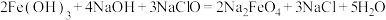
①该反应中氧化剂是_____ (用化学式表示,下同),____ 元素被氧化,还原产物为____ 。
②用双线桥法在方程式中标出电子转移的情况:_____ 。
(6)将 与水反应的化学方程式补充完整并用双线桥表示出电子转移的方向和数目
与水反应的化学方程式补充完整并用双线桥表示出电子转移的方向和数目____ 。
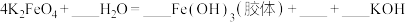
| 高铁酸钾使用说明书 【化学式】  【性状】暗紫色具有金属光泽的粉末,无臭无味 【产品特点】干燥品在室温下稳定,在强碱溶液中稳定,随着pH减小,稳定性下降,与水反应放出氧气  通过强烈的氧化作用可迅速杀灭细菌,有消毒作用,同时不会产生有害物质。 通过强烈的氧化作用可迅速杀灭细菌,有消毒作用,同时不会产生有害物质。 与水反应还能产生具有强吸附性的 与水反应还能产生具有强吸附性的 胶体,可除去水中细微的悬浮物,有净水作用 胶体,可除去水中细微的悬浮物,有净水作用【用途】主要用于饮用水消毒净化、城市生活污水和工业污水处理 【用量】消毒净化1L水投放5mg  ,即可达到卫生标准 ,即可达到卫生标准…… |
(1)
 中铁元素的化合价为
中铁元素的化合价为(2)制备
 需要在
需要在(3)下列关于
 的说法中,不正确的是
的说法中,不正确的是a.是强氧化性的盐 b.固体保存需要防潮
c.其消毒和净化水的原理相同 d.其净水优点有:作用快、安全性好、无异味
(4)消毒净化
 水,至少需要
水,至少需要 的质量为
的质量为(5)高铁酸钠
 是一种新型的净水剂,可以通过下述反应制取:
是一种新型的净水剂,可以通过下述反应制取: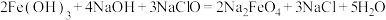
①该反应中氧化剂是
②用双线桥法在方程式中标出电子转移的情况:
(6)将
 与水反应的化学方程式补充完整并用双线桥表示出电子转移的方向和数目
与水反应的化学方程式补充完整并用双线桥表示出电子转移的方向和数目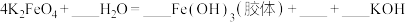
您最近一年使用:0次
解题方法
3 . 氧化剂和还原剂在生产生活中广泛使用。
(1)高锰酸钾和氢溴酸溶液可以发生如下反应:2KMnO4+16HBr=2KBr+2MnBr2+8H2O+5Br2
①其中还原剂为_________ ,还原产物为_________ (均填化学式)
②若消耗0.1mol氧化剂,则被氧化的还原剂的物质的量为_________ ,转移电子的数目是_________ 。
③用线桥表示转移电子的数目_________________________________ 。
(2)人体内所含铁元素以Fe2+和Fe3+的形式存在。市场出售的某种麦片中含有微量的颗粒细小的还原铁粉,这些铁粉在人体胃酸的作用下转化成亚铁盐,此反应的离子方程式为____________________ ,但Fe2+在酸性条件下很容易被空气中的氧气氧化,写出该反应的离子方程式_________________________________ 。
(3)次磷酸(H3PO2)是一种精细化工产品,具有较强还原性,H3PO2及NaH2PO2均可将溶液中的银离子还原为银单质,从而用于化学镀银。利用(H3PO2)进行化学镀银反应中,氧化剂与还原剂的物质的量之比为4︰1,则氧化产物为:_________ 。
A.PH3 B.H3PO3 C.P D.H3PO4
(1)高锰酸钾和氢溴酸溶液可以发生如下反应:2KMnO4+16HBr=2KBr+2MnBr2+8H2O+5Br2
①其中还原剂为
②若消耗0.1mol氧化剂,则被氧化的还原剂的物质的量为
③用线桥表示转移电子的数目
(2)人体内所含铁元素以Fe2+和Fe3+的形式存在。市场出售的某种麦片中含有微量的颗粒细小的还原铁粉,这些铁粉在人体胃酸的作用下转化成亚铁盐,此反应的离子方程式为
(3)次磷酸(H3PO2)是一种精细化工产品,具有较强还原性,H3PO2及NaH2PO2均可将溶液中的银离子还原为银单质,从而用于化学镀银。利用(H3PO2)进行化学镀银反应中,氧化剂与还原剂的物质的量之比为4︰1,则氧化产物为:
A.PH3 B.H3PO3 C.P D.H3PO4
您最近一年使用:0次
名校
解题方法
4 . 高铁酸钾(K2FeO4)是一种新型,高效、多功能绿色水处理剂,可通过KClO溶液与Fe(NO3)3溶液的反应制备。已知:①KClO在较高温度下发生歧化反应生成KClO3。②K2FeO4具有下列性质:可溶于水、微溶于浓KOH溶液;在强碱性溶液中比较稳定;在Fe3+催化作用下发生分解,在酸性至弱碱性条件下,能与水反应生成Fe(OH)3和O2,如图所示是实验室模拟工业制备KClO溶液装置。______ ;
(2)反应时需将C装置置于冷水浴中,其原因为______ ;
(3)制备K2FeO4时,不能将碱性的KClO溶液滴加到Fe(NO3)3饱和溶液中,其原因是______ ,制备K2FeO4的离子方程式______ ;
(4)工业上常用废铁屑为原料制备Fe(NO3)3溶液,检验Fe3+所需试剂名称______ ,其反应原理为______ (用离子方程式表示);
(5)向反应后的三颈瓶中加入饱和KOH溶液,析出K2FeO4固体,过滤、洗涤、干燥。洗涤操作所用最佳试剂为______ ;
A.水 B.无水乙醇 C.稀KOH溶液
(6)工业上用“间接碘量法”测定高铁酸钾的纯度:用碱性KI溶液溶解1.00g K2FeO4样品,调节pH使高铁酸根全部被还原成亚铁离子,再调节pH为3~4,用1.0mol/L的Na2S2O3标准溶液作为滴定剂进行滴定(2Na2S2O3+I2=Na2S4O6+2NaI),淀粉作指示剂,装有Na2S2O3标准溶液的滴定管起始和终点读数如如图所示:______ mL。
②原样品中高铁酸钾的质量分数为______ 。[M(K2FeO4)=198g/mol]
③若在配制Na2S2O3标准溶液的过程中定容时俯视刻度线,则导致所测高铁酸钾的质量分数______ (填“偏高”、“偏低”或“无影响”)。
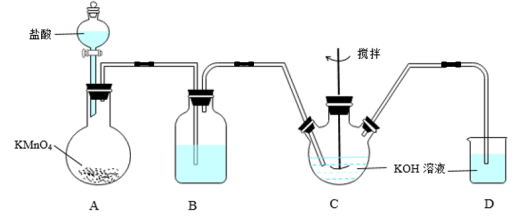
(2)反应时需将C装置置于冷水浴中,其原因为
(3)制备K2FeO4时,不能将碱性的KClO溶液滴加到Fe(NO3)3饱和溶液中,其原因是
(4)工业上常用废铁屑为原料制备Fe(NO3)3溶液,检验Fe3+所需试剂名称
(5)向反应后的三颈瓶中加入饱和KOH溶液,析出K2FeO4固体,过滤、洗涤、干燥。洗涤操作所用最佳试剂为
A.水 B.无水乙醇 C.稀KOH溶液
(6)工业上用“间接碘量法”测定高铁酸钾的纯度:用碱性KI溶液溶解1.00g K2FeO4样品,调节pH使高铁酸根全部被还原成亚铁离子,再调节pH为3~4,用1.0mol/L的Na2S2O3标准溶液作为滴定剂进行滴定(2Na2S2O3+I2=Na2S4O6+2NaI),淀粉作指示剂,装有Na2S2O3标准溶液的滴定管起始和终点读数如如图所示:
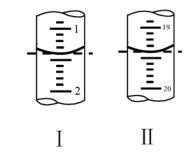
②原样品中高铁酸钾的质量分数为
③若在配制Na2S2O3标准溶液的过程中定容时俯视刻度线,则导致所测高铁酸钾的质量分数
您最近一年使用:0次
2021-02-02更新
|
109次组卷
|
2卷引用:宁夏海原县第一中学2021届高三上学期期末考试化学试题
名校
5 . 氯酸是一种强酸,浓度超过 40%时会发生分解,反应可表示为 aHClO3=bO2↑+ cCl2↑+ dHClO4 + eH2O,用湿润的淀粉碘化钾试纸检验气体产物时,试纸先变蓝后褪色。下列说法正确的是
| A.若化学计量数 a = 8,b = 3,则该反应转移电子为 20e- |
| B.变蓝的淀粉碘化钾试纸褪色是因为可能发生了:4Cl2+I2 + 6H2O=12H++8Cl-+2IO3- |
| C.氧化产物是高氯酸和氯气 |
| D.由反应可确定:氧化性:HClO4>HClO3 |
您最近一年使用:0次
2019-11-05更新
|
212次组卷
|
4卷引用:宁夏石嘴山市第三中学2022-2023学年高三上学期期中考试化学试题
宁夏石嘴山市第三中学2022-2023学年高三上学期期中考试化学试题山西省吕梁市2020届高三10月模拟化学试题2020届高三化学二轮冲刺新题专练——氯及其化合物(已下线)专题39 氯的氧化物、含氧酸及含氧酸盐-2022年高考化学毕业班二轮热点题型归纳与变式演练(全国通用)
名校
6 . 高铁酸钾 (K2FeO4)是一种新型、高效、多功能水处理剂,是比Cl2、O3、ClO2、KMnO4氧化性更强,无二次污染的绿色水处理剂。工业是先制得高铁酸钠,然后在低温下,在高铁酸钠溶液中加入KOH至饱和就可析出高铁酸钾(K2FeO4)。湿法制备的主要反应方程为:2Fe(OH)3+3ClO-+4OH-=2FeO42- +3Cl-+5H2O,干法制备的主要反应方程为:2FeSO4 +6Na2O2 = 2Na2FeO4 +2Na2O +2Na2SO4 +O2↑ 下列有关说法不正确的是
| A.低温下,高铁酸钾的溶解度比高铁酸钠更小 |
| B.湿法制备中每生成1mol Na2FeO4 转移3mol电子 |
| C.干法制备中还原剂与氧化剂的物质的量之比为1:3 |
| D.K2FeO4处理水时,不仅能消毒杀菌,还能除去水体中的H2S、NH3等,生成的Fe(OH)3胶体还能吸附水中的悬浮杂质 |
您最近一年使用:0次
名校
7 . 已知某一反应2H2CrO4+3H2O2=2Cr(OH)3+3O2↑+2H2O,则关于该反应的说法错误的是( )
| A.H2CrO4中铬元素显+6价 |
| B.该反应中的还原剂是H2O2,氧化产物是O2 |
| C.氧化性:H2CrO4>O2 |
| D.如反应转移了0.3mol电子,则产生的气体在标准状况下体积为1.68L |
您最近一年使用:0次
2018-11-12更新
|
128次组卷
|
3卷引用:【全国百强校】宁夏回族自治区银川一中2018-2019学年高一上学期期中考试化学试题



