名校
1 . 二氯化二硫( )是一种常用的橡胶硫化剂,其结构如图所示。
)是一种常用的橡胶硫化剂,其结构如图所示。 极易水解:
极易水解: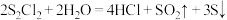 。下列说法错误的是
。下列说法错误的是
 )是一种常用的橡胶硫化剂,其结构如图所示。
)是一种常用的橡胶硫化剂,其结构如图所示。 极易水解:
极易水解: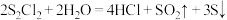 。下列说法错误的是
。下列说法错误的是
A. 中S为+1价 中S为+1价 |
B. 是由非极性键与极性键构成的极性分子 是由非极性键与极性键构成的极性分子 |
C.上述反应中 既作氧化剂又作还原剂 既作氧化剂又作还原剂 |
| D.上述反应中氧化产物与还原产物的质量比为3:1 |
您最近一年使用:0次
名校
解题方法
2 . 以下是一系列非金属元素间的置换反应,其中不能说明反应前的非金属单质的氧化性强于产物中非金属单质的氧化性的是
A. | B.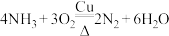 |
C. | D. |
您最近一年使用:0次
名校
3 . 回答下列问题:
(1)一种新型的人工固氮原理如图a所示,该过程中属于氧化还原反应的是_________ (填反应编号)。_________ 。
(3)SCR和NSR技术可有效降低柴油发动机在空气过量条件下的NOx排放,SCR(选择性催化还原)工作原理如图b所示,NSR(NOx储存还原)工作原理如图c所示。_________ 。
②SCR催化过程中,当燃油中含硫量较高时,尾气中SO2在O2作用下会形成(NH4)2SO4,使催化剂中毒,用化学方程式表示(NH4)2SO4的形成:_________ 。
③NSR转化中,通过BaO和Ba(NO3)2的相互转化实现NOx的储存和还原,其中储存NOx的物质是_________ 。
④用H2模拟尾气中还原性气体研究了Ba(NO3)2的催化还原过程,该过程分两步进行,图d表示该过程相关物质浓度随时间的变化关系,第一步反应中消耗的H2与Ba(NO3)2的物质的量之比是_________ 。
经过简单猜测,小组成员认为该氮肥的有效成分为铵盐,为了验证猜想,他们取了少量氮肥配制为溶液,后续应当进行的操作为_________ 。
(1)一种新型的人工固氮原理如图a所示,该过程中属于氧化还原反应的是

(3)SCR和NSR技术可有效降低柴油发动机在空气过量条件下的NOx排放,SCR(选择性催化还原)工作原理如图b所示,NSR(NOx储存还原)工作原理如图c所示。

②SCR催化过程中,当燃油中含硫量较高时,尾气中SO2在O2作用下会形成(NH4)2SO4,使催化剂中毒,用化学方程式表示(NH4)2SO4的形成:
③NSR转化中,通过BaO和Ba(NO3)2的相互转化实现NOx的储存和还原,其中储存NOx的物质是
④用H2模拟尾气中还原性气体研究了Ba(NO3)2的催化还原过程,该过程分两步进行,图d表示该过程相关物质浓度随时间的变化关系,第一步反应中消耗的H2与Ba(NO3)2的物质的量之比是

经过简单猜测,小组成员认为该氮肥的有效成分为铵盐,为了验证猜想,他们取了少量氮肥配制为溶液,后续应当进行的操作为
您最近一年使用:0次
2024-04-10更新
|
172次组卷
|
2卷引用:江苏省南京市金陵中学2023-2024学年高一下学期3月月考化学试题
4 . 消除氮氧化物尾气和水中硝酸盐造成的氮污染已成为环境修复研究的热点。
(1)氧化吸收法
酸性条件下,加入 溶液可以氧化
溶液可以氧化 和
和 等生成
等生成 和
和 。其他条件一定,
。其他条件一定, 转化为
转化为 的转化率随水体溶液初始
的转化率随水体溶液初始 的变化如图1所示。
的变化如图1所示。

①在酸性水体中,加入 溶液吸收
溶液吸收 的离子方程式为
的离子方程式为_________ 。
②水体浴液初始 越小,
越小, 转化率越高。其原因是
转化率越高。其原因是_________ 。
③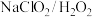 酸性复合吸收剂可有效去除
酸性复合吸收剂可有效去除 。复合吸收剂组成一定时,温度对
。复合吸收剂组成一定时,温度对 去除率的影响如图2。温度高于
去除率的影响如图2。温度高于 后,NO去除率下降的主要原因是
后,NO去除率下降的主要原因是_________ 。
(2)催化还原法
①在W-Cu/ 的催化条件下,使用
的催化条件下,使用 作为还原剂,可将水中的
作为还原剂,可将水中的 转化为
转化为 。该反应机理分为三步,如图3所示:第一步:
。该反应机理分为三步,如图3所示:第一步: 在
在 表面被还原为
表面被还原为 被氧化为
被氧化为 ;第二步:
;第二步: 从
从 表面迁移至
表面迁移至 的表面;第三步:
的表面;第三步: 在
在 表面吸附并解离为活性氢原子(W-H),
表面吸附并解离为活性氢原子(W-H),_________ 。(补充完整该步反应机理)

(1)氧化吸收法
酸性条件下,加入
 溶液可以氧化
溶液可以氧化 和
和 等生成
等生成 和
和 。其他条件一定,
。其他条件一定, 转化为
转化为 的转化率随水体溶液初始
的转化率随水体溶液初始 的变化如图1所示。
的变化如图1所示。
①在酸性水体中,加入
 溶液吸收
溶液吸收 的离子方程式为
的离子方程式为②水体浴液初始
 越小,
越小, 转化率越高。其原因是
转化率越高。其原因是③
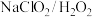 酸性复合吸收剂可有效去除
酸性复合吸收剂可有效去除 。复合吸收剂组成一定时,温度对
。复合吸收剂组成一定时,温度对 去除率的影响如图2。温度高于
去除率的影响如图2。温度高于 后,NO去除率下降的主要原因是
后,NO去除率下降的主要原因是(2)催化还原法
①在W-Cu/
 的催化条件下,使用
的催化条件下,使用 作为还原剂,可将水中的
作为还原剂,可将水中的 转化为
转化为 。该反应机理分为三步,如图3所示:第一步:
。该反应机理分为三步,如图3所示:第一步: 在
在 表面被还原为
表面被还原为 被氧化为
被氧化为 ;第二步:
;第二步: 从
从 表面迁移至
表面迁移至 的表面;第三步:
的表面;第三步: 在
在 表面吸附并解离为活性氢原子(W-H),
表面吸附并解离为活性氢原子(W-H),
②若改用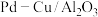 作为还原硝酸盐过程的催化剂,其催化机理与W-Cu/
作为还原硝酸盐过程的催化剂,其催化机理与W-Cu/ 相似。但还原过程中检测到三种含氮化合物微粒,其浓度变化如图4所示,在1.5~2.5h过程中,硝酸根
相似。但还原过程中检测到三种含氮化合物微粒,其浓度变化如图4所示,在1.5~2.5h过程中,硝酸根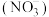 部分转化为
部分转化为 的可能原因是
的可能原因是
您最近一年使用:0次
名校
解题方法
5 . 土壤中的 在硝化细菌的作用下转化为
在硝化细菌的作用下转化为 后,土壤中的
后,土壤中的 进一步将
进一步将 氧化为
氧化为 。在氧气较少的环境下,
。在氧气较少的环境下, 又可以在反硝化细菌的作用下与
又可以在反硝化细菌的作用下与 反应,使氮以
反应,使氮以 形式放出。下列说法
形式放出。下列说法不正确 的是
 在硝化细菌的作用下转化为
在硝化细菌的作用下转化为 后,土壤中的
后,土壤中的 进一步将
进一步将 氧化为
氧化为 。在氧气较少的环境下,
。在氧气较少的环境下, 又可以在反硝化细菌的作用下与
又可以在反硝化细菌的作用下与 反应,使氮以
反应,使氮以 形式放出。下列说法
形式放出。下列说法A. 被氧化为 被氧化为 的过程中, 的过程中, 与 与 的物质的量之比为 的物质的量之比为 |
B.在反硝化过程中,土壤 降低 降低 |
C. 与 与 反应时,每生成 反应时,每生成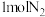 ,转移电子数为 ,转移电子数为 |
| D.适当疏松土壤,有利于提高铵态氮肥的肥效 |
您最近一年使用:0次
名校
解题方法
6 . 某兴趣小组以海藻灰(主要成分是 )为原料进行
)为原料进行 的制备实验。具体步骤如下:将海菜灰浸泡加热过滤后,得到
的制备实验。具体步骤如下:将海菜灰浸泡加热过滤后,得到 溶液,将适量
溶液,将适量 固体溶于
固体溶于 溶液,再将
溶液,再将 饱和溶液滴入上述溶液中,生成白色
饱和溶液滴入上述溶液中,生成白色 ,向白色沉淀中边搅拌边滴入适量浓硝酸得
,向白色沉淀中边搅拌边滴入适量浓硝酸得 。下列有关反应的离子方程式正确的是
。下列有关反应的离子方程式正确的是
 )为原料进行
)为原料进行 的制备实验。具体步骤如下:将海菜灰浸泡加热过滤后,得到
的制备实验。具体步骤如下:将海菜灰浸泡加热过滤后,得到 溶液,将适量
溶液,将适量 固体溶于
固体溶于 溶液,再将
溶液,再将 饱和溶液滴入上述溶液中,生成白色
饱和溶液滴入上述溶液中,生成白色 ,向白色沉淀中边搅拌边滴入适量浓硝酸得
,向白色沉淀中边搅拌边滴入适量浓硝酸得 。下列有关反应的离子方程式正确的是
。下列有关反应的离子方程式正确的是A.生成白色沉淀的反应为: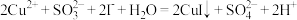 |
B. 固体中加入适量浓硝酸: 固体中加入适量浓硝酸: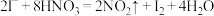 |
C. 中加入过量盐酸: 中加入过量盐酸: |
D. 溶液与氢氧化钡溶液混合: 溶液与氢氧化钡溶液混合: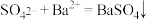 |
您最近一年使用:0次
2024-03-23更新
|
274次组卷
|
2卷引用:江苏省南京市第一中学2023-2024学年高一下学期3月月考化学试题
名校
解题方法
7 . 向含Fe2+、I-、Br-的溶液中通入过量的氯气,溶液中四种粒子的物质的量变化如图所示,已知b-a=5,线段IV表示一种含氧酸,且Ⅰ和Ⅳ表示的物质中含有相同的元素。下列说法不正确的是

| A.原溶液中n(FeBr2):n(FeI2)=1:3 |
| B.线段Ⅱ表示Fe2+的变化情况 |
C.线段Ⅳ表示IO 的变化情况 的变化情况 |
| D.根据图像可计算出a=6 |
您最近一年使用:0次
名校
8 . 氧及其化合物具有广泛用途。 是常用的氧化剂,
是常用的氧化剂, 的燃烧热为
的燃烧热为 ,氧炔焰产生的高温可用于焊接金属。
,氧炔焰产生的高温可用于焊接金属。 可用于水处理,pH约为8时,
可用于水处理,pH约为8时, 可与
可与 反应生成
反应生成 、
、 和
和 。
。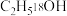 可用于研究酯化反应的机理。CaO可用于烟气(含
可用于研究酯化反应的机理。CaO可用于烟气(含 、
、 、
、 、
、 等)脱硫。
等)脱硫。 是一种绿色氧化剂,电解
是一种绿色氧化剂,电解 饱和溶液产生的
饱和溶液产生的 经水解可制得
经水解可制得 。下列物质结构与性质或物质性质与用途具有对应关系的是
。下列物质结构与性质或物质性质与用途具有对应关系的是
 是常用的氧化剂,
是常用的氧化剂, 的燃烧热为
的燃烧热为 ,氧炔焰产生的高温可用于焊接金属。
,氧炔焰产生的高温可用于焊接金属。 可用于水处理,pH约为8时,
可用于水处理,pH约为8时, 可与
可与 反应生成
反应生成 、
、 和
和 。
。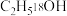 可用于研究酯化反应的机理。CaO可用于烟气(含
可用于研究酯化反应的机理。CaO可用于烟气(含 、
、 、
、 、
、 等)脱硫。
等)脱硫。 是一种绿色氧化剂,电解
是一种绿色氧化剂,电解 饱和溶液产生的
饱和溶液产生的 经水解可制得
经水解可制得 。下列物质结构与性质或物质性质与用途具有对应关系的是
。下列物质结构与性质或物质性质与用途具有对应关系的是A. 分子中含共价三键, 分子中含共价三键, 的沸点比 的沸点比 的低 的低 |
B. 分子之间形成氢键,可与水任意比例互溶 分子之间形成氢键,可与水任意比例互溶 |
C. 具有氧化性,可作为燃料电池的氧化剂 具有氧化性,可作为燃料电池的氧化剂 |
D. 的溶解度比 的溶解度比 大,可用于饮用水消毒杀菌 大,可用于饮用水消毒杀菌 |
您最近一年使用:0次
2023-09-11更新
|
305次组卷
|
2卷引用:江苏省南京市南京师范大学附属中学2023-2024 学年高三9月考试化学试题
名校
解题方法
9 . ①向蓝色的 溶液中滴加酸性
溶液中滴加酸性 溶液,溶液由蓝色变为淡黄色
溶液,溶液由蓝色变为淡黄色 ;②向
;②向 溶液中滴加浓盐酸产生黄绿色气体
溶液中滴加浓盐酸产生黄绿色气体 ,溶液变蓝,下列有关说法正确的是
,溶液变蓝,下列有关说法正确的是
 溶液中滴加酸性
溶液中滴加酸性 溶液,溶液由蓝色变为淡黄色
溶液,溶液由蓝色变为淡黄色 ;②向
;②向 溶液中滴加浓盐酸产生黄绿色气体
溶液中滴加浓盐酸产生黄绿色气体 ,溶液变蓝,下列有关说法正确的是
,溶液变蓝,下列有关说法正确的是| A.①中还原剂与氧化剂物质的量之比为1:5 |
B.由①②可知,酸性条件下氧化性: |
C.②中每生成 分子,转移2mol电子 分子,转移2mol电子 |
D.向 溶液中滴加 溶液中滴加 溶液发生反应 溶液发生反应 |
您最近一年使用:0次
2024-01-24更新
|
136次组卷
|
2卷引用:江苏省南京市金陵中学2023-2024学年高一上学期期中化学试卷
名校
10 . 工业废气中的 的脱除是目前学术界研究的热点。
的脱除是目前学术界研究的热点。
I.某研究小组用新型 催化剂对
催化剂对 、
、 催化转化进行研究,测得一段时间内
催化转化进行研究,测得一段时间内 的转化率、
的转化率、 剩余的百分率随温度变化情况如下图所示。已知NO可发生下列反应:
剩余的百分率随温度变化情况如下图所示。已知NO可发生下列反应:
反应I: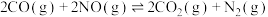

反应Ⅱ:


○:无CO且无催化剂时 直接分解成
直接分解成 的转化率
的转化率
△: 时,
时, 转化为
转化为 的转化率
的转化率
□: 时,
时, 的剩余百分率
的剩余百分率
(1)无 且无催化剂时,在
且无催化剂时,在 以上,随着温度的升高,
以上,随着温度的升高, 的转化率不断降低,其可能原因是
的转化率不断降低,其可能原因是___________ 。
(2) 时,该催化剂脱除
时,该催化剂脱除 的最适宜温度在
的最适宜温度在___________ ℃左右。
(3) ,初始
,初始 ,且不考虑除反应
,且不考虑除反应 、反应Ⅱ之外的反应时,反应相同时间后体系内
、反应Ⅱ之外的反应时,反应相同时间后体系内
___________ 。
(4) 条件下,温度高于
条件下,温度高于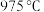 时,随着温度的升高,
时,随着温度的升高, 的转化率迅速降低,其可能原因是
的转化率迅速降低,其可能原因是___________ 。
Ⅱ.在 催化剂中,起催化作用的
催化剂中,起催化作用的 被负载于纳米
被负载于纳米 颗粒上。将含有
颗粒上。将含有 的尾气与空气、氨气按一定比例通入已知催化体系中,已知反应过程如下图所示:
的尾气与空气、氨气按一定比例通入已知催化体系中,已知反应过程如下图所示:

(5)根据上图所示反应过程,请推断过程I中 的化合价如何变化
的化合价如何变化 :反应前
:反应前___________ 价,反应后___________ 价。
(6)请写出NO被催化还原的总反应方程式___________ 。
 的脱除是目前学术界研究的热点。
的脱除是目前学术界研究的热点。I.某研究小组用新型
 催化剂对
催化剂对 、
、 催化转化进行研究,测得一段时间内
催化转化进行研究,测得一段时间内 的转化率、
的转化率、 剩余的百分率随温度变化情况如下图所示。已知NO可发生下列反应:
剩余的百分率随温度变化情况如下图所示。已知NO可发生下列反应:反应I:
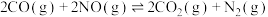

反应Ⅱ:



○:无CO且无催化剂时
 直接分解成
直接分解成 的转化率
的转化率△:
 时,
时, 转化为
转化为 的转化率
的转化率□:
 时,
时, 的剩余百分率
的剩余百分率(1)无
 且无催化剂时,在
且无催化剂时,在 以上,随着温度的升高,
以上,随着温度的升高, 的转化率不断降低,其可能原因是
的转化率不断降低,其可能原因是(2)
 时,该催化剂脱除
时,该催化剂脱除 的最适宜温度在
的最适宜温度在(3)
 ,初始
,初始 ,且不考虑除反应
,且不考虑除反应 、反应Ⅱ之外的反应时,反应相同时间后体系内
、反应Ⅱ之外的反应时,反应相同时间后体系内
(4)
 条件下,温度高于
条件下,温度高于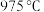 时,随着温度的升高,
时,随着温度的升高, 的转化率迅速降低,其可能原因是
的转化率迅速降低,其可能原因是Ⅱ.在
 催化剂中,起催化作用的
催化剂中,起催化作用的 被负载于纳米
被负载于纳米 颗粒上。将含有
颗粒上。将含有 的尾气与空气、氨气按一定比例通入已知催化体系中,已知反应过程如下图所示:
的尾气与空气、氨气按一定比例通入已知催化体系中,已知反应过程如下图所示:
(5)根据上图所示反应过程,请推断过程I中
 的化合价如何变化
的化合价如何变化 :反应前
:反应前(6)请写出NO被催化还原的总反应方程式
您最近一年使用:0次



