名校
解题方法
1 . 研究不同价态硫元素之间的转化是合理利用硫元素的基本途径。
I.以下是硫元素形成物质的“价—类”二维图及含硫物质相互转化的部分信息。
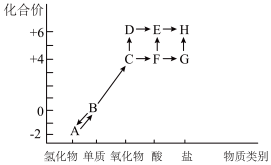
(1)G是一种由四种元素组成的钠盐,它的电离方程式是___________ 。
(2)C有毒,实验室可以用过量的NaOH溶液吸收,反应的离子方程式是___________ 。
(3)检验H中阴离子的实验操作及现象是_____________ 。
(4)C→F→E是造成酸雨的可能途径,请写出其中的化学方程式___________ 。
II.某小组同学设计实验实现几种价态硫元素的转化。可选用的实验药品如下:①Na2SO3溶液②浓硫酸③Na2S溶液④稀硫酸⑤酸性KMnO4溶液⑥品红溶液⑦铜片
(5)实验i选择的试剂是①和___________ (填序号),证明实现转化的现象是___________ ,该转化利用了Na2SO3的___________ 性。
(6)实验ii实现了-2价S向0价S的转化,相应的离子方程式为_____________ 。
I.以下是硫元素形成物质的“价—类”二维图及含硫物质相互转化的部分信息。

(1)G是一种由四种元素组成的钠盐,它的电离方程式是
(2)C有毒,实验室可以用过量的NaOH溶液吸收,反应的离子方程式是
(3)检验H中阴离子的实验操作及现象是
(4)C→F→E是造成酸雨的可能途径,请写出其中的化学方程式
II.某小组同学设计实验实现几种价态硫元素的转化。可选用的实验药品如下:①Na2SO3溶液②浓硫酸③Na2S溶液④稀硫酸⑤酸性KMnO4溶液⑥品红溶液⑦铜片
| 实验序号 | 预期转化 | 选择试剂(填序号) | 证明实现转化的现象 |
| i |  → → | ||
| ii | ①、③、④ | 淡黄色沉淀 | |
| iii |  → → | ②、⑦、⑥ |
(5)实验i选择的试剂是①和
(6)实验ii实现了-2价S向0价S的转化,相应的离子方程式为
您最近一年使用:0次
2023-12-19更新
|
299次组卷
|
3卷引用:第3课时 不同价态含硫物质的转化
解题方法
2 . 实验证明,以下六种物质是一个氧化还原反应的反应物和生成物:NO、 、
、 、
、 、
、 和
和 。
。
(1)这六种物质中,_______ 是反应物,_______ 是生成物。
(2)反应物中,氧化剂是_______ ,被还原的元素是_______ 。
 、
、 、
、 、
、 和
和 。
。(1)这六种物质中,
(2)反应物中,氧化剂是
您最近一年使用:0次
3 . 为探究 的性质,某学习小组进行了如下探究。
的性质,某学习小组进行了如下探究。
(1)向制得的 溶液中加入铁粉,其目的是
溶液中加入铁粉,其目的是_______ 。
(2)预测 既有氧化性又有还原性。你认为预测的依据是
既有氧化性又有还原性。你认为预测的依据是_______ 。
(3)进行实验探究。实验室提供了下列试剂: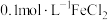 溶液、
溶液、 溶液、新制氯水、KSCN溶液、锌片、铜片。
溶液、新制氯水、KSCN溶液、锌片、铜片。
①向 溶液中滴入新制氯水,探究的是
溶液中滴入新制氯水,探究的是 的
的_______ 性(填“氧化”或“还原”),所发生反应的离子方程式为_______ 。
②在实验中,甲同学发现现象不太明显,老师分析可能是反应产物的含量太低,建议通过检验 反应产物的存在以获取证据。可选
反应产物的存在以获取证据。可选_______ 滴入甲同学所得的混合溶液中,并通过溶液出现_______ 的现象证明 具有还原性,能被氯水氧化。
具有还原性,能被氯水氧化。
③设计实验证明 具有氧化性:
具有氧化性:_______ 。
 的性质,某学习小组进行了如下探究。
的性质,某学习小组进行了如下探究。(1)向制得的
 溶液中加入铁粉,其目的是
溶液中加入铁粉,其目的是(2)预测
 既有氧化性又有还原性。你认为预测的依据是
既有氧化性又有还原性。你认为预测的依据是(3)进行实验探究。实验室提供了下列试剂:
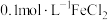 溶液、
溶液、 溶液、新制氯水、KSCN溶液、锌片、铜片。
溶液、新制氯水、KSCN溶液、锌片、铜片。①向
 溶液中滴入新制氯水,探究的是
溶液中滴入新制氯水,探究的是 的
的②在实验中,甲同学发现现象不太明显,老师分析可能是反应产物的含量太低,建议通过检验
 反应产物的存在以获取证据。可选
反应产物的存在以获取证据。可选 具有还原性,能被氯水氧化。
具有还原性,能被氯水氧化。③设计实验证明
 具有氧化性:
具有氧化性:
您最近一年使用:0次
2022-11-25更新
|
220次组卷
|
2卷引用:2019版鲁科化学必修第一册第3章第1节 铁的多样性课后习题
名校
解题方法
4 . 下列物质中,可与Fe3+反应且能证明Fe3+具有氧化性的是
| A.KSCN | B.NaOH | C.H2SO4 | D.Fe |
您最近一年使用:0次
2021-12-30更新
|
316次组卷
|
3卷引用:2019版鲁科化学必修第一册第3章总结与检测课后习题
5 . 某小组同学研究FeSO4的性质,经历如下研究过程:
预测:从FeSO4的类别角度,预测其可能与某些金属、酸、碱、盐发生反应;聚焦FeSO4中的Fe元素作为核心元素,预测FeSO4既具有氧化性,又具有还原性。
(1)从FeSO4的元素组成看,它的物质类别是_______________ 。
(2)预测其具有还原性的思路是____________________ 。
实验和观察:该小组同学分别实施以下实验。
(3)实验①的目的是___________ ,观察到现象:_______________ ,可证明预测成立。FeSO4发生反应的离子方程式是______________ 。
(4)实验②中的现象是___________________ 。
(5)实验⑤未观察到明显现象,该小组同学反思后认为该反应不能发生,理由是________________ 。
(6)以上实验中能够证明FeSO4有氧化性的是______________ (填序号),该反应的离子方程式是______________ 。
解释和结论:
(7)以上实验可得出的结论是_____________________ 。
预测:从FeSO4的类别角度,预测其可能与某些金属、酸、碱、盐发生反应;聚焦FeSO4中的Fe元素作为核心元素,预测FeSO4既具有氧化性,又具有还原性。
(1)从FeSO4的元素组成看,它的物质类别是
(2)预测其具有还原性的思路是
实验和观察:该小组同学分别实施以下实验。
| 实验① | 实验② | 实验③ | 实验④ | 实验⑤ |
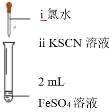 | 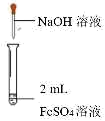 | 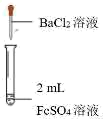 |  | 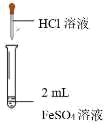 |
(4)实验②中的现象是
(5)实验⑤未观察到明显现象,该小组同学反思后认为该反应不能发生,理由是
(6)以上实验中能够证明FeSO4有氧化性的是
解释和结论:
(7)以上实验可得出的结论是
您最近一年使用:0次
6 . 已知:①向KMnO4晶体滴加浓盐酸,产生黄绿色气体;②向FeCl2溶液中通入少量实验①产生的气体,溶液变黄色;③取实验②生成的溶液滴在淀粉KI试纸上,试纸变蓝色。下列判断正确的是
A.上述实验证明氧化性:MnO >Cl2>Fe3+>I2 >Cl2>Fe3+>I2 |
| B.上述实验中,共有两个氧化还原反应 |
| C.实验①生成的气体不能使湿润的淀粉KI试纸变蓝 |
| D.实验②证明Fe2+既有氧化性又有还原性 |
您最近一年使用:0次
2021-06-22更新
|
1632次组卷
|
19卷引用:1.3 氧化还原反应-同步学习必备知识
(已下线)1.3 氧化还原反应-同步学习必备知识(已下线)2.2.1氯气的性质-同步学习必备知识四川省南充市阆中中学2020届高三化学选择题专项训练(12)吉林油田高级中学2019-2020学年高二下学期期末考试化学试题云南省罗平县第五中学2020-2021学年高一上学期12月月考化学试题陕西省西安市长安区第一中学2020-2021学年高一上学期第二次月考化学试题河南省新蔡县第一高级中学2020-2021学年高一上学期1月月考化学试题福建省福州市闽江口联盟校2021届高三上学期期中联考化学试题江西省赣州市信丰中学2020-2021学年高三上学期第二次月考化学试题福建省武平县第一中学2020-2021学年高一上学期第二次阶段考试(实验班)化学试题江西省九江市柴桑区第一中学2021-2022学年高三上学期第二次月考化学试题黑龙江省哈尔滨市德强高中2021-2022学年高一上学期期中考试化学试题新疆师范大学附属中学2021-2022学年高三9月月考化学试题云南省玉溪市通海县第一中学2021—2022学年高一上学期期末考试化学试题黑龙江省黑河市第九中学2022-2023学年高三上学期摸底考试化学试题 山东省济宁市兖州区2022-2023学年高一上学期期中考试化学试题福建省诏安县桥东中学2022-2023学年高三上学期期中考试化学试题云南省广南县第二中学校2021-2022学年高一下学期开学考试化学试题广东省云浮市罗定中学2023-2024学年高一上学期期中考试化学试题
名校
7 . 某小组同学欲探究H2O2的性质,经历如下探究过程:
预测:聚焦H2O2中的O作为核心元素,因此预测H2O2既具有氧化性,也具有还原性。
(1)预测其具有氧化性的思路是_________ 。
实验和观察:小组同学分别选用酸性KMnO4溶液、酸化的KI溶液与5% H2O2溶液反应以验证预测。
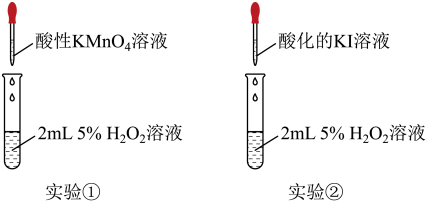
(2)实验①利用了酸性高锰酸钾的_________ 性质,该实验中,证明KMnO4溶液与H2O2反应的现象除了溶液颜色变浅或褪色外,还有________ 。
(3)实验②是为了验证H2O2的_________ 性质,在反应后的溶液中加入淀粉溶液,可观察到溶液变蓝,写出该反应的离子方程式____________ 。
解释和结论:
(4)以上实验可得出的结论是______________________ 。
预测:聚焦H2O2中的O作为核心元素,因此预测H2O2既具有氧化性,也具有还原性。
(1)预测其具有氧化性的思路是
实验和观察:小组同学分别选用酸性KMnO4溶液、酸化的KI溶液与5% H2O2溶液反应以验证预测。

(2)实验①利用了酸性高锰酸钾的
(3)实验②是为了验证H2O2的
解释和结论:
(4)以上实验可得出的结论是
您最近一年使用:0次
2020-01-10更新
|
613次组卷
|
8卷引用:专题3 本专题达标检测-高中化学苏教2019版必修第一册
名校
8 . 已知重铬酸钾(K2Cr2O7)溶液中存在如下平衡: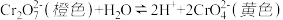
实验①:向2mL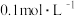 K2Cr2O7溶液中滴入3滴
K2Cr2O7溶液中滴入3滴 NaOH溶液,溶液由橙色变为黄色;向所得溶液中再滴入5滴浓
NaOH溶液,溶液由橙色变为黄色;向所得溶液中再滴入5滴浓 ,溶液由黄色变为橙色.
,溶液由黄色变为橙色.
实验②:向2mL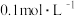 酸化的K2Cr2O7溶液中滴入适量
酸化的K2Cr2O7溶液中滴入适量 溶液,溶液由橙色变为绿色,发生反应:
溶液,溶液由橙色变为绿色,发生反应: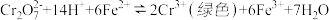 .
.
下列分析正确的是( )
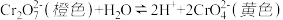
实验①:向2mL
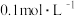 K2Cr2O7溶液中滴入3滴
K2Cr2O7溶液中滴入3滴 NaOH溶液,溶液由橙色变为黄色;向所得溶液中再滴入5滴浓
NaOH溶液,溶液由橙色变为黄色;向所得溶液中再滴入5滴浓 ,溶液由黄色变为橙色.
,溶液由黄色变为橙色.实验②:向2mL
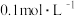 酸化的K2Cr2O7溶液中滴入适量
酸化的K2Cr2O7溶液中滴入适量 溶液,溶液由橙色变为绿色,发生反应:
溶液,溶液由橙色变为绿色,发生反应: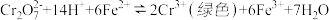 .
.下列分析正确的是( )
| A.实验①和②均能证明K2Cr2O7溶液中存在上述平衡 |
B.实验②能说明氧化性: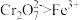 |
C. 和Fe2+在酸性溶液中可以大量共存 和Fe2+在酸性溶液中可以大量共存 |
| D.稀释 K2Cr2O7溶液时,溶液中各离子浓度均减小 |
您最近一年使用:0次
2019-08-19更新
|
884次组卷
|
15卷引用:2.2.2 影响化学平衡的因素(练习)-2020-2021学年上学期高二化学同步精品课堂(新教材人教版选择性必修1)
(已下线)2.2.2 影响化学平衡的因素(练习)-2020-2021学年上学期高二化学同步精品课堂(新教材人教版选择性必修1)2015届北京市海淀区高三一模理综化学试卷2015届浙江省宁波市高三4月模拟练习化学试卷2016届辽宁省大连二十四中高三上学期期中测试化学试卷2016-2017学年天津市六校高二上学期期中化学卷北京市西城区重点中学2018届高三上学期期末复习检验化学试题【全国百强校】河北省辛集中学2017-2018学年高二6月月考化学试题甘肃省兰州第一中学2018-2019学年高二(理)上学期期中考试化学试题百所名校联考-化学物质及其变化北京师范大学附中2019-2020学年高二上学期期中考试化学试题(已下线)小题必刷08 氧化还原反应的规律及应用——2021年高考化学一轮复习小题必刷(通用版)(已下线)练习4 化学平衡-2020-2021学年【补习教材·寒假作业】高二化学(人教版2019)(已下线)微专题07 氧化性和还原性强弱的实验探究及应用-备战2022年高考化学考点微专题重庆市育才中学2021-2022学年上学期高二上学期第六次定时练习化学试题辽宁省部分高中2021-2022学年高三上学期期中评测化学试题
9 . 能与Fe3+反应且能证明Fe3+具有氧化性的物质是( )
| A.氢氧化钠 | B.硫氰化钾 | C.氯化亚铁 | D.铁 |
您最近一年使用:0次
2019-09-16更新
|
314次组卷
|
7卷引用:3.1.1 铁及其化合物练习(2)——《高中新教材同步备课》(鲁科版 必修第一册)
(已下线)3.1.1 铁及其化合物练习(2)——《高中新教材同步备课》(鲁科版 必修第一册)云南省通海县三中2019-2020学年高二9月份(开学考试)化学试题云南省普洱市江城县第一中学2019—2020学年高一上学期期末考试化学试题湖南省长沙市浏阳市2019-2020学年高一上学期期末考试化学试题广西河池市都安第五高中2019-2020学年高一上学期期末考试化学试题云南省沧源县民中2019-2020学年高一12月月考化学试题(已下线)第12讲 铁、亚铁盐和铁盐-【暑假自学课】2022年新高一化学暑假精品课(鲁科版2019必修第一册)
10 . 过氧化钠和氢化钠(NaH),广泛应用于工业生产.
(1)氢化钠(NaH)中氢元素的化合价为_____________ .
(2)NaH能与水剧烈反应:NaH+H2O═NaOH+H2↑,该反应中的氧化剂是_________ ,氧化剂与还原剂的物质的量之比是_____________ .
(3)在高温下氢化钠(NaH)可将四氯化钛(TiC14)还原成金属钛,该反应的化学方程式为_____________________ .
(4)过氧化钠是呼吸面和防毒面具中氧气的来源,写出过氧化钠与二氧化碳反应的化学方程式______________ ,证明有氧气产生的方法是______________ .
(1)氢化钠(NaH)中氢元素的化合价为
(2)NaH能与水剧烈反应:NaH+H2O═NaOH+H2↑,该反应中的氧化剂是
(3)在高温下氢化钠(NaH)可将四氯化钛(TiC14)还原成金属钛,该反应的化学方程式为
(4)过氧化钠是呼吸面和防毒面具中氧气的来源,写出过氧化钠与二氧化碳反应的化学方程式
您最近一年使用:0次



