2024高三·全国·专题练习
解题方法
1 . 化学需氧量(COD)是指用强氧化剂将1 L废水中的还原性物质氧化为二氧化碳和水所消耗的氧化剂的量,并换算成以O2为氧化剂时所消耗O2的质量。水体COD值常作为水体中有机污染物相对含量的综合指标之一,Fenton(Fe2+/H2O2)法能产生Fe3+和具有强氧化性的羟基自由基(·OH)引发一系列链式反应,被广泛应用于有机废水的治理。
(1)羟基自由基(·OH)的电子式为___________ 。
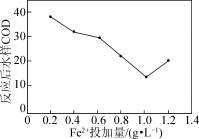
(2)分别取初始pH=4、COD=80的废水200 mL,加入200 mL H2O2,改变起始投加FeSO4·7H2O的量,反应相同时间。测得反应后水样COD随Fe2+投加量的关系如图所示。当Fe2+投加量超过1 g·L-1时,反应后水样COD不降反升的原因可能是___________ 。 )的氧化技术引起关注。研究发现,一种Mn3O4石墨烯纳米复合材料对催化活化S2O
)的氧化技术引起关注。研究发现,一种Mn3O4石墨烯纳米复合材料对催化活化S2O 产生SO
产生SO 具有很好的效果。S2O
具有很好的效果。S2O 结构如图所示。
结构如图所示。 的使用范围更广。SO
的使用范围更广。SO 在强碱性条件下反应生成·OH,写出该反应的离子方程式:
在强碱性条件下反应生成·OH,写出该反应的离子方程式:___________ 。
② 一种制取Mn3O4—石墨烯纳米复合材料的物种转化关系可表示如下(GO表示石墨烯):___________ mol。
③利用该复合材料催化活化S2O 并去除废水中有机污染物的可能反应机理如图所示。该机理可描述为
并去除废水中有机污染物的可能反应机理如图所示。该机理可描述为___________ 。
(1)羟基自由基(·OH)的电子式为
(2)分别取初始pH=4、COD=80的废水200 mL,加入200 mL H2O2,改变起始投加FeSO4·7H2O的量,反应相同时间。测得反应后水样COD随Fe2+投加量的关系如图所示。当Fe2+投加量超过1 g·L-1时,反应后水样COD不降反升的原因可能是
 )的氧化技术引起关注。研究发现,一种Mn3O4石墨烯纳米复合材料对催化活化S2O
)的氧化技术引起关注。研究发现,一种Mn3O4石墨烯纳米复合材料对催化活化S2O 产生SO
产生SO 具有很好的效果。S2O
具有很好的效果。S2O 结构如图所示。
结构如图所示。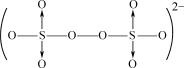
 的使用范围更广。SO
的使用范围更广。SO 在强碱性条件下反应生成·OH,写出该反应的离子方程式:
在强碱性条件下反应生成·OH,写出该反应的离子方程式:② 一种制取Mn3O4—石墨烯纳米复合材料的物种转化关系可表示如下(GO表示石墨烯):
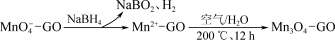
③利用该复合材料催化活化S2O
 并去除废水中有机污染物的可能反应机理如图所示。该机理可描述为
并去除废水中有机污染物的可能反应机理如图所示。该机理可描述为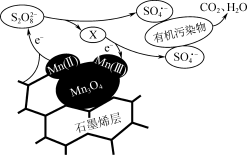
您最近一年使用:0次
2024高三下·全国·专题练习
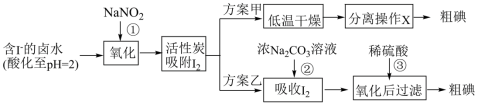
2 . 从海水中可以提取很多有用的物质,例如从海水制盐所得到的卤水中可以提取碘。活性炭吸附法是工业提碘的方法之一,其流程如下:
Ⅱ. ;
;
Ⅲ.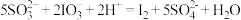 ;
;
方案甲中,根据I2的特性,分离操作X的名称是________ 。
Ⅱ.
 ;
;Ⅲ.
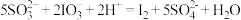 ;
;方案甲中,根据I2的特性,分离操作X的名称是
您最近一年使用:0次
2024高三·全国·专题练习
解题方法
3 . 下列离子方程式正确的是_______ 。
A.(2023·浙江卷)碘化亚铁溶液与等物质的量的氯气:
B.(2023·浙江卷)向次氯酸钙溶液通入足量二氧化碳: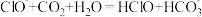
C.(2022·全国卷)将等物质的量浓度的Ba(OH)2和NH4HSO4溶液以体积比1∶2混合:Ba2++2OH-+2H++SO =BaSO4↓+2H2O
=BaSO4↓+2H2O
D.(2021·全国卷)硫酸铝溶液中滴加少量氢氧化钾溶液: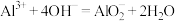
E.(2021·湖北卷)向次氯酸钙溶液中通入少量二氧化碳气体:ClO-+CO2+H2O=HClO+HCO
A.(2023·浙江卷)碘化亚铁溶液与等物质的量的氯气:

B.(2023·浙江卷)向次氯酸钙溶液通入足量二氧化碳:
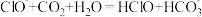
C.(2022·全国卷)将等物质的量浓度的Ba(OH)2和NH4HSO4溶液以体积比1∶2混合:Ba2++2OH-+2H++SO
 =BaSO4↓+2H2O
=BaSO4↓+2H2OD.(2021·全国卷)硫酸铝溶液中滴加少量氢氧化钾溶液:
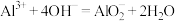
E.(2021·湖北卷)向次氯酸钙溶液中通入少量二氧化碳气体:ClO-+CO2+H2O=HClO+HCO

您最近一年使用:0次
23-24高三上·上海嘉定·阶段练习
名校
解题方法
4 . 工业上利用NaIO3和NaHSO3反应来制取单质I2
(1)配平下列化学方程式并标出电子转移方向和个数。___________ 。
_______NaIO3+_______NaHSO3—_______I2+_______Na2SO4+_______H2SO4+_______H2O
(2)在该反应中NaHSO3体现___________ (填“氧化性”或“还原性”),I2为___________ (填“氧化产物”或“还原产物”)。
(3)已知:HSO 、I2、I-、SO
、I2、I-、SO 和一些未知物组成的一个氧化还原反应,其中SO
和一些未知物组成的一个氧化还原反应,其中SO 是氧化产物,该反应中还原性HSO
是氧化产物,该反应中还原性HSO
___________ I-(填“>”或“<”),写出该反应的化学方程式___________ 。
(1)配平下列化学方程式并标出电子转移方向和个数。
_______NaIO3+_______NaHSO3—_______I2+_______Na2SO4+_______H2SO4+_______H2O
(2)在该反应中NaHSO3体现
(3)已知:HSO
 、I2、I-、SO
、I2、I-、SO 和一些未知物组成的一个氧化还原反应,其中SO
和一些未知物组成的一个氧化还原反应,其中SO 是氧化产物,该反应中还原性HSO
是氧化产物,该反应中还原性HSO
您最近一年使用:0次
2023高三上·全国·专题练习
解题方法
5 . 正确书写离子方程式:
(1)酸性溶液中,H2O2将Fe2+氧化为Fe3+的离子方程式为___________ ;
(2)铜与浓硝酸反应的离子方程式为___________ ;
(3)酸性KMnO4溶液与FeCl2反应的离子方程式为___________ ;
(4)在H2O2存在下Cu溶于稀H2SO4,反应的离子方程式为___________ ;
(5)Cl2与NaOH溶液反应生成NaClO3和NaCl,其离子方程式___________ ;
(6)在弱碱性溶液中,FeS与CrO 反应生成Fe(OH)3、Cr(OH)3和单质S,其离子方程式为
反应生成Fe(OH)3、Cr(OH)3和单质S,其离子方程式为___________ ;
(7)用酸性高锰酸钾溶液与辉铜矿(主要成分是Cu2S)冶炼铜,反应的离子方程式为________ ;
(8)硫酸酸化的Na2Cr2O7溶液可以将乙醇氧化成乙酸,本身被还原成Cr3+,该反应可用于检验司机是否酒驾,相应的离子方程式___________ ;
(9)雾霾中含有的污染物NO可以被含Ce4+的溶液吸收,生成NO 、NO
、NO 物质的量之比为1∶1,试写出该反应的离子方程式
物质的量之比为1∶1,试写出该反应的离子方程式___________ 。
(1)酸性溶液中,H2O2将Fe2+氧化为Fe3+的离子方程式为
(2)铜与浓硝酸反应的离子方程式为
(3)酸性KMnO4溶液与FeCl2反应的离子方程式为
(4)在H2O2存在下Cu溶于稀H2SO4,反应的离子方程式为
(5)Cl2与NaOH溶液反应生成NaClO3和NaCl,其离子方程式
(6)在弱碱性溶液中,FeS与CrO
 反应生成Fe(OH)3、Cr(OH)3和单质S,其离子方程式为
反应生成Fe(OH)3、Cr(OH)3和单质S,其离子方程式为(7)用酸性高锰酸钾溶液与辉铜矿(主要成分是Cu2S)冶炼铜,反应的离子方程式为
(8)硫酸酸化的Na2Cr2O7溶液可以将乙醇氧化成乙酸,本身被还原成Cr3+,该反应可用于检验司机是否酒驾,相应的离子方程式
(9)雾霾中含有的污染物NO可以被含Ce4+的溶液吸收,生成NO
 、NO
、NO 物质的量之比为1∶1,试写出该反应的离子方程式
物质的量之比为1∶1,试写出该反应的离子方程式
您最近一年使用:0次
2023高三·全国·专题练习
6 . 氧化还原反应在工业生产、环保及科研中有广泛的应用,请根据以上信息,结合自己所掌握的化学知识,回答下列问题:
Ⅰ.氢化亚铜(CuH)是一种难溶物质,用CuSO4溶液和“另一物质”在40~50℃时反应可生成CuH。CuH具有的性质:不稳定,易分解,在氯气中能燃烧;与稀盐酸反应能生成气体,Cu+在酸性条件下发生的反应是2Cu+=Cu2++Cu。
(1)写出CuH在氯气中燃烧的化学方程式:___________ 。
(2)CuH溶解在稀盐酸中生成的气体是___________ (填化学式)。
(3)将CuH溶解在足量的稀硝酸中生成的气体只有NO,请写出CuH溶解在足量稀硝酸中反应的离子方程式:___________ 。
Ⅱ.钒性能优良,用途广泛,有金属“维生素”之称。完成下列填空:
(4)将废钒催化剂(主要成分V2O5)与稀硫酸、亚硫酸钾溶液混合,充分反应后生成VO2+等离子,该反应的化学方程式是___________ 。
(5)V2O5能与盐酸反应产生VO2+和一种黄绿色气体,该气体能与Na2SO3溶液反应而被吸收,则 、Cl-、VO2+还原性由强到弱的顺序是
、Cl-、VO2+还原性由强到弱的顺序是___________ 。
Ⅰ.氢化亚铜(CuH)是一种难溶物质,用CuSO4溶液和“另一物质”在40~50℃时反应可生成CuH。CuH具有的性质:不稳定,易分解,在氯气中能燃烧;与稀盐酸反应能生成气体,Cu+在酸性条件下发生的反应是2Cu+=Cu2++Cu。
(1)写出CuH在氯气中燃烧的化学方程式:
(2)CuH溶解在稀盐酸中生成的气体是
(3)将CuH溶解在足量的稀硝酸中生成的气体只有NO,请写出CuH溶解在足量稀硝酸中反应的离子方程式:
Ⅱ.钒性能优良,用途广泛,有金属“维生素”之称。完成下列填空:
(4)将废钒催化剂(主要成分V2O5)与稀硫酸、亚硫酸钾溶液混合,充分反应后生成VO2+等离子,该反应的化学方程式是
(5)V2O5能与盐酸反应产生VO2+和一种黄绿色气体,该气体能与Na2SO3溶液反应而被吸收,则
 、Cl-、VO2+还原性由强到弱的顺序是
、Cl-、VO2+还原性由强到弱的顺序是
您最近一年使用:0次
7 . 价态规律
(1)高低规律
元素最高价态:只有___________ 。
元素中间价态:既有___________ 。
元素最低价态:只有___________ 。
(2)归中规律
①同种元素不同价态之间发生氧化还原反应时,高价态+低价态→中间价态,遵循___________ 的规律。
②同种元素___________ 间不发生化学反应。
(3)歧化规律
同种元素的中间价态生成___________ ,即中间价态→高价态+低价态。
(1)高低规律
元素最高价态:只有
元素中间价态:既有
元素最低价态:只有
(2)归中规律
①同种元素不同价态之间发生氧化还原反应时,高价态+低价态→中间价态,遵循
②同种元素
(3)歧化规律
同种元素的中间价态生成
您最近一年使用:0次
2023高三·全国·专题练习
8 . 一般用K2Cr2O7滴定分析法测定还原铁粉纯度。实验步骤:称取一定量样品,用过量稀硫酸溶解,用标准K2Cr2O7溶液滴定其中的Fe2+。反应式:  +6Fe2++14H+=2Cr3++6Fe3++7H2O某次实验称取0.2800g样品,滴定时消耗浓度为0.03000mol·L-1的K2Cr2O7溶液25.10mL,则样品中铁含量为
+6Fe2++14H+=2Cr3++6Fe3++7H2O某次实验称取0.2800g样品,滴定时消耗浓度为0.03000mol·L-1的K2Cr2O7溶液25.10mL,则样品中铁含量为_______ %。
 +6Fe2++14H+=2Cr3++6Fe3++7H2O某次实验称取0.2800g样品,滴定时消耗浓度为0.03000mol·L-1的K2Cr2O7溶液25.10mL,则样品中铁含量为
+6Fe2++14H+=2Cr3++6Fe3++7H2O某次实验称取0.2800g样品,滴定时消耗浓度为0.03000mol·L-1的K2Cr2O7溶液25.10mL,则样品中铁含量为
您最近一年使用:0次
2023高三·全国·专题练习
解题方法
9 . 完成下列问题。
(1)Ba(OH)2溶液与NaHSO4溶液的反应:
①当反应后的溶液呈碱性时,反应的离子方程式为___________ 。
②当n[Ba(OH)2]∶n(NaHSO4)=1∶2时反应的离子方程式为___________ 。
(2)在富氧条件下,通过硝酸盐菌的作用,将氨氮(以 表示)氧化成硝酸盐的离子方程式为
表示)氧化成硝酸盐的离子方程式为________________ 。
(3)将过碳酸钠(2Na2CO3·3H2O2)溶于水配成溶液,加入适量稀硫酸,再加入足量KI,充分反应后加入少量淀粉试剂,溶液呈蓝色,该反应的离子方程式为___________ 。
(1)Ba(OH)2溶液与NaHSO4溶液的反应:
①当反应后的溶液呈碱性时,反应的离子方程式为
②当n[Ba(OH)2]∶n(NaHSO4)=1∶2时反应的离子方程式为
(2)在富氧条件下,通过硝酸盐菌的作用,将氨氮(以
 表示)氧化成硝酸盐的离子方程式为
表示)氧化成硝酸盐的离子方程式为(3)将过碳酸钠(2Na2CO3·3H2O2)溶于水配成溶液,加入适量稀硫酸,再加入足量KI,充分反应后加入少量淀粉试剂,溶液呈蓝色,该反应的离子方程式为
您最近一年使用:0次
10 . 守恒规律
(1)还原剂___________ ,化合价___________ 总数=氧化剂___________ ,化合价___________ 总数。
(2)___________ 。
(3)n(氧化剂)×变价原子个数×化合价变化值=n(还原剂)×变价原子个数×化合价变化值
(1)还原剂
(2)
(3)n(氧化剂)×变价原子个数×化合价变化值=n(还原剂)×变价原子个数×化合价变化值
您最近一年使用:0次



