名校
解题方法
1 . 已知A为淡黄色固体,R是地壳中含量最多的金属元素的单质,T 为生活中使用最广泛的金属单质,D是具有磁性的黑色晶体,C、F是无色无味的气体,M为红褐色。
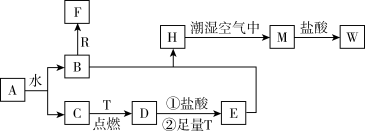
请回答下列问题:
(1)A的电子式是___________ ,R元素在元素周期表中位置为___________ ,D的俗称是___________ 。
(2)A与水反应的离子方程式为___________ 。
(3)检验W 溶液中金属阳离子的操作方法是___________ 。
(4)H转化为M的化学方程式为___________ 。
(5)B生成F反应的离子方程式为___________ 。
(6)向一定量T和D的混合物中加入200mL 1mol/L的盐酸,固体恰好完全溶解,且产生氢气448mL(标准状况下),所得溶液只有一种溶质,则混合物中两种物质的物质的量之比为___________ 。

请回答下列问题:
(1)A的电子式是
(2)A与水反应的离子方程式为
(3)检验W 溶液中金属阳离子的操作方法是
(4)H转化为M的化学方程式为
(5)B生成F反应的离子方程式为
(6)向一定量T和D的混合物中加入200mL 1mol/L的盐酸,固体恰好完全溶解,且产生氢气448mL(标准状况下),所得溶液只有一种溶质,则混合物中两种物质的物质的量之比为
您最近一年使用:0次
名校
解题方法
2 . 已知图是由常见元素组成的一些单质及其化合物之间的转化关系图。A是由单质C在D中燃烧生成的淡黄色固体。B是最常见的无色液体,常温常压下,D、F、K均为无色无刺激性气味的气体。H和I焰色反应均为黄色。(反应中生成的部分物质已略去)请回答下列问题:
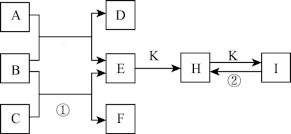
(1)物质A的化学式为____________________ 。
(2)反应①的离子方程式为_________________________________________ 。
(3)反应②的化学方程式为__________________________________________ 。
(4)加热10g H和I的混合物质至质量不再变化,剩余固体质量8.45g,原混合物中H的质量分数为________________ 。

(1)物质A的化学式为
(2)反应①的离子方程式为
(3)反应②的化学方程式为
(4)加热10g H和I的混合物质至质量不再变化,剩余固体质量8.45g,原混合物中H的质量分数为
您最近一年使用:0次
3 . 已知A、B均是由两种元素组成的化合物,A中某种元素的质量分数为75%,B是一种淡黄色固体,C、J是同周期元素的气态氢化物,其中C是含氢量最高的烃,X为常见的无色液体。反应生成的水均已略去。它们有如下图所示的关系。
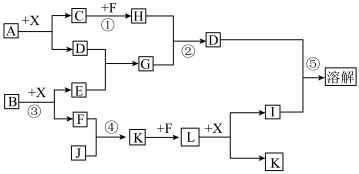
(1)写出化学式:A________ ,B________ ,J________ ;
(2)反应③中每生成1 mol F,转移电子的数目为______________ ;
(3)反应④的化学方程式为:______________________________ ;
(4)写出离子方程式:反应②________________________________ ,反应⑤________________________________________________ 。

(1)写出化学式:A
(2)反应③中每生成1 mol F,转移电子的数目为
(3)反应④的化学方程式为:
(4)写出离子方程式:反应②
您最近一年使用:0次
解题方法
4 . 兰尼镍是一种带有多孔结构的细小晶粒组成的镍铝合金,被广泛用作有机物的氢化反应的催化剂。以红土镍矿(主要成分为NiS、FeS和SiO2等)为原料制备兰尼镍的工艺流程如下图所示:
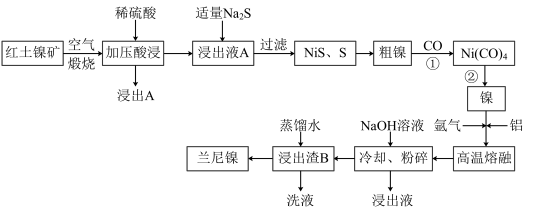
(1)煅烧时主要生成的气体产物是___________ ,浸出渣A的主要成分是____________ 。
(2)向浸出液A中加入适量Na2S,发生氧化还原的离子方程式为________________________ 。若Na2S过量时,则过滤出的固体中会混有__________ ;
(3)已知Ni(CO)4的沸点是42.2℃,Ni(S)+CO(g)⇌ Ni(CO)4(g)的平衡常数与温度的关系如下:
步骤①、步骤②的最佳温度分别是_______ 、_______ (填选项代号)
A. 25℃ B. 30℃ C. 50℃ D. 80℃ E. 230℃
(4)加氢氧化钠的目的是溶解部分铝,形成多孔结构的镍铝合金,已知红土镍矿中NiS质量分数45.5%,取1kg红土镍矿进行制备(不考虑制备过程中镍的损耗),熔融时加入270g铝,浸出时消耗800mL 5mol/LNaOH,理论上生成的兰尼镍的化学式为__________ 。

(1)煅烧时主要生成的气体产物是
(2)向浸出液A中加入适量Na2S,发生氧化还原的离子方程式为
(3)已知Ni(CO)4的沸点是42.2℃,Ni(S)+CO(g)⇌ Ni(CO)4(g)的平衡常数与温度的关系如下:
| 温度/℃ | 25 | 80 | 230 |
| 平衡常数 | 5×104 | 2 | 1.9×10-5 |
A. 25℃ B. 30℃ C. 50℃ D. 80℃ E. 230℃
(4)加氢氧化钠的目的是溶解部分铝,形成多孔结构的镍铝合金,已知红土镍矿中NiS质量分数45.5%,取1kg红土镍矿进行制备(不考虑制备过程中镍的损耗),熔融时加入270g铝,浸出时消耗800mL 5mol/LNaOH,理论上生成的兰尼镍的化学式为
您最近一年使用:0次
解题方法
5 . 已知A、B均是由一种金属元素和一种非金属元素组成的化合物,A中金属元素的质量分数为75%,B是一种淡黄色固体,C、J是同周期元素的气态氢化物,其中C是含氢量最高的烃,X为常见的无色液体。反应生成的水均已略去。它们有如图所示的关系。
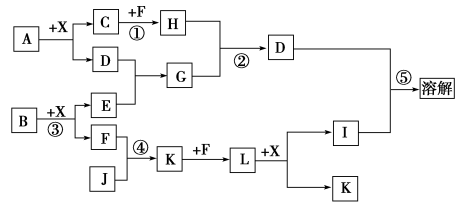
(1)写出B的化学式:___ ;
(2)反应③中每生成1molF,转移电子的数目为___ ;
(3)反应④的化学方程式为:___ ;
(4)写出少量H与G发生反应②的离子方程式:___ 。

(1)写出B的化学式:
(2)反应③中每生成1molF,转移电子的数目为
(3)反应④的化学方程式为:
(4)写出少量H与G发生反应②的离子方程式:
您最近一年使用:0次
解题方法
6 . (1)部分中学化学常见元素的原子结构及性质如下表所示。
①这五种元素的原子半径最大是______ (用元素符号表示)。
②E与D可以按原子个数比2:1、1:1形成两种化合物X、Y, E与C组成的两种化合物M、N,所含电子数分别与X、Y相等,M中共用电子对对数为______ ,N的结构式为______ 。
(2)已知:某无色废水中可能含有H+、NH 、Fe3+、Al3+、Mg2+、Na+、NO
、Fe3+、Al3+、Mg2+、Na+、NO 、CO
、CO 、SO
、SO 中的几种,为分析其成分,分别取废水样品1 L,进行了三组实验,其操作和有关图象如下所示:
中的几种,为分析其成分,分别取废水样品1 L,进行了三组实验,其操作和有关图象如下所示:
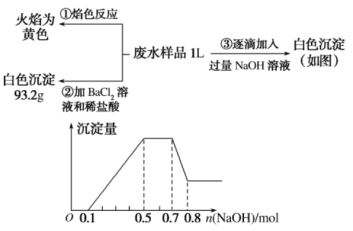
请回答下列问题:
①根据上述3组实验可以分析废水中一定不存在的阴离子是______ 。
②写出实验③图象中沉淀达到最大量且质量不再发生变化阶段发生反应的离子方程式______ 。
③分析图象,所得沉淀的最大质量是______ g。
④若通过实验确定原废水中c(Na+)=0.18 mol·L-1,试判断原废水中NO 是否存在
是否存在______ ,若存在,c(NO )=
)=______ mol·L-1 (若不存在或不确定则此空不填)。
| 元素 | 结构及性质 |
| A | A为地壳中含量仅次于氧的非金属元素,其单质晶体结构与金刚石相似 |
| B | B原子最外层电子数是内层电子总数的1/5 |
| C | C是常用化肥的主要元素,单质常温下呈气态 |
| D | 通常情况下,D在化合物中显负价,A、B、C都能与D形成中学常见化合物 |
| E | E元素的一种同位素原子无中子 |
②E与D可以按原子个数比2:1、1:1形成两种化合物X、Y, E与C组成的两种化合物M、N,所含电子数分别与X、Y相等,M中共用电子对对数为
(2)已知:某无色废水中可能含有H+、NH
 、Fe3+、Al3+、Mg2+、Na+、NO
、Fe3+、Al3+、Mg2+、Na+、NO 、CO
、CO 、SO
、SO 中的几种,为分析其成分,分别取废水样品1 L,进行了三组实验,其操作和有关图象如下所示:
中的几种,为分析其成分,分别取废水样品1 L,进行了三组实验,其操作和有关图象如下所示:
请回答下列问题:
①根据上述3组实验可以分析废水中一定不存在的阴离子是
②写出实验③图象中沉淀达到最大量且质量不再发生变化阶段发生反应的离子方程式
③分析图象,所得沉淀的最大质量是
④若通过实验确定原废水中c(Na+)=0.18 mol·L-1,试判断原废水中NO
 是否存在
是否存在 )=
)=
您最近一年使用:0次
名校
7 . Ⅰ.X、Y、Z为短周期元素的单质,U、V为它们的化合物,这些物质之间的关系如图所示,其中反应条件和某些产物已经略去:

(1)如果X、Y的组成元素是同主族的
①若已知V是水,写出反应Ⅰ的化学反应方程式:_______ ;
②若已知U、V均为氧化物,写出Y的组成元素的原子结构示意图_______ 。
(2)如果X、Y的组成元素不同主族时
①X组成元素是地壳中含量最多的金属元素时,则Z的化学式为_______ 。
②若Y在自然界中形成的化合物的种类最多时,U是一种气态氧化物,则V的电子式是:_______ 。
Ⅱ.X、Y、Z和W代表原子序数依次增大的四种短周期元素,它们满足以下条件:①元素周期表中,Z与Y相邻,Z与W也相邻;②Y、Z和W三种元素的原子最外层电子数之和为17。X、Y、Z和W可组成一化合物,其原子个数之比为8:2:4:1。写出该化合物的化学式_______ ,所含化学键_______ 。

(1)如果X、Y的组成元素是同主族的
①若已知V是水,写出反应Ⅰ的化学反应方程式:
②若已知U、V均为氧化物,写出Y的组成元素的原子结构示意图
(2)如果X、Y的组成元素不同主族时
①X组成元素是地壳中含量最多的金属元素时,则Z的化学式为
②若Y在自然界中形成的化合物的种类最多时,U是一种气态氧化物,则V的电子式是:
Ⅱ.X、Y、Z和W代表原子序数依次增大的四种短周期元素,它们满足以下条件:①元素周期表中,Z与Y相邻,Z与W也相邻;②Y、Z和W三种元素的原子最外层电子数之和为17。X、Y、Z和W可组成一化合物,其原子个数之比为8:2:4:1。写出该化合物的化学式
您最近一年使用:0次
18-19高一下·江西南昌·阶段练习
解题方法
8 . A、B、C均为短周期元素组成的物质,其转化关系如图所示:

请回答:
(1)若A为淡黄色固体,C是单质。
① 组成C的元素在周期表中的位置是________________ 。
② 取少量A与水反应,下列叙述正确的是___________ (填字母)。
a.该反应是氧化还原反应
b.向B的溶液中滴加酚酞,溶液变红
c.当有1 mol A参加反应时,共转移2 mol 电子
(2)若A由两种元素组成,其中一种元素的最外层电子数比电子层数多3,另一种是地壳中含量最多的元素。B与A的组成元素相同。
① A与水反应的化学方程式为_________________________ 。
②A与O2混合通入到水中,恰好生成4molC,则通入的A为________ mol,O2为__________ mol

请回答:
(1)若A为淡黄色固体,C是单质。
① 组成C的元素在周期表中的位置是
② 取少量A与水反应,下列叙述正确的是
a.该反应是氧化还原反应
b.向B的溶液中滴加酚酞,溶液变红
c.当有1 mol A参加反应时,共转移2 mol 电子
(2)若A由两种元素组成,其中一种元素的最外层电子数比电子层数多3,另一种是地壳中含量最多的元素。B与A的组成元素相同。
① A与水反应的化学方程式为
②A与O2混合通入到水中,恰好生成4molC,则通入的A为
您最近一年使用:0次
9 . 已知A为淡黄色固体,R是地壳中含量最多的金属元素的单质,T为生活中使用最广泛的金属单质,D 是具有磁性的黑色晶体,C、F是无色无味的气体,H是白色沉淀,W溶液中滴加KSCN溶液出现红色。
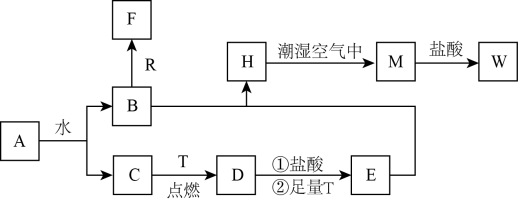
(1)物质D的化学式为_______ ,E化学式为_______ 。
(2)点燃气体F前必须先_______ 。
(3)H在潮湿空气中变成M的实验现象是_______ ,化学方程式为_______ 。
(4)B和R在溶液中反应生成F的离子方程式为_______ 。

(1)物质D的化学式为
(2)点燃气体F前必须先
(3)H在潮湿空气中变成M的实验现象是
(4)B和R在溶液中反应生成F的离子方程式为
您最近一年使用:0次
名校
10 . A、B、C、X为中学化学常见物质,A、B、C含有相同元素甲,可以发生如下转化(水参与的反应,水未标出)。
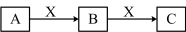
下列说法不正确 的是

下列说法
| A.若A、B、C的焰色反应呈黄色、水溶液均呈碱性,则X可以是CO2 |
| B.若C为红棕色气体,则A一定为空气中含量最高的气体 |
| C.若B为FeCl3,则X一定是Fe |
| D.A可以是碳单质,也可以是O2 |
您最近一年使用:0次
2019-11-13更新
|
765次组卷
|
13卷引用:江西省赣州市2020届高三上学期期末考试化学试题
江西省赣州市2020届高三上学期期末考试化学试题江西省赣州市赣县第三中学2022-2023学年高一上学期10月月考化学试题2020届高三化学海淀区高三第一学期期中练习北京市海淀区2019-2020学年高三期中考试化学试题重庆南开中学高2020届高三11月月考理综化学试题内蒙古呼和浩特市2020届高三第一次质量普查调研考试化学试题重庆市南开中学2020届高三年级网课学习能力自测理科综合化学试题北京市清华附中2019-2020学年高一下学期居家自主学习在线检测化学试题山东省济宁市泗水县2021届高三上学期期中考试化学试题天津市南开区2021届高三上学期期中质量调查化学试题河南省顶级名校2021届高三年级上学期期中考试化学试题黑龙江省鹤岗市第一中学2020-2021学年高二6月月考化学试题天津市汇文中学2022-2023学年高一上学期第二次阶段性测试化学试题



