名校
解题方法
1 . 已知A为淡黄色固体,R是地壳中含量最多的金属元素的单质,T为生活中 使用最广泛的金属单质,D是具有磁性的黑色晶体,C、F是无色无味的气体,H是白色沉淀。

(1)物质A的化学式为________ ,F化学式为 ________ ;
(2)B和R在溶液中反应生成F的离子方程式为__________________________ ;
(3)H在潮湿空气中变成M的实验现象是________ ,化学方程式为______________ ;
(4)A和水反应生成B和C的化学方程式为__________________________
(5)印刷行业刻制印刷电路板(含有铜箔)时,要用W溶液中作为“腐蚀液”,写出该反应的离子方程式______________________ 。

(1)物质A的化学式为
(2)B和R在溶液中反应生成F的离子方程式为
(3)H在潮湿空气中变成M的实验现象是
(4)A和水反应生成B和C的化学方程式为
(5)印刷行业刻制印刷电路板(含有铜箔)时,要用W溶液中作为“腐蚀液”,写出该反应的离子方程式
您最近一年使用:0次
2019-02-19更新
|
357次组卷
|
4卷引用:江西省南昌市进贤一中2019-2020学年高一上学期期末考试化学试题
名校
解题方法
2 . X、Y、Z均为短周期元素组成的物质,其转化关系如下:
请回答:

(1)若X为淡黄色固体,Z是单质。
①组成Z的元素在周期表中的位置是_________ 。
②取少量X与水反应,下列叙述正确的是_____ (填字母)。
a.该反应是氧化还原反应
b.向反应后的溶液中滴加酚酞试剂,溶液变红
c.当有1 molX参加反应时,共转移2mol电子
(2)若X由两种元素组成,其中一种元素的最外层电子数比电子层数多3,另一种是地壳中含量最多的元素。Y与X的组成元素相同。
①X与水反应的化学方程式为______________ 。
②X与O2混合通入水中,恰好生成4molZ,则通入的X为____ mol,O2为____ mol。
请回答:

(1)若X为淡黄色固体,Z是单质。
①组成Z的元素在周期表中的位置是
②取少量X与水反应,下列叙述正确的是
a.该反应是氧化还原反应
b.向反应后的溶液中滴加酚酞试剂,溶液变红
c.当有1 molX参加反应时,共转移2mol电子
(2)若X由两种元素组成,其中一种元素的最外层电子数比电子层数多3,另一种是地壳中含量最多的元素。Y与X的组成元素相同。
①X与水反应的化学方程式为
②X与O2混合通入水中,恰好生成4molZ,则通入的X为
您最近一年使用:0次
2019-03-29更新
|
285次组卷
|
3卷引用:江西省南昌市八一中学、洪都中学、十七中、实验中学四校2018-2019学年高一下学期3月联考化学试题
解题方法
3 . 各物质之间的转化关系如下图,部分生成物省略。C、D是由X、Y、Z中两种元素组成的化合物,X、Y、Z的原子序数依次增大,在周期表中X的原子半径最小,Y、Z原子最外层电子数之和为10。D为无色非可燃性气体,G为黄绿色单质气体,J、M为金属,I有漂白作用,反应①常用于制作印刷线路板。请回答下列问题:

(1)G元素在周期表中的位置______________ 。
(2)写出实验室制备G的离子反应方程式___________________ 。
(3)气体D与NaOH溶液反应可生成两种盐P和Q,在P中Na的质量分数为43%,其俗名为____________ 。
(4)实验室中检验L溶液中的阳离子常选用___________ 溶液,现象是_____________ 。
(5)A中包含X、Y、Z元素,A的化学式为____________ 。

(1)G元素在周期表中的位置
(2)写出实验室制备G的离子反应方程式
(3)气体D与NaOH溶液反应可生成两种盐P和Q,在P中Na的质量分数为43%,其俗名为
(4)实验室中检验L溶液中的阳离子常选用
(5)A中包含X、Y、Z元素,A的化学式为
您最近一年使用:0次
4 . 如图中,A、B、C、D、E是常见单质,其中B、C、E为金属。G、H、I、F是B、C、D、E分别和A形成的化合物,G物质有磁性。已知:①C与G反应生成B和H且放出大量的热,该反应可用于焊接铁轨;②I是一种常见的温室气体,它和E可以发生反应: ,F中E元素的质量分数为60%。回答问题:
,F中E元素的质量分数为60%。回答问题:
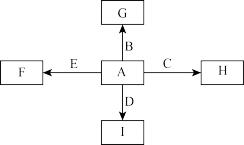
(1)C与G反应的化学方程式为____________________________ ;
(2)单质A的分子式为_____________ ,化合物I的名称为_______________ ;
(3)C与NaOH溶液反应的化学方程式为___________________________________ ;
(4)过量I与NaOH溶液反应的离子方程式为______________________________ ;
 ,F中E元素的质量分数为60%。回答问题:
,F中E元素的质量分数为60%。回答问题:
(1)C与G反应的化学方程式为
(2)单质A的分子式为
(3)C与NaOH溶液反应的化学方程式为
(4)过量I与NaOH溶液反应的离子方程式为
您最近一年使用:0次
2010·江西·二模
解题方法
5 . 物质A有如下图所示转化关系,其中乙为金属单质,常温下,它在G 的浓溶液中发生钝化, F 的溶液中只含有一种溶质(有的反应可能在水溶液中进行,有的反应的生成物未全部给出,反应条件也未注明)。请讨论以下两种情况(注:两种情况下各字母代表的物质可能不同)

(1)第一种情况:A为气体;用两根玻璃棒分别蘸取 A、G的浓溶液并使它们接近时,有大量白烟生成;甲为焰色反应呈黄色的金属单质; D 和 F 的溶液均呈碱性。则:
① B与甲反应的化学方程式为________________________________________ 。
② D与乙反应的离子方程式为_______________________________________ 。
(2)第二种情况:A为黄色固体;甲可由两种单质直接化合得到; D 的水溶液加入用硝酸酸化的AgNO3溶液有白色沉淀生成。则:
① 工业上,反应 I 在___________________ (填设备名称)中进行。
② 甲的化学式为______________ 。
③ D和乙反应的离子方程式为________________________________________ 。
④ 请简述检验G溶液中阴离子的方法____________________________________
⑤ 若A的相对分子质量为M,反应Ⅰ、Ⅱ、Ⅲ均为完全转化。现取m克含A及少量杂质的样品,按上述过程充分反应后(杂质不参与反应),得到密度为ρg/cm3,溶质质量分数为a% 的G溶液n mL。则该样品中A的质量分数=_______ (列出计算式即可)。

(1)第一种情况:A为气体;用两根玻璃棒分别蘸取 A、G的浓溶液并使它们接近时,有大量白烟生成;甲为焰色反应呈黄色的金属单质; D 和 F 的溶液均呈碱性。则:
① B与甲反应的化学方程式为
② D与乙反应的离子方程式为
(2)第二种情况:A为黄色固体;甲可由两种单质直接化合得到; D 的水溶液加入用硝酸酸化的AgNO3溶液有白色沉淀生成。则:
① 工业上,反应 I 在
② 甲的化学式为
③ D和乙反应的离子方程式为
④ 请简述检验G溶液中阴离子的方法
⑤ 若A的相对分子质量为M,反应Ⅰ、Ⅱ、Ⅲ均为完全转化。现取m克含A及少量杂质的样品,按上述过程充分反应后(杂质不参与反应),得到密度为ρg/cm3,溶质质量分数为a% 的G溶液n mL。则该样品中A的质量分数=
您最近一年使用:0次
6 . 如图中,A、B、C、D、E是单质,G、H、I、F是B、C、D、E分别和A形成的二元化合物.已知:①反应C+G B+H能放出大量的热,该反应曾应用于铁轨的焊接;②I是一种常见的温室气体,它和E可以发生反应:2E+I
B+H能放出大量的热,该反应曾应用于铁轨的焊接;②I是一种常见的温室气体,它和E可以发生反应:2E+I 2F+D,F中的E元素的质量分数为60%.回答问题:
2F+D,F中的E元素的质量分数为60%.回答问题:
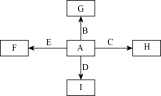
(1)① 中反应的化学方程式为________________________ ;
(2)化合物Ⅰ的电子式为____________ ,它的空间构型是______________ ;
(3)1.6g G 溶于盐酸,得到的溶液与铜粉完全反应,计算至少所需铜粉的质量_____________ (写出离子方程式和计算过程);
(4)C与过量NaOH溶液反应的离子方程式为___________________ ,反应后溶液与过量化合物Ⅰ反应的离子方程式为__________________ ;
(5)E在I中燃烧观察到的现象是_____________________ 。
 B+H能放出大量的热,该反应曾应用于铁轨的焊接;②I是一种常见的温室气体,它和E可以发生反应:2E+I
B+H能放出大量的热,该反应曾应用于铁轨的焊接;②I是一种常见的温室气体,它和E可以发生反应:2E+I 2F+D,F中的E元素的质量分数为60%.回答问题:
2F+D,F中的E元素的质量分数为60%.回答问题:
(1)① 中反应的化学方程式为
(2)化合物Ⅰ的电子式为
(3)1.6g G 溶于盐酸,得到的溶液与铜粉完全反应,计算至少所需铜粉的质量
(4)C与过量NaOH溶液反应的离子方程式为
(5)E在I中燃烧观察到的现象是
您最近一年使用:0次
2016-12-09更新
|
271次组卷
|
2卷引用:2016届江西省宜春市铜鼓中学高三四模化学试卷
7 . 已知M为氮元素与一种金属元素组成的离子化合物,其中金属元素的质量分数为35.4%,M在汽车安全气囊中有重要的作用。常温下G为淡黄色固体。H为一种常见的液体,A、B、C、X为单质,其中A、C、X为气体,A、X均为空气中成分。I、J为常见的工业原料。

①写出D与X反应的化学方程式___________________
②写出G与H反应的离子方程式___________________
③实验室中I应如何保存?_________________________
④常温下M受撞击时可分解,13gM完全分解为A和B时,放出akJ的热量,写出M分解的热化学方程式。______________________________
⑤M是一种易溶于水的盐,其水溶液显弱碱性,用离子方程式解释原因。__________

①写出D与X反应的化学方程式
②写出G与H反应的离子方程式
③实验室中I应如何保存?
④常温下M受撞击时可分解,13gM完全分解为A和B时,放出akJ的热量,写出M分解的热化学方程式。
⑤M是一种易溶于水的盐,其水溶液显弱碱性,用离子方程式解释原因。
您最近一年使用:0次
2011·江西赣州·一模
解题方法
8 . 已知:E为常见金属单质,C、D、F、I均为常见气体,其中C、D为单质,F、I为化合物,且组成元素相同,D、F有毒,I为直线型非极性分子,它们有如下框图关系:

(1)反应①阳极的电极反应式______ 。
(2)反应③的化学方程式______ ,
(3)反应④的离子方程式为______ 。
(4)K是一种难溶于水的固体,K受热分解可生成H。实现由G溶液到K的转化时可以加入的试剂是(填写选项字母)______
A.NaOH溶液 B.氨水 C.Na2CO3溶液 D.NaHCO3溶液
(5)将G的饱和溶液加入到沸水中,继续加热可得红褐色液体,写出反应的离子方程式:______
该液体接通直流电后______ 极附近颜色加深,这种过程叫做______ 。
(6)若E中含有合金元素,会导致G不纯。测定G的质量分数通常可用碘量法测定:称取mg无水G样品,溶于稀盐酸,再转移到100mL容量瓶,用蒸馏水定容;取出10.00mL,加入稍过量的KI溶液,充分反应后,用淀粉作指示剂并用cmol·L-1Na2S2O3溶液滴定(I2+2S2O =2I- +S4O
=2I- +S4O ),共用去VmL。(杂质不参与反应)则样品中G的质量分数为:
),共用去VmL。(杂质不参与反应)则样品中G的质量分数为:______ 。

(1)反应①阳极的电极反应式
(2)反应③的化学方程式
(3)反应④的离子方程式为
(4)K是一种难溶于水的固体,K受热分解可生成H。实现由G溶液到K的转化时可以加入的试剂是(填写选项字母)
A.NaOH溶液 B.氨水 C.Na2CO3溶液 D.NaHCO3溶液
(5)将G的饱和溶液加入到沸水中,继续加热可得红褐色液体,写出反应的离子方程式:
该液体接通直流电后
(6)若E中含有合金元素,会导致G不纯。测定G的质量分数通常可用碘量法测定:称取mg无水G样品,溶于稀盐酸,再转移到100mL容量瓶,用蒸馏水定容;取出10.00mL,加入稍过量的KI溶液,充分反应后,用淀粉作指示剂并用cmol·L-1Na2S2O3溶液滴定(I2+2S2O
 =2I- +S4O
=2I- +S4O ),共用去VmL。(杂质不参与反应)则样品中G的质量分数为:
),共用去VmL。(杂质不参与反应)则样品中G的质量分数为:
您最近一年使用:0次
解题方法
9 . A、B、C、D、E五种化合物中均含有地壳中含量最多的金属元素,它们的转化关系如图所示,其中A为澄清溶液,B、C为难溶的白色固体,E则易溶于水,若取A溶液灼烧,焰色反应为浅紫色(透过蓝色钴玻璃)。
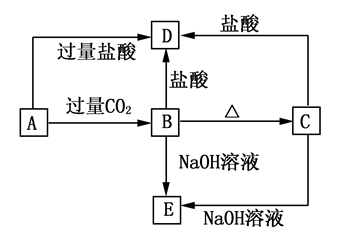
(1)写出化学式:A________ ,B________ ,C________ ,D________ ,E________ 。
(2)写出下列反应的离子方程式:
A→B:_____________________
A→D:_____________________

(1)写出化学式:A
(2)写出下列反应的离子方程式:
A→B:
A→D:
您最近一年使用:0次
2017-02-17更新
|
449次组卷
|
3卷引用:2016-2017学年江西省景德镇一中高一12月月考化学卷
10-11高三下·江西赣州·期中
解题方法
10 . W、X、Y、Z是原子序数依次增大的四种短周期元素,已知:W最外层电子数与电子层数相同,Y与X相邻,Y与Z也相邻;元素Z在地壳中含量最高。试回答下列各题:
(1)写出由其中两种元素组成的盐的电子式________________ 。
(2)比较Y、Z离子半径大小_____________________ ( 用化学式表示)
(3)已知W、Y、Z三种元素两两组合,可组成多种10电子微粒,请写出反应物生成物均为10电子微粒的离子方程式_______________________________________ 。
(4)由W、X、Z三种元素可组成A、B、C三种常见的有机化合物,其中A是日常生活中常用调味品的主要成分,且A与B能够反应生成C,C是一种有香味的液体。试写出该反应的化学方程式____________________________________________ 。
(5)由W、X、Y、Z四种元素中的三种元素组成的某种化合物,其浓溶液可与其中第四种元素的单质发生反应,写出该反应的化学方程式_________________________ 。
(6)已知由元素X和Z可组成A、B、C、D四种中学化学中常见的单质或化合物,四种物质之间存在如图所示的转化关系。

①写出A与B反应生成C的化学方程式____________________________________ ;
②向50 mL4 mol·L-1的NaOH溶液中通入1.12 L B(标准状况),反应后溶液中溶质的物质的量之比为__________________________________ 。
(1)写出由其中两种元素组成的盐的电子式
(2)比较Y、Z离子半径大小
(3)已知W、Y、Z三种元素两两组合,可组成多种10电子微粒,请写出反应物生成物均为10电子微粒的离子方程式
(4)由W、X、Z三种元素可组成A、B、C三种常见的有机化合物,其中A是日常生活中常用调味品的主要成分,且A与B能够反应生成C,C是一种有香味的液体。试写出该反应的化学方程式
(5)由W、X、Y、Z四种元素中的三种元素组成的某种化合物,其浓溶液可与其中第四种元素的单质发生反应,写出该反应的化学方程式
(6)已知由元素X和Z可组成A、B、C、D四种中学化学中常见的单质或化合物,四种物质之间存在如图所示的转化关系。

①写出A与B反应生成C的化学方程式
②向50 mL4 mol·L-1的NaOH溶液中通入1.12 L B(标准状况),反应后溶液中溶质的物质的量之比为
您最近一年使用:0次



