2010·江西·三模
解题方法
1 . 有A、B、C、D、E、F、G七瓶不同物质的溶液,它们各是 、
、 、
、 、
、 、
、 、
、 和
和 溶液中的一种。为了鉴别,各取少量溶液进行两两混合,实验结果如下表所示。表中“↓”表示生成沉淀或微溶化合物,“-”表示观察不到明显现象。试回答下列问题。
溶液中的一种。为了鉴别,各取少量溶液进行两两混合,实验结果如下表所示。表中“↓”表示生成沉淀或微溶化合物,“-”表示观察不到明显现象。试回答下列问题。
(1)A的电子式是___________ ,G的化学式是___________ 。判断理由是___________ 。
(2)写出其余几种物质的化学式B___________ ,C___________ ,D___________ 。
(3)①写出D与E反应的化学方程式___________ ;
②G与过量氨水总反应的离子方程式___________ 。
 、
、 、
、 、
、 、
、 、
、 和
和 溶液中的一种。为了鉴别,各取少量溶液进行两两混合,实验结果如下表所示。表中“↓”表示生成沉淀或微溶化合物,“-”表示观察不到明显现象。试回答下列问题。
溶液中的一种。为了鉴别,各取少量溶液进行两两混合,实验结果如下表所示。表中“↓”表示生成沉淀或微溶化合物,“-”表示观察不到明显现象。试回答下列问题。| A | B | C | D | E | F | G | |
| A | - | - | - | - | - | - | ↓ |
| B | - | - | - | - | ↓ | ↓ | ↓ |
| C | - | - | - | ↓ | - | ↓ | ↓ |
| D | - | - | ↓ | - | ↓ | ↓ | ↓ |
| E | - | ↓ | - | ↓ | - | ↓ | - |
| F | - | ↓ | ↓ | ↓ | ↓ | - | ↓ |
| G | ↓ | ↓ | ↓ | ↓ | - | ↓ | - |
(2)写出其余几种物质的化学式B
(3)①写出D与E反应的化学方程式
②G与过量氨水总反应的离子方程式
您最近一年使用:0次
2010·江西宜春·一模
名校
解题方法
2 . 下图所示各物质是由1~20号元素中部分元素组成的单质或化合物,图中部分反应条件未列出。已知D、L、M为气体单质,C、E、H为气体化合物,反应②、④、⑥是化工生产中的重要反应,反应⑤是实验室制备气体C的重要方法。
请回答下列问题:
(1)物质E的结构式为__________ 。
(2)属于化合反应,但不属于氧化还原反应的是__________ (用编号填空)。
(3)C、H的熔沸点比较:C___ H(填““>”、“<”或“=”))原因是:________________ 。
(4)物质A由三种元素组成,1molA与水反应可生成1molB和2molC,A的化学式为
______________ 。
(5)在一定温度下,有甲、乙两容积相等的密闭容器。
I.向甲容器中通入3 mol M和4 mol L,反应达到平衡时,生成C的物质的量为a mol。此时,M的转化率为__________ 。下列能提高反应物L的转化率,但实际生产过程中并没有采用的措施是_____________ 。
①降低合成塔温度 ②适当增大压强
③不断分离出产物C ④加入合适催化剂
II.向乙中通入2 mol C,欲使反应达到平衡时,各物质的浓度与I中第一次平衡时相同,则起始时还需通入__________ mol M和__________ mol L。
III.若起始时,向乙中通入6mol M和8mol L,达到平衡时,生成C的物质的量为b mol,
则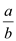
________  (选填“>”、“<”或“=”)。
(选填“>”、“<”或“=”)。

请回答下列问题:
(1)物质E的结构式为
(2)属于化合反应,但不属于氧化还原反应的是
(3)C、H的熔沸点比较:C
(4)物质A由三种元素组成,1molA与水反应可生成1molB和2molC,A的化学式为
(5)在一定温度下,有甲、乙两容积相等的密闭容器。
I.向甲容器中通入3 mol M和4 mol L,反应达到平衡时,生成C的物质的量为a mol。此时,M的转化率为
①降低合成塔温度 ②适当增大压强
③不断分离出产物C ④加入合适催化剂
II.向乙中通入2 mol C,欲使反应达到平衡时,各物质的浓度与I中第一次平衡时相同,则起始时还需通入
III.若起始时,向乙中通入6mol M和8mol L,达到平衡时,生成C的物质的量为b mol,
则
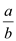
 (选填“>”、“<”或“=”)。
(选填“>”、“<”或“=”)。
您最近一年使用:0次
2010·江西·二模
解题方法
3 . 物质A有如下图所示转化关系,其中乙为金属单质,常温下,它在G 的浓溶液中发生钝化, F 的溶液中只含有一种溶质(有的反应可能在水溶液中进行,有的反应的生成物未全部给出,反应条件也未注明)。请讨论以下两种情况(注:两种情况下各字母代表的物质可能不同)

(1)第一种情况:A为气体;用两根玻璃棒分别蘸取 A、G的浓溶液并使它们接近时,有大量白烟生成;甲为焰色反应呈黄色的金属单质; D 和 F 的溶液均呈碱性。则:
① B与甲反应的化学方程式为________________________________________ 。
② D与乙反应的离子方程式为_______________________________________ 。
(2)第二种情况:A为黄色固体;甲可由两种单质直接化合得到; D 的水溶液加入用硝酸酸化的AgNO3溶液有白色沉淀生成。则:
① 工业上,反应 I 在___________________ (填设备名称)中进行。
② 甲的化学式为______________ 。
③ D和乙反应的离子方程式为________________________________________ 。
④ 请简述检验G溶液中阴离子的方法____________________________________
⑤ 若A的相对分子质量为M,反应Ⅰ、Ⅱ、Ⅲ均为完全转化。现取m克含A及少量杂质的样品,按上述过程充分反应后(杂质不参与反应),得到密度为ρg/cm3,溶质质量分数为a% 的G溶液n mL。则该样品中A的质量分数=_______ (列出计算式即可)。

(1)第一种情况:A为气体;用两根玻璃棒分别蘸取 A、G的浓溶液并使它们接近时,有大量白烟生成;甲为焰色反应呈黄色的金属单质; D 和 F 的溶液均呈碱性。则:
① B与甲反应的化学方程式为
② D与乙反应的离子方程式为
(2)第二种情况:A为黄色固体;甲可由两种单质直接化合得到; D 的水溶液加入用硝酸酸化的AgNO3溶液有白色沉淀生成。则:
① 工业上,反应 I 在
② 甲的化学式为
③ D和乙反应的离子方程式为
④ 请简述检验G溶液中阴离子的方法
⑤ 若A的相对分子质量为M,反应Ⅰ、Ⅱ、Ⅲ均为完全转化。现取m克含A及少量杂质的样品,按上述过程充分反应后(杂质不参与反应),得到密度为ρg/cm3,溶质质量分数为a% 的G溶液n mL。则该样品中A的质量分数=
您最近一年使用:0次
2010·江西·二模
4 . 短周期元素W、X、Y、Z、在元素周期表中的位置如图所示,
其中X、Y、Z三种元素的质子数之和为21。
(1)W与Z形成原子个数比为1∶1的化合物,其电子式为__________ 。
(2)Y的最高价氧化物对应的水化物与Y的氢化物恰好完全反应,生成物的水溶液呈
酸性,其原因是_____________________________________ (用化学用语表示);
该溶液中各种离子浓度由大到小的顺序为______________________________ 。
(3)由X W4、Z2和KOH溶液组成的新型燃料电池中,负极上发生反应的电极反应式为
__________________________________________________ 。
(4)已知:2YZ2(g) Y2Z4(g);△H<0。在恒温恒容条件下,将一定量XZ2和X2Z4的混合气体通入容积为2L的密闭容器中,反应过程中各物质的物质的量浓度c随时间
Y2Z4(g);△H<0。在恒温恒容条件下,将一定量XZ2和X2Z4的混合气体通入容积为2L的密闭容器中,反应过程中各物质的物质的量浓度c随时间
t的变化关系如下图所示。

① a、b、c、d四个点中,化学反应处于平衡状态的是__________ 点。
② 25 min时,增加了__________ (填物质的化学式)_______ mol。
③ a、b、c、d四个点中所表示的反应体系中,气体颜色由深到浅的顺序是________
(填字母)。
| W | |||||||
| X | Y | Z |
其中X、Y、Z三种元素的质子数之和为21。
(1)W与Z形成原子个数比为1∶1的化合物,其电子式为
(2)Y的最高价氧化物对应的水化物与Y的氢化物恰好完全反应,生成物的水溶液呈
酸性,其原因是
该溶液中各种离子浓度由大到小的顺序为
(3)由X W4、Z2和KOH溶液组成的新型燃料电池中,负极上发生反应的电极反应式为
(4)已知:2YZ2(g)
 Y2Z4(g);△H<0。在恒温恒容条件下,将一定量XZ2和X2Z4的混合气体通入容积为2L的密闭容器中,反应过程中各物质的物质的量浓度c随时间
Y2Z4(g);△H<0。在恒温恒容条件下,将一定量XZ2和X2Z4的混合气体通入容积为2L的密闭容器中,反应过程中各物质的物质的量浓度c随时间t的变化关系如下图所示。

① a、b、c、d四个点中,化学反应处于平衡状态的是
② 25 min时,增加了
③ a、b、c、d四个点中所表示的反应体系中,气体颜色由深到浅的顺序是
(填字母)。
您最近一年使用:0次
2010·江苏南通·三模
解题方法
5 . .下列转化关系图中,A、B、C、D、E常温下为气体,B、E、F、K为单质,其中F为黑色固体;C、D均能使澄清的石灰水变浑浊,D、E均能使品红溶液褪色;I是一种红棕色固体氧化物。
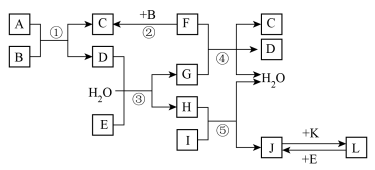
请回答下列问题:
⑴C的电子式为。
⑵检验溶液L中金属阳离子的方法是。
⑶反应③的离子方程式为。
⑷F与G的浓溶液反应的化学方程式为。
⑸气体A的密度为2.68g·L-1(标准状况),通过计算、推理,可确定A的分子式为。

请回答下列问题:
⑴C的电子式为。
⑵检验溶液L中金属阳离子的方法是。
⑶反应③的离子方程式为。
⑷F与G的浓溶液反应的化学方程式为。
⑸气体A的密度为2.68g·L-1(标准状况),通过计算、推理,可确定A的分子式为。
您最近一年使用:0次
2010·江西九江·二模
解题方法
6 . 甲、乙、丙为三种短周期元素组成的单质,X、Y是化合物,相互转化的关系如下图所示(图中反应条件未注明,反应不产生其它物质)。请回答下列问题:

(1)若X是水,甲、乙中的元素同一周期,写出甲和X反应的化学方程式_______ 。
(2)若Y是水,甲、乙中的元素同一主族,写出甲与X反应的化学方程式_______ 。
(3)若X、Y均为氧化物,若中X常温下为气态,Y常温下为固态,X为______ 分子(填极性或非极性);用电子式表示Y的形成过程______________ 。
(4)若X、Y均为氧化物,其中X常温下为固态,Y常温下为气态,则固体X熔化时破坏的是__________ (填共价键、离子键、金属键),请写出乙的一种用途________ 。

(1)若X是水,甲、乙中的元素同一周期,写出甲和X反应的化学方程式
(2)若Y是水,甲、乙中的元素同一主族,写出甲与X反应的化学方程式
(3)若X、Y均为氧化物,若中X常温下为气态,Y常温下为固态,X为
(4)若X、Y均为氧化物,其中X常温下为固态,Y常温下为气态,则固体X熔化时破坏的是
您最近一年使用:0次
真题
名校
7 . 短周期元素W、X、Y、Z的原子序数依次增加。m、p、r是由这些元素组成的二元化合物,n是元素Z的单质,通常为黄绿色气体,q的水溶液具有漂白性,0.01mol·L-1r溶液的pH为2,s通常是难溶于水的混合物。上述物质的转化关系如图所示。下列说法正确的是( )
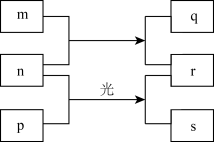

| A.原子半径的大小W <X<Y | B.元素的非金属性Z>X>Y |
| C.Y的氢化物常温常压下为液态 | D.X的最高价氧化物的水化物为强酸 |
您最近一年使用:0次
2016-06-10更新
|
6313次组卷
|
42卷引用:江西省新余市2017届高三下学期二模理综化学试卷
江西省新余市2017届高三下学期二模理综化学试卷江西省南昌市第三中学2016-2017学年高一下学期5月月考化学试题2016年全国普通高等学校招生统一考试化学(新课标1卷精编版)2015-2016学年河北省唐山市开滦一中高一下期末理科化学试卷湖北省武汉市第二中学、麻城市第一中学2016-2017学年高一下学期期中联考化学试题山东省泰安市第一中学2016-2017学年高一下学期学情检测化学试题2018版化学(苏教版)高考总复习专题五对接高考精练--元素周期律和元素周期表重庆市垫江县2018届高三上学期模底考试理综化学试题北京市一零一中学2018届高三10月月考化学试题人教版2017-2018学年高一化学必修二同步训练:第一章 物质结构 元素周期律北京市人大附中2017-2018学年下学期高一第一次月考 化学试卷福建省厦门市双十中学2017-2018学年高一下学期期中考试化学试题(已下线)《考前20天终极攻略》-5月19日 物质结构 元素周期律(已下线)解密07 物质结构和元素周期律(教师版)——备战2018年高考化学之高频考点解密安徽省合肥市合肥六中2017-2018学年高一下学期期中考试化学试题【全国百强校】陕西省西安市长安区第一中学2017-2018学年高一下学期期末考试(理)化学试题【全国百强校】河南省南阳市第一中学2017-2018学年高一下学期期末考前模拟化学试题(已下线)2019高考备考二轮复习精品资料-专题7 物质结构与元素周期律(教学案)2016年全国普通高等学校招生统一考试化学(全国1卷参考版)【全国百强校】四川省成都市第七中学2018-2019学年高一下学期3月月考化学试题湖南省邵阳市邵东县第十中学2020届高三9月月考(读论班)化学试题黑龙江省绥化市安达市第七中学2019-2020学年高二上学期月考化学试题山东省滕州市第一中学2020届高三3月线上模拟考试化学试题(已下线)专题八 物质结构与元素周期律(真题汇编)-2020年高考二轮模块化复习之《化学基本原理》名师讲案与提分特训安徽省黄山市屯溪第一中学2019-2020学年高一下学期入学考试化学试题河南省商丘市第一高级中学2019-2020学年高一下学期期末考试化学试题(已下线)第14讲 元素周期表和元素周期律-2021年高考化学一轮复习名师精讲练河南省南阳市第一中学2019-2020学年高一下学期期末考前模拟化学试题云南省玉溪一中2020-2021学年高二上学期第一次月考化学试题(已下线)第18讲 元素周期律和元素周期表(精练)-2021年高考化学一轮复习讲练测(已下线)专题讲座(五) “位-构-性”综合推断题的解题方法(精讲)——2021年高考化学一轮复习讲练测(已下线)练习14 元素周期表和元素周期律的应用-2020-2021学年【补习教材·寒假作业】高一化学(人教版)(已下线)专题04 物质结构和元素周期律——备战2021年高考化学纠错笔记(已下线)专题讲座(三)“位-构-性”综合推断题的解题方法(练) — 2022年高考化学一轮复习讲练测(新教材新高考)(已下线)专题05 元素周期律-【微专题·大素养】备战2022年高考化学讲透提分要点云南省弥勒市第一中学2021-2022学年高二上学期第三次月考化学试题(已下线)第一部分 二轮专题突破 专题9 “位—构—性”综合推断(已下线)专题12 元素周期律推断-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)(已下线)第五章 物质结构与性质 元素周期律 第28讲 元素推断与无机物的性质(已下线)题型79 以框图推断为载体考查元素周期律(已下线)专题07 突破原子结构和元素周期表(律)(选择题)-2023年高考化学毕业班二轮热点题型归纳与变式演练(全国通用)福建省泉州市三校2022-2023学年高二下学期4月期中联考化学试题
2010·江西新余·三模
8 . 现有A、B、C、D、E五种可溶强电解质,它们在水中可电离产生下列离子(各种离子不重复)。
已知:①A、B两溶液呈碱性;C、D、E溶液呈酸性。
②向E溶液中逐滴滴加B溶液至过量,沉淀量先增加后减少但不消失。
③D溶液与另外四种溶液反应都能产生沉淀。
试回答下列问题:
(1)A溶液呈碱性的原因是 。
(2)写出E溶液与过量的B溶液反应的离子方程式 。
(3)已知:NaOH(aq)+HNO3(aq)=NaNO3(aq)+H2O(1);△H=" —a" kJ·mol-1。
请写出相同条件下B与C的稀溶液反应的热化学方程式 。
(4)若25°时C、E溶液pH=4,则E溶液中水电离出的氢离子浓度是C溶液中水电离出的氢离子浓度 倍。
(5)将C溶液逐滴加入等体积、等物质的量的浓度的A溶液中,反应后溶液中一价离子(+1或一1)浓度由大到小的顺序为: 。
| 阳离子 | H+、Na+、Al3+、Ag+、Ba2+ |
| 阴离子 | OH—、Cl—、CO32—、NO3—、SO42— |
已知:①A、B两溶液呈碱性;C、D、E溶液呈酸性。
②向E溶液中逐滴滴加B溶液至过量,沉淀量先增加后减少但不消失。
③D溶液与另外四种溶液反应都能产生沉淀。
试回答下列问题:
(1)A溶液呈碱性的原因是 。
(2)写出E溶液与过量的B溶液反应的离子方程式 。
(3)已知:NaOH(aq)+HNO3(aq)=NaNO3(aq)+H2O(1);△H=" —a" kJ·mol-1。
请写出相同条件下B与C的稀溶液反应的热化学方程式 。
(4)若25°时C、E溶液pH=4,则E溶液中水电离出的氢离子浓度是C溶液中水电离出的氢离子浓度 倍。
(5)将C溶液逐滴加入等体积、等物质的量的浓度的A溶液中,反应后溶液中一价离子(+1或一1)浓度由大到小的顺序为: 。
您最近一年使用:0次



