名校
解题方法
1 . 利用如图所示装置进行Cl2的制备及性质检验实验。下列说法不正确的是
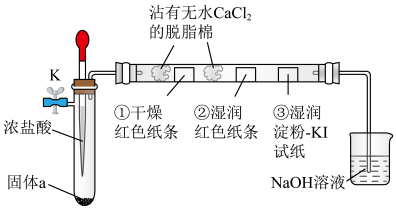
| A.固体a可为KMnO4 |
| B.①处纸条无明显现象且②处纸条褪色,说明Cl2具有漂白性 |
| C.③处试纸变蓝,说明氧化性:Cl2>I2 |
D.实验结束后,打开止水夹 向装置中鼓入空气以促进尾气吸收 向装置中鼓入空气以促进尾气吸收 |
您最近一年使用:0次
2024-04-28更新
|
706次组卷
|
2卷引用:广东省深圳市2024届高三二模考试化学试题
名校
解题方法
2 . 亚硝酰氯(NOCl,熔点:-64.5℃,沸点:-5.5℃)是一种黄色气体,遇水易水解。可用于合成清洁剂、触媒剂及中间体等。实验室可由氯气与一氧化氮在常温常压下合成。
(1)甲组同学拟用同一装置Ⅰ、Ⅱ、Ⅲ分别制备纯净干燥的NO和
_______ 。写出该装置制备氯气的离子方程式:_______ 。
(2)乙组同学利用甲组制得的NO和 制备NOCl,装置如图所示:
制备NOCl,装置如图所示:________ 。
②装置连接顺序为a→________ (按气流自左向右方向,用小写字母表示)。
③装置Ⅷ中吸收尾气时,NOCl发生反应的化学方程式为_______ 。
(3)丙组同学查阅资料,查得王水是浓硝酸与浓盐酸的混酸,一定条件下混酸可生成亚硝酰氯和氯气,该反应的化学方程式为______ 。
(4)丁组同学用以下方法测定亚硝酰氯(NOCl)纯度:取Ⅷ中所得液体m克溶于水,配制成250mL溶液,取出25.00 mL,用c mol/L 溶液反应,消耗
溶液反应,消耗 溶液的体积为bmL。亚硝酰氯(NOCl)的质量分数为
溶液的体积为bmL。亚硝酰氯(NOCl)的质量分数为________ (用代数式表示即可)。
(1)甲组同学拟用同一装置Ⅰ、Ⅱ、Ⅲ分别制备纯净干燥的NO和

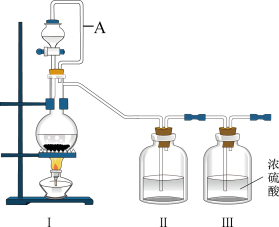
(2)乙组同学利用甲组制得的NO和
 制备NOCl,装置如图所示:
制备NOCl,装置如图所示: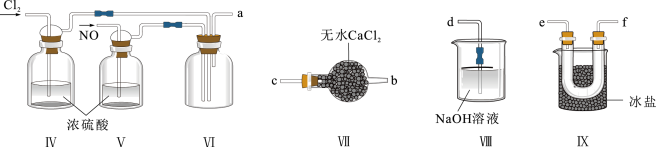
②装置连接顺序为a→
③装置Ⅷ中吸收尾气时,NOCl发生反应的化学方程式为
(3)丙组同学查阅资料,查得王水是浓硝酸与浓盐酸的混酸,一定条件下混酸可生成亚硝酰氯和氯气,该反应的化学方程式为
(4)丁组同学用以下方法测定亚硝酰氯(NOCl)纯度:取Ⅷ中所得液体m克溶于水,配制成250mL溶液,取出25.00 mL,用c mol/L
 溶液反应,消耗
溶液反应,消耗 溶液的体积为bmL。亚硝酰氯(NOCl)的质量分数为
溶液的体积为bmL。亚硝酰氯(NOCl)的质量分数为
您最近一年使用:0次
名校
解题方法
3 . 下列关于物质的制备、分离提纯或性质检验叙述正确的是

| A.甲装置:可用石英坩埚或陶瓷坩埚灼烧氢氧化钠固体 |
| B.实验室中可在乙装置中用CaF2与浓硫酸加热条件下制HF气体 |
| C.可用丙装置分离固体食盐和碘 |
| D.通过丁装置试管中下层液体呈紫红色,一定可以说明非金属性:Cl>Br>I |
您最近一年使用:0次
2024-04-01更新
|
196次组卷
|
3卷引用:广东省深圳市高级中学2023-2024学年高一下学期4月期中考试化学试题
名校
解题方法
4 . 下列离子方程式书写正确的是
A.向 溶液中滴加稀硫酸: 溶液中滴加稀硫酸: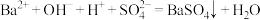 |
B.向 溶液中通入足量 溶液中通入足量 : :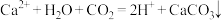 |
C.向 溶液中加入 溶液中加入 : :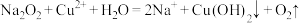 |
D.二氧化锰和浓盐酸反应: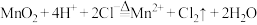 |
您最近一年使用:0次
名校
解题方法
5 . X、Y、Z、W为短周期主族元素,原子序数依次增加,G为温室气体,H为淡黄色固体,W原子在所在周期中半径最小.下列叙述正确的是


| A.③为置换反应 | B.X的氧化物有毒 |
| C.W单质能与Y的简单氢化物反应 | D.Y、W的简单氢化物均为酸 |
您最近一年使用:0次
6 . 元素及其化合物性质丰富。下列相关反应的化学方程式或离子方程式书写正确的是
A.将 置于水中: 置于水中: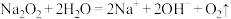 |
B.将 通入石灰乳中: 通入石灰乳中: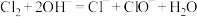 |
C.水蒸气通过灼热铁粉: |
D.氨的催化氧化: |
您最近一年使用:0次
2024-03-22更新
|
487次组卷
|
2卷引用:2024届广东省深圳市高三下学期一模考试化学试卷
名校
解题方法
7 . 利用下图所示装置进行实验,先向W形管中通入 ,一段时间后,再用注射器向其中加入浓盐酸,当
,一段时间后,再用注射器向其中加入浓盐酸,当 充满整个W形管后点燃酒精灯,下列说法正确的是
充满整个W形管后点燃酒精灯,下列说法正确的是
 ,一段时间后,再用注射器向其中加入浓盐酸,当
,一段时间后,再用注射器向其中加入浓盐酸,当 充满整个W形管后点燃酒精灯,下列说法正确的是
充满整个W形管后点燃酒精灯,下列说法正确的是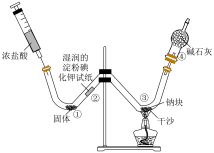
A.①处固体为 |
B.②处试纸变蓝,说明 具有氧化性 具有氧化性 |
| C.③处可观察到钠块剧烈燃烧,且产生大量白雾 |
D.④处碱石灰的主要作用是防止空气中的 、水蒸气与钠反应 、水蒸气与钠反应 |
您最近一年使用:0次
2024-03-22更新
|
760次组卷
|
3卷引用:2024届广东省深圳市高三下学期一模考试化学试卷
2024届广东省深圳市高三下学期一模考试化学试卷(已下线)通关练03 常考化学实验基础知识-【查漏补缺】2024年高考化学复习冲刺过关(新高考专用)广东省茂名市高州中学2023-2024学年高一下学期期中考试化学试题
8 . 某小组同学用 与浓盐酸反应制备
与浓盐酸反应制备 的过程中(装置如下图所示),观察到氯气不再逸出时,固液混合物
的过程中(装置如下图所示),观察到氯气不再逸出时,固液混合物 中仍存在盐酸和
中仍存在盐酸和 .
.

(1)发生装置中制取
 的
的(2)除杂装置①中的试剂是______(填序号)。
| A.浓硫酸 | B.饱和 溶液 溶液 |
C.饱和 溶液 溶液 | D. 溶液 溶液 |
(3)将虚线框中的收集装置补充完整
(4)尾气处理装置中发生反应的
(5)分析
 中仍存在盐酸和
中仍存在盐酸和 的可能原因。
的可能原因。ⅰ.随 降低或
降低或 浓度升高,
浓度升高, 氧化性减弱。
氧化性减弱。
ⅱ.随 降低,
降低,
设计补充实验证实上述分析。
实验操作 | 试剂 | 产物 | |
Ⅰ |
| 较浓 | 有氯气 |
Ⅱ |
| 有氯气 | |
Ⅲ |
| 无氯气 |
则 是
是 是
是
您最近一年使用:0次
9 . 某实验小组用如图装置制备氯气并探究其性质(夹持装置已省略),下列分析错误的是
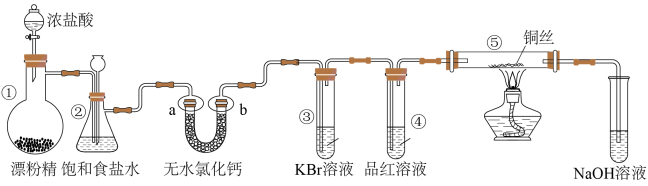

| A.用MnO2代替装置中的漂粉精也可以达到实验目的 |
| B.a、b处分别放干燥和湿润的有色布条,无法说明干燥的Cl2不具有漂白性 |
| C.反应开始后可观察到③中溶液变黄,④中溶液褪色,说明氯水具有氧化性和漂白性 |
| D.反应开始后点燃酒精灯,可在⑤号硬质玻璃管中观察到棕黄色烟 |
您最近一年使用:0次
名校
10 . 设NA为阿伏加德罗常数的值.下列说法正确的是
| A.在1 L0.1 mol/LHNO3溶液中氧原子总数为0.3NA |
| B.0.1 mol Fe和0.1 mol氯气充分反应,转移的电子数为0.3NA |
| C.1 mol N2与足量的H2反应,生成的NH3分子总数为2NA |
| D.60 g SiO2中含有Si-O单键数为4NA |
您最近一年使用:0次






