解题方法
1 . 高铁酸钠(Na2FeO4)是一种新型绿色消毒剂,主要用于饮用水处理。如图所示物质转化关系为高铁酸钠的一种制备方法及有关性质实验(部分反应产物已略去)。已知 A、F 为非金属单质气体,B为常见金属单质,E 为生活中最常见的调味品,F 在标准状况下密度为 0.090g·L-1。

请回答下列问题:
(1)写出 D 的名称___________ ,Na2FeO4中 Fe 元素的化合价为___________ 。
(2)反应③,F 在 A 中点燃的反应现象为___________ 。
(3)写出反应④的化学方程式,并用“双线桥”表示电子转移的方向和数目:___________ 。

请回答下列问题:
(1)写出 D 的名称
(2)反应③,F 在 A 中点燃的反应现象为
(3)写出反应④的化学方程式,并用“双线桥”表示电子转移的方向和数目:
您最近一年使用:0次
名校
解题方法
2 . 高铁酸钠 是一种新型绿色消毒剂,主要用于饮用水处理。如图所示物质转化关系为高铁酸钠的一种制备方法及有关性质实验(部分反应产物已略去)。已知A、F为非金属单质气体,B为常见金属单质,E为生活中最常见的调味品,F在标准状况下密度为0.090g/L。
是一种新型绿色消毒剂,主要用于饮用水处理。如图所示物质转化关系为高铁酸钠的一种制备方法及有关性质实验(部分反应产物已略去)。已知A、F为非金属单质气体,B为常见金属单质,E为生活中最常见的调味品,F在标准状况下密度为0.090g/L。
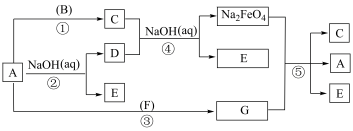
请回答下列问题:
(1)D是一种消毒液的主要成分,写出D的名称______ , 中Fe元素的化合价为
中Fe元素的化合价为______ 。
(2)利用C的饱和溶液可以配制与C溶液不同类型分散系,可利用______ 区别两种分散系。
(3)反应③,F在A中点燃的反应现象为:______ 。
(4)写出反应④的化学方程式:______ 。
(5)反应⑤中氧化剂和还原剂的物质的量之比为:______ 。
 是一种新型绿色消毒剂,主要用于饮用水处理。如图所示物质转化关系为高铁酸钠的一种制备方法及有关性质实验(部分反应产物已略去)。已知A、F为非金属单质气体,B为常见金属单质,E为生活中最常见的调味品,F在标准状况下密度为0.090g/L。
是一种新型绿色消毒剂,主要用于饮用水处理。如图所示物质转化关系为高铁酸钠的一种制备方法及有关性质实验(部分反应产物已略去)。已知A、F为非金属单质气体,B为常见金属单质,E为生活中最常见的调味品,F在标准状况下密度为0.090g/L。
请回答下列问题:
(1)D是一种消毒液的主要成分,写出D的名称
 中Fe元素的化合价为
中Fe元素的化合价为(2)利用C的饱和溶液可以配制与C溶液不同类型分散系,可利用
(3)反应③,F在A中点燃的反应现象为:
(4)写出反应④的化学方程式:
(5)反应⑤中氧化剂和还原剂的物质的量之比为:
您最近一年使用:0次
3 . 以生活中常见的调味品X为原料可以制备多种物质。下图是几种常见物质的转化关系图(部分产物和反应条件已略去),其中B、C、G都是单质,常温下B、C为气体,I为红棕色固体,J是白色沉淀。

请回答下列问题:
(1)C的化学式是___________ 。
(2)反应②的离子方程式是___________ 。
(3)H露置于空气中发生反应的化学方程式是___________ 。
(4)设计检验F中阳离子的实验方案___________ 。

请回答下列问题:
(1)C的化学式是
(2)反应②的离子方程式是
(3)H露置于空气中发生反应的化学方程式是
(4)设计检验F中阳离子的实验方案
您最近一年使用:0次
4 . 如图所示物质之间的转化,已知:A是金属单质,且焰色试验为黄色,Y是非金属单质,且呈黄绿色,X为常见温室气体。按要求回答下列问题:
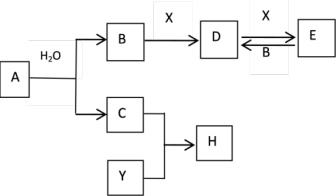
(1)E的化学式:___________ ;E常用来治疗胃酸过多,写出此反应的离子方程式:___________ ;
(2)写出A→B的离子方程式,并用双线桥法 标出电子转移的方向和数目:___________ 。
(3)C在Y中燃烧的实验现象:___________ 。

(1)E的化学式:
(2)写出A→B的离子方程式,并用
(3)C在Y中燃烧的实验现象:
您最近一年使用:0次
21-22高一上·浙江·阶段练习
解题方法
5 . 室温下,单质A、单质B、单质C分别为固体、黄绿色气体、无色气体。在一定条件下,它们之间的转化关系如图所示,已知E溶液是无色的。请回答下列问题:
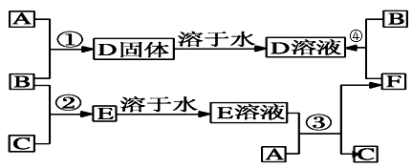
(1)反应①的化学方程式为___ 。
(2)反应③的化学方程式为____ 。
(3)反应④的化学方程式为___ 。

(1)反应①的化学方程式为
(2)反应③的化学方程式为
(3)反应④的化学方程式为
您最近一年使用:0次
2021高三·浙江·专题练习
解题方法
6 . KIO3是一种重要的无机化合物,可作为食盐中的补碘剂。回答下列问题:
(1)KIO3的化学名称是___________________________________ 。
(2)利用“KClO3氧化法”制备KIO3工艺流程如下图所示:

“酸化反应”所得产物有KH(IO3)2、Cl2和KCl。“逐Cl2”采用的方法是_______________________________ 。“滤液”中的溶质主要是____________ 。“调pH”中发生反应的化学方程式为___________________________________ 。
(1)KIO3的化学名称是
(2)利用“KClO3氧化法”制备KIO3工艺流程如下图所示:

“酸化反应”所得产物有KH(IO3)2、Cl2和KCl。“逐Cl2”采用的方法是
您最近一年使用:0次
20-21高一上·浙江·期中
解题方法
7 . 下图是部分短周期元素的单质及其化合物(或其溶液)的转化关系。已知B、C、D是非金属单质,且在常温常压下都是气体,D常用于自来水的杀菌、消毒;化合物G的焰色试验呈黄色,化合物F通常状态下呈气态。请回答下列问题。

(1)写出B和G的化学式: B___________ ;G___________ 。
(2) A~F物质中属于离子化合物的是___________ (填化学式),含有极性共价键的物质是___________ (填化学式)。
(3)写出E转化成G的化学方程式,用双线桥标出电子转移数目:___________ 。
(4)设计实验方案检验F溶液中阴离子___________ 。

(1)写出B和G的化学式: B
(2) A~F物质中属于离子化合物的是
(3)写出E转化成G的化学方程式,用双线桥标出电子转移数目:
(4)设计实验方案检验F溶液中阴离子
您最近一年使用:0次
19-20高一·浙江·阶段练习
8 . 有X、Y、Z、W四种元素,它们的单质X、Y、Z在常温常压下皆为气体,W为固体。
①X单质可在Z单质中燃烧生成XZ,火焰为苍白色;W在Y单质中燃烧产生黄色火焰,生成W2Y2。
②每2分子X2可与1分子Y2化合生成2分子X2Y,X2Y在常温下为液体;
③化合物XZ的水溶液可使蓝色石蕊试纸变红;W与水反应后的溶液可使无色酚酞试液变红色;
④Z单质溶于化合物X2Y,所得溶液具有漂白作用;
请回答:
(1) W2Y2的化学式__________ ;X2Y的化学式__________ 。
(2)画出W原子的原子结构示意图_________ ;少量的W可保存在______ 中(填试剂名称)。
(3)Z单质与X2Y反应的化学方程式___________ 。
(4)W单质与X2Y反应的离子方程式________ 。
(5)完成W2Y2与X2Y反应方程式,并标出电子转移的方向与数目:________ 。
①X单质可在Z单质中燃烧生成XZ,火焰为苍白色;W在Y单质中燃烧产生黄色火焰,生成W2Y2。
②每2分子X2可与1分子Y2化合生成2分子X2Y,X2Y在常温下为液体;
③化合物XZ的水溶液可使蓝色石蕊试纸变红;W与水反应后的溶液可使无色酚酞试液变红色;
④Z单质溶于化合物X2Y,所得溶液具有漂白作用;
请回答:
(1) W2Y2的化学式
(2)画出W原子的原子结构示意图
(3)Z单质与X2Y反应的化学方程式
(4)W单质与X2Y反应的离子方程式
(5)完成W2Y2与X2Y反应方程式,并标出电子转移的方向与数目:
您最近一年使用:0次
19-20高一·浙江·阶段练习
解题方法
9 . 室温下,单质A、B、C分别为银白色固体、黄绿色气体、无色气体,且A在空气中燃烧会变成淡黄色粉末。在合适的反应条件下,它们可以按下面框图进行反应,且E溶液是无色的。请据图回答:

(1)写出下列物质的化学式:A_____ ;B_______ ;C______________ 。
(2)写出下列反应的化学方程式:
反应①___________________ ;
反应②__________________ ;
反应③___________________ 。
(3)实验室中保存少量单质A的方法是_________ ,A在空气中燃烧后所得产物中氧元素的化合价是_____________ 。

(1)写出下列物质的化学式:A
(2)写出下列反应的化学方程式:
反应①
反应②
反应③
(3)实验室中保存少量单质A的方法是
您最近一年使用:0次
19-20高二·浙江·期末
解题方法
10 . 现有金属单质A、B和气体甲、乙、丙及物质C、D、E、F它们之间能发生如下反应(图中有些反应的产物和反应的条件没有全部标出)。
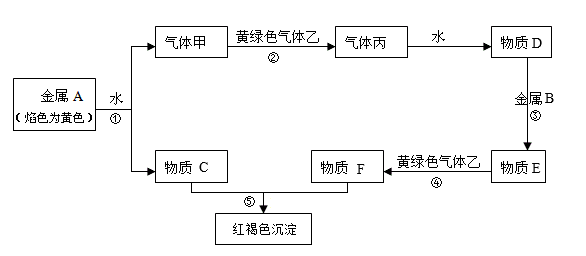
请根据以上信息回答下列问题:
(1)写出下列物质的化学式:A________ 、丙________
(2)写出下列反应化学方程式:
反应①________________
反应⑤________________

请根据以上信息回答下列问题:
(1)写出下列物质的化学式:A
(2)写出下列反应化学方程式:
反应①
反应⑤
您最近一年使用:0次



