名校
1 . 高铁酸钾(K2FeO4)是一种新型、高效、多功能水处理剂。
已知:①K2FeO4为紫色固体,微溶于KOH溶液
②在碱性条件下,次氯酸盐(MClO)可将Fe(OH)3氧化成高铁酸盐(M2FeO4)。
④K2FeO4具有强氧化性,在酸性或中性溶液中迅速产生O2,在碱性溶液中较稳定。某学习小组设计了下面的实验制备K2FeO4并探究其性质。
(1)K2FeO4的制备
该小组用如图所示装置制备K2FeO4(夹持装置路)。
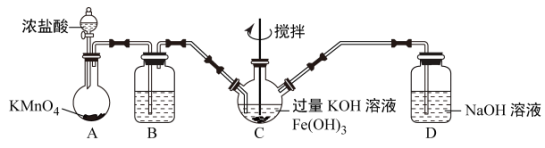
①K2FeO4中铁元素的化合价为___ 价。
②以上装置图中有一处明显的错误请你帮助指出来:___ 。
③A装置作用是产生黄绿色氯气(Cl2),写出A中发生反应的离子方程式__ 。
④C中发生的反应有Cl2+2KOH=KCl+KClO+H2O,还有生成K2FeO4的反应。写出得到K2FeO4的化学方程式为___ 。
(2)性质探究
用KOH溶液充分洗涤C中所得固体得到固体物质K2FeO4
①絮凝实验:甲同学取少量K2FeO4加入浑的泥浆水中,发现产生气体,搅拌,浑浊的泥浆水很快澄清。查阅资料此时发生反应的离子方程式为:4FeO +10H2O=4Fe(OH)3(胶体)+3O2↑+8OH-,请结合方程式,说明K2FeO4的净水原理:
+10H2O=4Fe(OH)3(胶体)+3O2↑+8OH-,请结合方程式,说明K2FeO4的净水原理:___ 。
②乙同学取少量K2FeO4,向其中滴入稀盐酸发现产生黄绿色气体。产生黄绿色气体的原因可能是___ 。(用文字描述)
已知:①K2FeO4为紫色固体,微溶于KOH溶液
②在碱性条件下,次氯酸盐(MClO)可将Fe(OH)3氧化成高铁酸盐(M2FeO4)。
④K2FeO4具有强氧化性,在酸性或中性溶液中迅速产生O2,在碱性溶液中较稳定。某学习小组设计了下面的实验制备K2FeO4并探究其性质。
(1)K2FeO4的制备
该小组用如图所示装置制备K2FeO4(夹持装置路)。

①K2FeO4中铁元素的化合价为
②以上装置图中有一处明显的错误请你帮助指出来:
③A装置作用是产生黄绿色氯气(Cl2),写出A中发生反应的离子方程式
④C中发生的反应有Cl2+2KOH=KCl+KClO+H2O,还有生成K2FeO4的反应。写出得到K2FeO4的化学方程式为
(2)性质探究
用KOH溶液充分洗涤C中所得固体得到固体物质K2FeO4
①絮凝实验:甲同学取少量K2FeO4加入浑的泥浆水中,发现产生气体,搅拌,浑浊的泥浆水很快澄清。查阅资料此时发生反应的离子方程式为:4FeO
 +10H2O=4Fe(OH)3(胶体)+3O2↑+8OH-,请结合方程式,说明K2FeO4的净水原理:
+10H2O=4Fe(OH)3(胶体)+3O2↑+8OH-,请结合方程式,说明K2FeO4的净水原理:②乙同学取少量K2FeO4,向其中滴入稀盐酸发现产生黄绿色气体。产生黄绿色气体的原因可能是
您最近一年使用:0次
2021-09-17更新
|
322次组卷
|
2卷引用:陕西省榆林市第十二中学2021-2022学年高三上学期班级教学自主质量评估测试化学试题
名校
解题方法
2 . 双氧水和含氯消毒剂是生活中常用的消毒剂,了解物质的性质是科学合理使用化学品的基础和前提。请回答下列问题:
(1)某同学设计如下实验研究H2O2的性质:
①从理论上看H2O2既有氧化性又有还原性,具有还原性的原因是_______ 。
②能证明H2O2具有还原性的实验是_______ (填序号),写出该过程的离子方程式_______ 。
(2)“84”消毒液的有效成分为NaClO。
①将Cl2通入NaOH溶液中可制得“84”消毒液,反应的化学方程式_______ 。
②“84”消毒液不能与洁厕灵(主要成分为盐酸)混用的原因_______ (用化学用语解释其原理)。
(3)二氧化氯(ClO2)是广谱性具有强氧化性的高效低毒的消毒剂。
①用NaClO3氧化浓盐酸来制取ClO2,同时有Cl2生成,该过程的化学方程式为_______ 。
②若上述反应产生0.1 mol Cl2,转移电子的物质的量为_______ mol。
③ClO2消毒的效率(以单位质量得到电子数表示)是Cl2的_______ 倍。
(1)某同学设计如下实验研究H2O2的性质:
| 序号 | 实验 | 实验现象 |
| i | 向5%H2O2溶液中滴加酸性KMnO4溶液 | a.溶液紫色褪去 b.有大量气泡产生 |
| ii | 向5%H2O2溶液中滴加淀粉碘化钾溶液 | c.溶液变蓝 |
②能证明H2O2具有还原性的实验是
(2)“84”消毒液的有效成分为NaClO。
①将Cl2通入NaOH溶液中可制得“84”消毒液,反应的化学方程式
②“84”消毒液不能与洁厕灵(主要成分为盐酸)混用的原因
(3)二氧化氯(ClO2)是广谱性具有强氧化性的高效低毒的消毒剂。
①用NaClO3氧化浓盐酸来制取ClO2,同时有Cl2生成,该过程的化学方程式为
②若上述反应产生0.1 mol Cl2,转移电子的物质的量为
③ClO2消毒的效率(以单位质量得到电子数表示)是Cl2的
您最近一年使用:0次
3 . 如图为实验室制取纯净、干燥的Cl2,并用Cl2与铜反应。
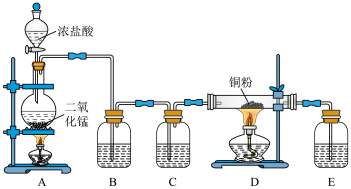
试回答下列问题:
(1)写出A中反应的离子方程式___________ 。
(2)反应中浓盐酸显示出来的性质是___________。
(3)为得到干燥纯净的氯气,一般在B瓶中加入饱和食盐水,C瓶中加入___________ 试剂。(填试剂名称)
(4)装置E的作用是___________ ;E处发生反应的离子方程式为___________ 。

试回答下列问题:
(1)写出A中反应的离子方程式
(2)反应中浓盐酸显示出来的性质是___________。
| A.只有还原性 | B.还原性和酸性 | C.只有氧化性 | D.氧化性和酸性 |
(3)为得到干燥纯净的氯气,一般在B瓶中加入饱和食盐水,C瓶中加入
(4)装置E的作用是
您最近一年使用:0次
解题方法
4 . 下图是实验室制备 的实验装置图,其中甲为氯气的发生装置,丙装置中反应的离子方程式为
的实验装置图,其中甲为氯气的发生装置,丙装置中反应的离子方程式为 (未配平)。(资料:
(未配平)。(资料: 为紫色固体,微溶于
为紫色固体,微溶于 ,在碱性环境中稳定,具有强氧化性)下列说法不正确的是
,在碱性环境中稳定,具有强氧化性)下列说法不正确的是

 的实验装置图,其中甲为氯气的发生装置,丙装置中反应的离子方程式为
的实验装置图,其中甲为氯气的发生装置,丙装置中反应的离子方程式为 (未配平)。(资料:
(未配平)。(资料: 为紫色固体,微溶于
为紫色固体,微溶于 ,在碱性环境中稳定,具有强氧化性)下列说法不正确的是
,在碱性环境中稳定,具有强氧化性)下列说法不正确的是
A.B装置的作用是干燥水,所用试剂为浓 |
| B.工业上利用D中所发生的反应原理制备漂白液 |
| C.三颈烧瓶中使用搅拌器的目的是加快反应速率,增大反应物的利用率 |
D.A中浓盐酸中的 在该反应中既失电子又为反应提供所需的酸性环境 在该反应中既失电子又为反应提供所需的酸性环境 |
您最近一年使用:0次
5 . 某实验小组制取“84”消毒液(主要成分为NaClO)并探究其性质。
[查阅资料]
①常温下:16HCl(浓)+2KMnO4=2MnCl2+81H2O+2KCl+5Cl2↑;
②苯为有机物,密度比水小且不溶于水;
③氯、溴、碘的单质均易溶于有机溶剂。
I.制取NaClO的装置如图1所示(夹持装置略):

(1)仪器a的名称为_____ 。
(2)装置B中发生反应的化学方程式为_____ 。
(3)上述装置存在一个缺陷,会导致“84”消毒液的产率降低,改进的方法是_____ 。
II.探究“84”消毒液的性质:
(4)为验证“84”消毒液的某些性质,实验小组设计图2实验方案。观察到试管1中溶液不褪色;试管2中溶液变蓝,短时间内无明显现象;试管3中溶液先变蓝,通入CO2后,溶液快速褪色。
①试管1的作用是_____ 。
②由试管2、3的现象可得到的结论是_____ 。
③若将试管3中通入的CO2换成盐酸也可达到相同的效果,且速度更快,但有可能产生Cl2而带来不良的实验后果,试用离子方程式解释产生Cl2的原因_____ 。
(5)同学们观察到“84”消毒液的液体呈浅黄绿色,猜想其中可能溶有氯气。现设计实验证明“84”消毒液中溶有氯气,可供选择的实验仪器、药品:试管、苯、酒精、“84”消毒液。请你简述实验操作、现象及结论_____ 。
[查阅资料]
①常温下:16HCl(浓)+2KMnO4=2MnCl2+81H2O+2KCl+5Cl2↑;
②苯为有机物,密度比水小且不溶于水;
③氯、溴、碘的单质均易溶于有机溶剂。
I.制取NaClO的装置如图1所示(夹持装置略):

(1)仪器a的名称为
(2)装置B中发生反应的化学方程式为
(3)上述装置存在一个缺陷,会导致“84”消毒液的产率降低,改进的方法是
II.探究“84”消毒液的性质:
(4)为验证“84”消毒液的某些性质,实验小组设计图2实验方案。观察到试管1中溶液不褪色;试管2中溶液变蓝,短时间内无明显现象;试管3中溶液先变蓝,通入CO2后,溶液快速褪色。
①试管1的作用是
②由试管2、3的现象可得到的结论是
③若将试管3中通入的CO2换成盐酸也可达到相同的效果,且速度更快,但有可能产生Cl2而带来不良的实验后果,试用离子方程式解释产生Cl2的原因
(5)同学们观察到“84”消毒液的液体呈浅黄绿色,猜想其中可能溶有氯气。现设计实验证明“84”消毒液中溶有氯气,可供选择的实验仪器、药品:试管、苯、酒精、“84”消毒液。请你简述实验操作、现象及结论
您最近一年使用:0次
名校
6 . 某家用防疫品“84消毒液”的包装说明如下,回答下列问题:
(1)“84”消毒液可由 与
与 溶液反应制得,该反应的离子方程式为
溶液反应制得,该反应的离子方程式为___________ 。
(2)欲将“84消毒液”原液稀释配制成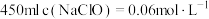 的溶液。
的溶液。
①配制过程中,需要用到的玻璃仪器有烧杯、玻璃棒、胶头滴管、量筒、______ 。
②配制时,需要取用______ mL“84消毒液”原液。
③下列操作会使溶液中 浓度偏高的是
浓度偏高的是______ 。
A.取用的“84消毒液”原液是久置的
B.定容操作时,俯视刻度线
C.量取“84消毒液”原液时,仰视读数
D.定容摇匀后,液面低于刻度线,再加水至刻度线
E.转移时没有洗涤烧杯和玻璃棒
(3)用次氯酸钠固体配置一定物质的量浓度溶液的消毒液,下列操作正确的是______ 。
A. B.
B. C.
C.
(4)利用如图装置探究84消毒液与洁厕灵(主要成分为盐酸)的反应,当注射器中的洁厕灵注入试管中时,装置内产生黄绿色气体,可观察到 试纸的现象是
试纸的现象是______ 。棉花团(蘸有溶液A)的作用是___________ 。

(5)资料查得:“84消毒液”与双氧水混合会反应产生一种常见的无色无味气体,且消毒能力大大降低,写出该反应的离子方程式___________ 。
| 【产品名称】84消毒液 【有效成分】  【规格】  【物质的量浓度】  注:①按一定比例稀释后使用 ②不得与酸性产品(如洁厕灵)同时使用 |
(1)“84”消毒液可由
 与
与 溶液反应制得,该反应的离子方程式为
溶液反应制得,该反应的离子方程式为(2)欲将“84消毒液”原液稀释配制成
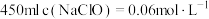 的溶液。
的溶液。①配制过程中,需要用到的玻璃仪器有烧杯、玻璃棒、胶头滴管、量筒、
②配制时,需要取用
③下列操作会使溶液中
 浓度偏高的是
浓度偏高的是A.取用的“84消毒液”原液是久置的
B.定容操作时,俯视刻度线
C.量取“84消毒液”原液时,仰视读数
D.定容摇匀后,液面低于刻度线,再加水至刻度线
E.转移时没有洗涤烧杯和玻璃棒
(3)用次氯酸钠固体配置一定物质的量浓度溶液的消毒液,下列操作正确的是
A.
 B.
B. C.
C.
(4)利用如图装置探究84消毒液与洁厕灵(主要成分为盐酸)的反应,当注射器中的洁厕灵注入试管中时,装置内产生黄绿色气体,可观察到
 试纸的现象是
试纸的现象是
(5)资料查得:“84消毒液”与双氧水混合会反应产生一种常见的无色无味气体,且消毒能力大大降低,写出该反应的离子方程式
您最近一年使用:0次
名校
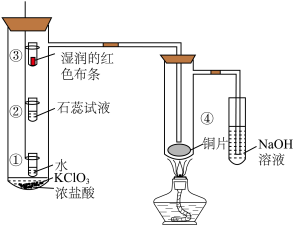
7 . 某化学实验小组利用下图所示装置制备 并进行性质验证,下列说法中正确的是
并进行性质验证,下列说法中正确的是
 并进行性质验证,下列说法中正确的是
并进行性质验证,下列说法中正确的是
A.①处小试管中溶液逐渐变成浅绿色说明 能溶于水 能溶于水 |
| B.②处石蕊试液先变红说明新制氯水具有酸性 |
C.③处湿润的红色布条褪色说明 具有漂白性 具有漂白性 |
D.④处出现棕黄色的烟说明 具有还原性 具有还原性 |
您最近一年使用:0次
2023-02-14更新
|
258次组卷
|
5卷引用:陕西省渭南市大荔县2022-2023学年高一上学期期末考试(鲁科版)化学试题
陕西省渭南市大荔县2022-2023学年高一上学期期末考试(鲁科版)化学试题陕西省渭南市大荔县2022-2023学年高一上学期期末考试(人教版)化学试题(已下线)第02讲 氯气的性质及实验室制法-【暑假自学课】2023年新高一化学暑假精品课(鲁科版2019必修第一册)山东省新泰市第一中学(实验部)2023-2024学年高一上学期第二次月考化学试题山东省青岛第三十九中学2023-2024学年高一上学期期中考试化学试卷
8 . 某小组为探究 的性质,做了如下实验。下列有关说法错误的是
的性质,做了如下实验。下列有关说法错误的是

 的性质,做了如下实验。下列有关说法错误的是
的性质,做了如下实验。下列有关说法错误的是
| A.装置A的作用是与装置C进行对比 |
| B.装置D中的现象为溶液先变红后褪色 |
C.装置E中的反应为 |
D.装置F中充入 后溶液颜色恢复为浅绿色,说明氧化性: 后溶液颜色恢复为浅绿色,说明氧化性: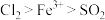 |
您最近一年使用:0次
9 . 化学来源于生活,也服务于生活。下列叙述错误的是
| A.氯气与烧碱溶液或石灰乳反应都能得到含氯消毒剂 |
| B.铁锅可用作炊具,主要利用了铁的导热性 |
| C.铝制餐具能用来蒸煮或长时间存放酸性或碱性食物 |
| D.漂白粉在空气中久置会变质 |
您最近一年使用:0次
10 . 海水中含有大量的卤族元素,具有十分巨大的开发利用潜力。
Ⅰ.向硫酸酸化的浓缩海水中通入 ,可获得含
,可获得含 的海水,
的海水,
(1)其反应的离子方程式为_______ ,由此可知氧化性:
_______  (填“>”或“<”)。
(填“>”或“<”)。
Ⅱ.氯是非常重要的非金属元素,如图是探究氯气性质和用途的实验装置。

(2)写出B中的化学反应方程式_______ 。
(3)该实验中设置装置C、D、E的主要目的是_______ ,与该实验目的直接相关的实验现象是_______ 。
(4)装置F可用于制漂白粉,漂白粉的有效成分是_______ (填化学式)。
(5)烧杯G的作用是_______ (用离子方程式表示)。
Ⅰ.向硫酸酸化的浓缩海水中通入
 ,可获得含
,可获得含 的海水,
的海水,(1)其反应的离子方程式为

 (填“>”或“<”)。
(填“>”或“<”)。Ⅱ.氯是非常重要的非金属元素,如图是探究氯气性质和用途的实验装置。

(2)写出B中的化学反应方程式
(3)该实验中设置装置C、D、E的主要目的是
(4)装置F可用于制漂白粉,漂白粉的有效成分是
(5)烧杯G的作用是
您最近一年使用:0次



