名校
解题方法
1 . 实验小组制备高铁酸钾(K2FeO4)并探究其性质。
资料:K2FeO4为紫色固体,微溶于KOH溶液;具有强氧化性,在酸性或中性溶液中快速产生O2,在碱性溶液中较稳定。
Ⅰ.制备K2FeO4(夹持装置略)
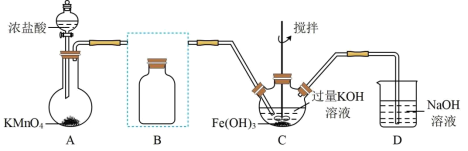
(1)写出A中产生氯气的离子方程式:_______
(2)在答题纸上将除杂装置B补充完整并标明所用试剂:_______
(3)在C中发生的2个反应的离子方程式:_______ ;_______
Ⅱ.探究K2FeO4的性质:取C中紫色溶液,加入稀硫酸,产生气体和溶液a.为证明是否K2FeO4氧化了Cl-而产生Cl2,设计以下方案:
(4)由方案Ⅰ中溶液变红可知a中含有_______ 离子,根据方案Ⅱ得出:氧化性Cl2_______  (填“>”或“<”)
(填“>”或“<”)
(5)使用时经常通过测定高铁酸钾的纯度来判断其是否变质。K2FeO4在硫酸溶液中反应如下:
_______FeO +_______H+=_______O2↑+_______Fe3++ _______
+_______H+=_______O2↑+_______Fe3++ _______
①完成并配平上述离子方程式_______ 。
②现取C中洗涤并干燥后样品的质量10 g,加入稀硫酸,收集到0.672 L气体(标准状况)。则样品中高铁酸钾的质量分数为_______ 。(计算结果保留到0.1%)
资料:K2FeO4为紫色固体,微溶于KOH溶液;具有强氧化性,在酸性或中性溶液中快速产生O2,在碱性溶液中较稳定。
Ⅰ.制备K2FeO4(夹持装置略)

(1)写出A中产生氯气的离子方程式:
(2)在答题纸上将除杂装置B补充完整并标明所用试剂:
(3)在C中发生的2个反应的离子方程式:
Ⅱ.探究K2FeO4的性质:取C中紫色溶液,加入稀硫酸,产生气体和溶液a.为证明是否K2FeO4氧化了Cl-而产生Cl2,设计以下方案:
| 方案Ⅰ | 取少量a,滴加KSCN溶液至过量,溶液呈红色 |
| 方案Ⅱ | 用KOH溶液充分洗涤C中所得固体,再用KOH溶液将K2FeO4溶解,得到紫色溶液b,取少量b,滴加盐酸,有Cl2产生 |
 (填“>”或“<”)
(填“>”或“<”)(5)使用时经常通过测定高铁酸钾的纯度来判断其是否变质。K2FeO4在硫酸溶液中反应如下:
_______FeO
 +_______H+=_______O2↑+_______Fe3++ _______
+_______H+=_______O2↑+_______Fe3++ _______①完成并配平上述离子方程式
②现取C中洗涤并干燥后样品的质量10 g,加入稀硫酸,收集到0.672 L气体(标准状况)。则样品中高铁酸钾的质量分数为
您最近一年使用:0次
2 . 利用下图,可以从不同角度研究含氯物质的性质及其转化关系,图中甲~辛均含氯元素。回答下列问题:

(1)丙的化学式为_______ ;从组成和性质上分析,丁属于_______ (填“酸性”或“碱性”)氧化物。
(2)图中甲、乙、丁、戊中,属于电解质的是__________ (填化学式);根据氯元素的化合价判断,乙物质__________ 。
a 只有氧化性 b 既有氧化性又有还原性
c 只有还原性 d 既能做氧化剂也能做还原剂
(3)电解甲溶液制备己的化学反应为:甲+ H2O→己+H2↑,反应中甲与H2O的物质的量之比是______ 。
(4)庚是漂白粉的有效成分,用乙制取庚的化学反应方程式为_________ 。
(5)辛在MnO2催化下受热分解可用于制备一种常见气体,这种气体的化学式是____ 。

(1)丙的化学式为
(2)图中甲、乙、丁、戊中,属于电解质的是
a 只有氧化性 b 既有氧化性又有还原性
c 只有还原性 d 既能做氧化剂也能做还原剂
(3)电解甲溶液制备己的化学反应为:甲+ H2O→己+H2↑,反应中甲与H2O的物质的量之比是
(4)庚是漂白粉的有效成分,用乙制取庚的化学反应方程式为
(5)辛在MnO2催化下受热分解可用于制备一种常见气体,这种气体的化学式是
您最近一年使用:0次
2020-03-15更新
|
265次组卷
|
4卷引用:山东省淄博市2019-2020学年高一上学期期末质量检测化学试题
山东省淄博市2019-2020学年高一上学期期末质量检测化学试题(已下线)【浙江新东方】【2020】【高一上】【期中】【HD-LP409】【化学】(已下线)【浙江新东方】72云南省大理州祥云县2019-2020学年高一下学期期末统测化学试题
解题方法
3 . 某小组同学探究不同条件下氯气与二价锰化合物的反应
资料:i. 在一定条件下被
在一定条件下被 或
或 氧化成
氧化成 (棕黑色)、
(棕黑色)、 (绿色)、
(绿色)、 (紫色)。
(紫色)。
ii.浓碱条件下, 可被
可被 还原为
还原为 。
。
iii. 的氧化性与溶液的酸碱性无关,NaClO的氧化性随碱性增强而减弱。
的氧化性与溶液的酸碱性无关,NaClO的氧化性随碱性增强而减弱。
实验装置如图(夹持装置略)
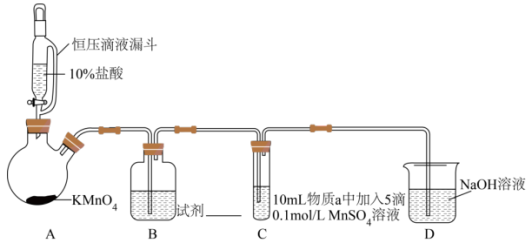
(1)通入 前,II、III中沉淀由白色变为黑色的化学方程式为
前,II、III中沉淀由白色变为黑色的化学方程式为_______ 。
(2)对比实验I、II通入 后的实验现象,对于二价锰化合物还原性的认识是
后的实验现象,对于二价锰化合物还原性的认识是_______ 。
(3)根据资料ⅱ,III中应得到绿色溶液,实验中得到紫色溶液,分析现象与资料不符的原因:
原因一:可能是通入 发生反应
发生反应 ,导致溶液的碱性减弱。但通过实验测定溶液的碱性变化很小。
,导致溶液的碱性减弱。但通过实验测定溶液的碱性变化很小。
原因二:可能是氧化剂过量,氧化剂将 氧化为
氧化为 。
。
①取III中放置后的1mL悬浊液,加入4mL40%NaOH溶液,溶液紫色迅速变为绿色,且绿色缓慢加深。溶液紫色变为绿色的离子方程式为_______ ,溶液绿色缓慢加深,原因是 被
被_______ (填“化学式”)氧化,可证明III的悬浊液中氧化剂过量;
②取II中放置后的1mL悬浊液,加入4mL水,溶液紫色缓慢加深,发生的反应是_______ 。
③从反应速率的角度,分析实验III未得到绿色溶液的可能原因_______ 。
资料:i.
 在一定条件下被
在一定条件下被 或
或 氧化成
氧化成 (棕黑色)、
(棕黑色)、 (绿色)、
(绿色)、 (紫色)。
(紫色)。ii.浓碱条件下,
 可被
可被 还原为
还原为 。
。iii.
 的氧化性与溶液的酸碱性无关,NaClO的氧化性随碱性增强而减弱。
的氧化性与溶液的酸碱性无关,NaClO的氧化性随碱性增强而减弱。实验装置如图(夹持装置略)

| 序号 | 物质a | C中实验现象 | |
通入 前 前 | 通入 后 后 | ||
| I | 水 | 得到无色溶液 | 产生棕黑色沉淀,且放置后不发生变化 |
| II | 5%NaOH溶液 | 产生白色沉淀,在空气中缓慢变成棕黑色沉淀 | 棕黑色沉淀增多,放置后溶液变为紫色,仍有沉淀 |
| III | 40%NaOH溶液 | 产生白色沉淀,在空气中缓慢变成棕黑色沉淀 | 棕黑色沉淀增多,放置后溶液变为紫色,仍有沉淀 |
 前,II、III中沉淀由白色变为黑色的化学方程式为
前,II、III中沉淀由白色变为黑色的化学方程式为(2)对比实验I、II通入
 后的实验现象,对于二价锰化合物还原性的认识是
后的实验现象,对于二价锰化合物还原性的认识是(3)根据资料ⅱ,III中应得到绿色溶液,实验中得到紫色溶液,分析现象与资料不符的原因:
原因一:可能是通入
 发生反应
发生反应 ,导致溶液的碱性减弱。但通过实验测定溶液的碱性变化很小。
,导致溶液的碱性减弱。但通过实验测定溶液的碱性变化很小。原因二:可能是氧化剂过量,氧化剂将
 氧化为
氧化为 。
。①取III中放置后的1mL悬浊液,加入4mL40%NaOH溶液,溶液紫色迅速变为绿色,且绿色缓慢加深。溶液紫色变为绿色的离子方程式为
 被
被②取II中放置后的1mL悬浊液,加入4mL水,溶液紫色缓慢加深,发生的反应是
③从反应速率的角度,分析实验III未得到绿色溶液的可能原因
您最近一年使用:0次
名校
解题方法
4 . Ⅰ.某实验小组为探究ClO-、I2、SO42-在酸性条件下的氧化性强弱,设计实验如下:
实验①:在淀粉-碘化钾溶液中加入少量次氯酸钠溶液,并加入少量的稀硫酸,溶液立即变蓝;
实验②:向实验①的溶液中加入6mL0.5mol·L-1的亚硫酸钠溶液,蓝色恰好完全褪去。
(1)写出实验①中发生反应的离子方程式:___ 。
(2)实验②的化学反应中转移电子的物质的量是__ 。
(3)以上实验说明,在酸性条件下ClO-、I2、SO42-的氧化性由弱到强的顺序是__ 。
Ⅱ.(4)Cl2、H2O2、ClO2(还原产物为Cl-)、O3(1molO3转化为1molO2和1molH2O)等物质常被用作消毒剂。等物质的量的上述物质消毒效率最高的是___ (填序号)。
A.Cl2 B.H2O2 C.ClO2 D.O3
(5)“84”消毒液(主要成分是NaClO)和洁厕剂(主要成分是浓盐酸)不能混用,原因是___ (用离子方程式表示)。
实验①:在淀粉-碘化钾溶液中加入少量次氯酸钠溶液,并加入少量的稀硫酸,溶液立即变蓝;
实验②:向实验①的溶液中加入6mL0.5mol·L-1的亚硫酸钠溶液,蓝色恰好完全褪去。
(1)写出实验①中发生反应的离子方程式:
(2)实验②的化学反应中转移电子的物质的量是
(3)以上实验说明,在酸性条件下ClO-、I2、SO42-的氧化性由弱到强的顺序是
Ⅱ.(4)Cl2、H2O2、ClO2(还原产物为Cl-)、O3(1molO3转化为1molO2和1molH2O)等物质常被用作消毒剂。等物质的量的上述物质消毒效率最高的是
A.Cl2 B.H2O2 C.ClO2 D.O3
(5)“84”消毒液(主要成分是NaClO)和洁厕剂(主要成分是浓盐酸)不能混用,原因是
您最近一年使用:0次
2019-12-10更新
|
143次组卷
|
7卷引用:山东省肥城市泰西中学2019-2020学年高三上学期第一次月考化学试题
山东省肥城市泰西中学2019-2020学年高三上学期第一次月考化学试题2018版化学(苏教版)高考总复习课时跟踪训练:氧化还原反应基础重庆市南开中学2019届高三上学期第一次月考化学试题(已下线)2019高考热点题型和提分秘籍 第二章 化学物质及其变化 第3讲 氧化还原反应 (题型专练)吉林省东辽五中2020届高三上学期9月月考化学试题江西省南昌市新建县第一中学2020届高三上学期第一次月考化学试题吉林省大安市第一中学校2021届高三上学期第二次月考化学试题
5 . 次氯酸盐具有强氧化性。在碱性条件下,利用 氧化
氧化 生成高铁酸钾
生成高铁酸钾 的工艺流程如下:
的工艺流程如下:
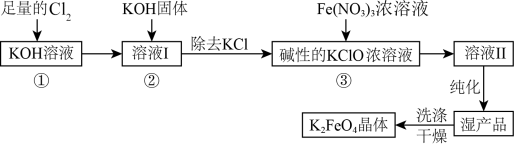
已知:①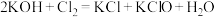 (条件:温度较低);
(条件:温度较低);
②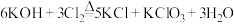 (条件:温度较高)。
(条件:温度较高)。
回答下列问题:
(1)反应①应在
(2)在溶液I中加入
 固体的目的是
固体的目的是(3)从溶液Ⅱ中分离出
 后,还会有副产品
后,还会有副产品 、
、 ,则反应③中发生的离子反应方程式为
,则反应③中发生的离子反应方程式为(4)
 可作饮用水处理剂,该反应的离子方程式:
可作饮用水处理剂,该反应的离子方程式: ,
, 处理水中悬浮颗粒物的原理是
处理水中悬浮颗粒物的原理是(5)目前,人们针对
 的稳定性进行了大量的探索,并取得了一定的进展。下列物质中有可能提高
的稳定性进行了大量的探索,并取得了一定的进展。下列物质中有可能提高 水溶液稳定性的物质是___________(填字母)。
水溶液稳定性的物质是___________(填字母)。A. | B. | C. | D. |
您最近一年使用:0次
2023-09-21更新
|
349次组卷
|
3卷引用:山东省滨州市沾化区实验高级中学2023-2024学年高三上学期第二次月考化学试题
解题方法
6 . 氯的含氧酸盐具有较强的氧化性,能够杀菌消毒,在预防新冠疫情中起到重要作用。某化学兴趣小组用氯气和相应的碱溶液反应制取NaClO和 ,制备装置如图所示(部分加持仪器略去),并研究
,制备装置如图所示(部分加持仪器略去),并研究 的氧化性。已知:氯气与碱反应,温度较高时生成
的氧化性。已知:氯气与碱反应,温度较高时生成 ,温度较低时生成
,温度较低时生成 。
。

(1)盛装浓盐酸的仪器名称是_______ 。
(2)装置A烧瓶中反应的化学方程式为_______ 。
(3)装置C中 与试剂a反应的离子方程式为
与试剂a反应的离子方程式为_______ 。
(4)如果缺少装置B,对制取NaClO和 的影响是
的影响是_______ 。
(5)E中可选用试剂有_______ (填标号)。
A.饱和 溶液 B.浓
溶液 B.浓 C.饱和NaCl溶液 D.NaOH溶液
C.饱和NaCl溶液 D.NaOH溶液
(6)该小组在探究 氧化性时,发现
氧化性时,发现 与
与 的反应速率先增大后减小,反应为
的反应速率先增大后减小,反应为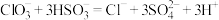 。小组分析认为,反应生成的离子可能对反应速率产生影响。为了探究
。小组分析认为,反应生成的离子可能对反应速率产生影响。为了探究 对化学反应速率的影响,设计如下实验:
对化学反应速率的影响,设计如下实验:
该实验_______ (填“能”或“不能”)达到实验目的,理由是_______ 。
 ,制备装置如图所示(部分加持仪器略去),并研究
,制备装置如图所示(部分加持仪器略去),并研究 的氧化性。已知:氯气与碱反应,温度较高时生成
的氧化性。已知:氯气与碱反应,温度较高时生成 ,温度较低时生成
,温度较低时生成 。
。
(1)盛装浓盐酸的仪器名称是
(2)装置A烧瓶中反应的化学方程式为
(3)装置C中
 与试剂a反应的离子方程式为
与试剂a反应的离子方程式为(4)如果缺少装置B,对制取NaClO和
 的影响是
的影响是(5)E中可选用试剂有
A.饱和
 溶液 B.浓
溶液 B.浓 C.饱和NaCl溶液 D.NaOH溶液
C.饱和NaCl溶液 D.NaOH溶液(6)该小组在探究
 氧化性时,发现
氧化性时,发现 与
与 的反应速率先增大后减小,反应为
的反应速率先增大后减小,反应为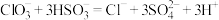 。小组分析认为,反应生成的离子可能对反应速率产生影响。为了探究
。小组分析认为,反应生成的离子可能对反应速率产生影响。为了探究 对化学反应速率的影响,设计如下实验:
对化学反应速率的影响,设计如下实验:| 实验序号 | 温度 |  | 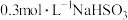 |  盐酸 盐酸 |  |
| ① | 25℃ | 10mL | 10mL | 0mL | 1mL |
| ② | 25℃ | 10mL | 10mL | 1mL | 0mL |
您最近一年使用:0次
2021-06-17更新
|
401次组卷
|
2卷引用:山东省临朐县实验中学2020-2021学年高一7月月考化学试题
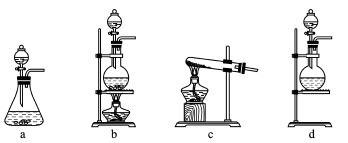
7 . 某研究性学习小组查阅资料得知,漂白粉与硫酸溶液反应可制取氯气,化学方程式为Ca(ClO)2+CaCl2+2H2SO4 2CaSO4+2Cl2↑+2H2O,他们设计如图实验装置制取氯气并验证其性质。请回答下列问题:
2CaSO4+2Cl2↑+2H2O,他们设计如图实验装置制取氯气并验证其性质。请回答下列问题:

(1)该实验中A部分的装置是_____ (填字母)。
(2)装置B中的现象是_____ 。
(3)请写出装置C中发生反应的离子方程式:_____ 。请帮助他们设计一个实验,证明洗气瓶C中的亚硫酸钠已被氧化(简述实验步骤):______ 。
(4)装置E的作用是______ 。
(5)制取Cl2的方法有多种,若A部分的装置是a,请再写出一种制备方法:______ (用化学方程式表示)。
 2CaSO4+2Cl2↑+2H2O,他们设计如图实验装置制取氯气并验证其性质。请回答下列问题:
2CaSO4+2Cl2↑+2H2O,他们设计如图实验装置制取氯气并验证其性质。请回答下列问题:
(1)该实验中A部分的装置是

(2)装置B中的现象是
(3)请写出装置C中发生反应的离子方程式:
(4)装置E的作用是
(5)制取Cl2的方法有多种,若A部分的装置是a,请再写出一种制备方法:
您最近一年使用:0次
解题方法
8 . 某化学兴趣小组设计了如图装置制取Cl2进行相关性质实验,并模拟工业生产无水氯化铁的过程。
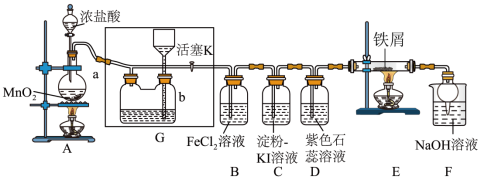
资料:①工业上向500~600℃的铁屑中通入氯气生产无水氯化铁。②无水氯化铁有强烈的吸水性,能吸收空气中的水分而潮解变质。装置G中的液体是饱和氯化钠溶液,用于储存反应后多余的氯气。
根据各小题的要求,填写下列空白:
(1)装置A中装浓盐酸的玻璃仪器名称为______ ,A中发生反应的离子方程式为______ 。
(2)实验开始时,先打开分液漏斗旋塞和活塞K,点燃A处酒精灯,让氯气充满整个装置,再点燃E处酒精灯。回答下列问题:
①装置B中发生反应的化学方程式为______ 。
②装置C和D中看到的实验现象分别是______ 、______ 。
(3)若要得到较纯净的无水氯化铁,上述装置的改进措施是:______ 。

资料:①工业上向500~600℃的铁屑中通入氯气生产无水氯化铁。②无水氯化铁有强烈的吸水性,能吸收空气中的水分而潮解变质。装置G中的液体是饱和氯化钠溶液,用于储存反应后多余的氯气。
根据各小题的要求,填写下列空白:
(1)装置A中装浓盐酸的玻璃仪器名称为
(2)实验开始时,先打开分液漏斗旋塞和活塞K,点燃A处酒精灯,让氯气充满整个装置,再点燃E处酒精灯。回答下列问题:
①装置B中发生反应的化学方程式为
②装置C和D中看到的实验现象分别是
(3)若要得到较纯净的无水氯化铁,上述装置的改进措施是:
您最近一年使用:0次
9 . Ⅰ.在一定量的石灰乳中通入一定量的氯气,二者恰好完全反应(发生的反映均为放热反应)。生成物中含有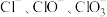 三种含氯元素的离子,其中
三种含氯元素的离子,其中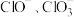 两种离子的物质的量
两种离子的物质的量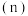 与反应时间(
与反应时间( )的曲线如图所示。
)的曲线如图所示。

(1) 时刻之前发生的反应是:
时刻之前发生的反应是:_______ 。
(2) 时,
时, 与
与 发生反应的总化学方程式为
发生反应的总化学方程式为 ,该反应中氯气的作用是
,该反应中氯气的作用是_______ ;则该石灰乳中含有 的物质的量是
的物质的量是_______ mol。
(3)据分析,生成 的反应是由温度升高引起的,通入
的反应是由温度升高引起的,通入 的速度不同,
的速度不同, 和
和 的比例也不同。若在原石灰乳中通入氯气的速度加快,则反应后
的比例也不同。若在原石灰乳中通入氯气的速度加快,则反应后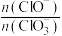
_______ 2(填“>”“<”或“=”);氯酸钙 为有毒化学品,其粉尘对呼吸道、眼及皮肤有刺激性,吸入氯酸钙粉尘,会因积累在体内而引起中毒。为了防止使用漂白粉时出现意外,制备漂白粉时可以采取的措施
为有毒化学品,其粉尘对呼吸道、眼及皮肤有刺激性,吸入氯酸钙粉尘,会因积累在体内而引起中毒。为了防止使用漂白粉时出现意外,制备漂白粉时可以采取的措施_______ (写一条即可)。
(4)请配平一下化学方程式: 。若反应过程中转移
。若反应过程中转移 ,则生成标准状况下
,则生成标准状况下 的体积为
的体积为_______ L。
Ⅱ.有下列三个在溶液中发生的氧化还原反应:
① ;
;
②
③
请根据上述反应分析推断后回答下列问题:
(5) 的氧化性由强到弱依次是
的氧化性由强到弱依次是_______ 。
(6)在酸性溶液中存在大量的 ,则
,则 中能与
中能与 大量共存的离子是
大量共存的离子是_______ 。
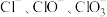 三种含氯元素的离子,其中
三种含氯元素的离子,其中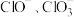 两种离子的物质的量
两种离子的物质的量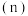 与反应时间(
与反应时间( )的曲线如图所示。
)的曲线如图所示。
(1)
 时刻之前发生的反应是:
时刻之前发生的反应是:(2)
 时,
时, 与
与 发生反应的总化学方程式为
发生反应的总化学方程式为 ,该反应中氯气的作用是
,该反应中氯气的作用是 的物质的量是
的物质的量是(3)据分析,生成
 的反应是由温度升高引起的,通入
的反应是由温度升高引起的,通入 的速度不同,
的速度不同, 和
和 的比例也不同。若在原石灰乳中通入氯气的速度加快,则反应后
的比例也不同。若在原石灰乳中通入氯气的速度加快,则反应后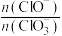
 为有毒化学品,其粉尘对呼吸道、眼及皮肤有刺激性,吸入氯酸钙粉尘,会因积累在体内而引起中毒。为了防止使用漂白粉时出现意外,制备漂白粉时可以采取的措施
为有毒化学品,其粉尘对呼吸道、眼及皮肤有刺激性,吸入氯酸钙粉尘,会因积累在体内而引起中毒。为了防止使用漂白粉时出现意外,制备漂白粉时可以采取的措施(4)请配平一下化学方程式:
 。若反应过程中转移
。若反应过程中转移 ,则生成标准状况下
,则生成标准状况下 的体积为
的体积为Ⅱ.有下列三个在溶液中发生的氧化还原反应:
①
 ;
;②

③

请根据上述反应分析推断后回答下列问题:
(5)
 的氧化性由强到弱依次是
的氧化性由强到弱依次是(6)在酸性溶液中存在大量的
 ,则
,则 中能与
中能与 大量共存的离子是
大量共存的离子是
您最近一年使用:0次
名校
解题方法
10 . 氯的含氧酸盐具有较强的氧化性,能够杀菌消毒,在预防新冠疫情中起到重要作用。某化学兴趣小组用氯气和相应的碱溶液反应制取NaClO和KClO3,制备装置如图所示(部分加持仪器略去)。已知:
①MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O;
MnCl2+Cl2↑+2H2O;
②氯气与碱反应,温度较高时生成ClO ,温度较低时生成ClO-。
,温度较低时生成ClO-。
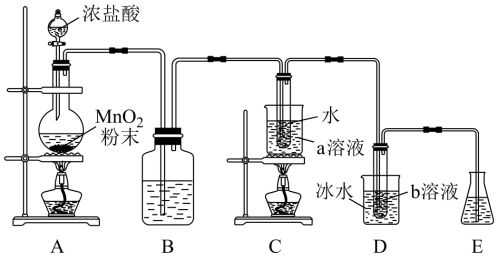
(1)在实验开始之前,应当进行的操作是_______ 。
(2)盛装浓盐酸的仪器名称是_______ 。
(3)装置B中的试剂为_______ 。
(4)a溶液是_______ ,原因是_______ 。
(5)如果缺少装置B,对制取NaClO和KClO3的影响是_______ 。
(6)装置E的作用是_______ ,写出所发生反应的化学方程式:_______ 。
①MnO2+4HCl(浓)
 MnCl2+Cl2↑+2H2O;
MnCl2+Cl2↑+2H2O;②氯气与碱反应,温度较高时生成ClO
 ,温度较低时生成ClO-。
,温度较低时生成ClO-。
(1)在实验开始之前,应当进行的操作是
(2)盛装浓盐酸的仪器名称是
(3)装置B中的试剂为
(4)a溶液是
(5)如果缺少装置B,对制取NaClO和KClO3的影响是
(6)装置E的作用是
您最近一年使用:0次



