名校
1 . 分类是认识和研究物质及其变化的一种常用的科学方法。依据物质类别和元素价态可以对物质的性质进行解释和预测。
(1)阅读资料,回答下列相关问题。
①以上画横线的物质中:属于电解质的有_______ 种;其中属于酸式盐的物质的电离方程式_______ 。
②Cl2与NaOH溶液反应的离子方程式是_______ 。
(2)“84”消毒液不能与洁厕灵(含盐酸)混用,混用会发生如下反应: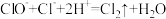 。
。
①该反应中起氧化作用的微粒是_______ 。
②若反应中生成了0.01molCl2,转移电子的物质的量为_______ mol。
(3)2016年巴西奥运会期间,由于工作人员将“84”消毒液与双氧水两种消毒剂混用,导致游泳池藻类快速生长,池水变绿。一种可能的原因是NaClO将H2O2氧化产生的O2促进藻类快速生长。该反应说明氧化性:NaClO_______ H2O2(填“>”或“<”)。
(1)阅读资料,回答下列相关问题。
| 资料:人们常用“84”消毒液进行消毒。“84”消毒液的名称源于北京某医院在1984年研制成功的一种高效含氯消毒剂。“84”消毒液呈无色或淡黄色,可由Cl2和NaOH溶液反应制得,其主要成分为NaClO、NaCl。发挥漂白作用时NaClO与空气中的CO2、H2O反应生成NaHCO3和HClO。 |
②Cl2与NaOH溶液反应的离子方程式是
(2)“84”消毒液不能与洁厕灵(含盐酸)混用,混用会发生如下反应:
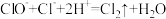 。
。①该反应中起氧化作用的微粒是
②若反应中生成了0.01molCl2,转移电子的物质的量为
(3)2016年巴西奥运会期间,由于工作人员将“84”消毒液与双氧水两种消毒剂混用,导致游泳池藻类快速生长,池水变绿。一种可能的原因是NaClO将H2O2氧化产生的O2促进藻类快速生长。该反应说明氧化性:NaClO
您最近一年使用:0次
2 . 肼( ,无色液体)是一种用途广泛的化工原料。实验室中先制备次氯酸钠,再用次氯酸钠溶液和氨反应制备肼并验证肼的性质。实验装置如图所示。
,无色液体)是一种用途广泛的化工原料。实验室中先制备次氯酸钠,再用次氯酸钠溶液和氨反应制备肼并验证肼的性质。实验装置如图所示。

已知: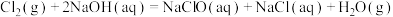
 。当温度超过40℃时,
。当温度超过40℃时, 与
与 溶液反应生成
溶液反应生成 。
。
回答下列问题:
(1)装置B的作用是______________ 。
(2)为控制D装置中的反应温度,除用冷水浴外,还需采取的实验操作是_________ 。
(3)当三颈烧瓶中出现黄绿色气体时立即关闭分液漏斗活塞、移去酒精灯、关闭 。此时装置C的作用是
。此时装置C的作用是_______________ 。
(4)将D装置水槽中的冷水换为热水,把三颈烧瓶中黄绿色气体赶走后,打开 ,通入
,通入 ,使其与
,使其与 溶液反应制取肼。理论上通入三颈烧瓶的
溶液反应制取肼。理论上通入三颈烧瓶的 和
和 的最佳物质的量之比为
的最佳物质的量之比为______ 。
(5)请从提供的下列试剂中选择合适试剂,设计合理的实验方案验证肼的还原性(说明操作、现象和结论)。____________ 。
①淀粉- 溶液 ②稀硫酸(酚酞) ③
溶液 ②稀硫酸(酚酞) ③ ④
④
 ,无色液体)是一种用途广泛的化工原料。实验室中先制备次氯酸钠,再用次氯酸钠溶液和氨反应制备肼并验证肼的性质。实验装置如图所示。
,无色液体)是一种用途广泛的化工原料。实验室中先制备次氯酸钠,再用次氯酸钠溶液和氨反应制备肼并验证肼的性质。实验装置如图所示。
已知:
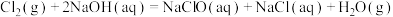
 。当温度超过40℃时,
。当温度超过40℃时, 与
与 溶液反应生成
溶液反应生成 。
。回答下列问题:
(1)装置B的作用是
(2)为控制D装置中的反应温度,除用冷水浴外,还需采取的实验操作是
(3)当三颈烧瓶中出现黄绿色气体时立即关闭分液漏斗活塞、移去酒精灯、关闭
 。此时装置C的作用是
。此时装置C的作用是(4)将D装置水槽中的冷水换为热水,把三颈烧瓶中黄绿色气体赶走后,打开
 ,通入
,通入 ,使其与
,使其与 溶液反应制取肼。理论上通入三颈烧瓶的
溶液反应制取肼。理论上通入三颈烧瓶的 和
和 的最佳物质的量之比为
的最佳物质的量之比为(5)请从提供的下列试剂中选择合适试剂,设计合理的实验方案验证肼的还原性(说明操作、现象和结论)。
①淀粉-
 溶液 ②稀硫酸(酚酞) ③
溶液 ②稀硫酸(酚酞) ③ ④
④
您最近一年使用:0次
解题方法
3 . 氯及其化合物在生产生活中有重要的作用。已知某品牌的84消毒液和洁厕灵的部分标签如图所示:
回答下列问题:
(1)工业上通常将氯气通入氢氧化钠溶液中制备84消毒液,请写出该反应的离子方程式___________ 。
(2)各类杀菌消毒剂使用时,必须严格按照使用说明。
①巴西奥运会期间,由于工作人员将“84”消毒液与双氧水两种消毒剂混用,导致游泳池藻类快速生长,池水变绿。一种可能的原因是 与
与 反应产生
反应产生 促进藻类快速生长。该反应说明氧化性:
促进藻类快速生长。该反应说明氧化性:
___________  (填“>”或“<”)。当有0.1
(填“>”或“<”)。当有0.1
 生成时,反应中转移电子为
生成时,反应中转移电子为___________  。
。
②王女士在清洁马桶时,在倒入上述洁厕灵后将上述84消毒液也倒入其中,随后突然晕倒,原因是该过程产生了有毒的氯气,该过程发生反应的离子方程式为___________ 。
| ××牌洁厕灵 规格:1L 有效成分:盐酸,表面活性剂,香精 | ××牌84消毒液 规格:500  有效成分:  (“有效氯”含量:5.5%~6.5%) |
回答下列问题:
(1)工业上通常将氯气通入氢氧化钠溶液中制备84消毒液,请写出该反应的离子方程式
(2)各类杀菌消毒剂使用时,必须严格按照使用说明。
①巴西奥运会期间,由于工作人员将“84”消毒液与双氧水两种消毒剂混用,导致游泳池藻类快速生长,池水变绿。一种可能的原因是
 与
与 反应产生
反应产生 促进藻类快速生长。该反应说明氧化性:
促进藻类快速生长。该反应说明氧化性:
 (填“>”或“<”)。当有0.1
(填“>”或“<”)。当有0.1
 生成时,反应中转移电子为
生成时,反应中转移电子为 。
。②王女士在清洁马桶时,在倒入上述洁厕灵后将上述84消毒液也倒入其中,随后突然晕倒,原因是该过程产生了有毒的氯气,该过程发生反应的离子方程式为
您最近一年使用:0次
名校
4 . Ⅰ.在一定量的石灰乳中通入一定量的氯气,二者恰好完全反应(发生的反应均为放热反应)。生成物中含有Cl-、ClO-、ClO 三种含氯元素的离子,其中ClO-、ClO
三种含氯元素的离子,其中ClO-、ClO 两种离子的物质的量(n)与反应时间(t)的曲线如图所示。
两种离子的物质的量(n)与反应时间(t)的曲线如图所示。
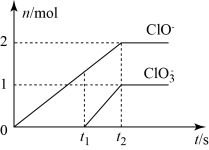
(1)t1时刻之前发生的反应是:___________
(2)t2时,Ca(OH)2与Cl2发生反应的总化学方程式为10Ca(OH)2+10Cl2=2Ca(ClO)2+Ca(ClO3)2+7CaCl2+10H2O,则该石灰乳中含有Ca(OH)2的物质的量是___________ mol。
(3)据分析,生成Ca(ClO3)2的反应是由温度升高引起的,通入Cl2的速度不同,ClO-和ClO 的比例也不同。若在原石灰乳中通入氯气的速度加快,则反应后
的比例也不同。若在原石灰乳中通入氯气的速度加快,则反应后
___________ 2(填“>”、“<”或“=”);氯酸钙(Ca(ClO3)2)为有毒化学品,其粉尘对呼吸道、眼及皮肤有刺激性,吸入氯酸钙粉尘,会因积累在体内而引起中毒。为了防止使用漂白粉时出现意外,制备漂白粉时可以采取的措施___________ (写一条即可)。
(4)请配平化学方程式:KClO3+HCl--KCl+Cl2↑+H2O___________ 。若反应过程中转移2mol e-,则生成标准状况下Cl2的体积为___________ L。
Ⅱ.有下列三个在溶液中发生的氧化还原反应:
①3FeCl3+2KI=2FeCl2+2KCl+I2;
②2FeCl2+Cl2=2FeCl3;
③K2Cr2O7+14HCl=2KCl+2CrCl3+7H2O+3Cl2↑
请根据上述反应分析推断后回答下列问题:
(5)FeCl3、I2、Cl2、K2Cr2O7的氧化性由强到弱依次是___________ 。
(6)在酸性溶液中存在大量的I-,则Cr2O 、Fe3+、Fe2+、Cl-中能与I-大量共存的离子是
、Fe3+、Fe2+、Cl-中能与I-大量共存的离子是___________ 。
 三种含氯元素的离子,其中ClO-、ClO
三种含氯元素的离子,其中ClO-、ClO 两种离子的物质的量(n)与反应时间(t)的曲线如图所示。
两种离子的物质的量(n)与反应时间(t)的曲线如图所示。
(1)t1时刻之前发生的反应是:
(2)t2时,Ca(OH)2与Cl2发生反应的总化学方程式为10Ca(OH)2+10Cl2=2Ca(ClO)2+Ca(ClO3)2+7CaCl2+10H2O,则该石灰乳中含有Ca(OH)2的物质的量是
(3)据分析,生成Ca(ClO3)2的反应是由温度升高引起的,通入Cl2的速度不同,ClO-和ClO
 的比例也不同。若在原石灰乳中通入氯气的速度加快,则反应后
的比例也不同。若在原石灰乳中通入氯气的速度加快,则反应后
(4)请配平化学方程式:KClO3+HCl--KCl+Cl2↑+H2O
Ⅱ.有下列三个在溶液中发生的氧化还原反应:
①3FeCl3+2KI=2FeCl2+2KCl+I2;
②2FeCl2+Cl2=2FeCl3;
③K2Cr2O7+14HCl=2KCl+2CrCl3+7H2O+3Cl2↑
请根据上述反应分析推断后回答下列问题:
(5)FeCl3、I2、Cl2、K2Cr2O7的氧化性由强到弱依次是
(6)在酸性溶液中存在大量的I-,则Cr2O
 、Fe3+、Fe2+、Cl-中能与I-大量共存的离子是
、Fe3+、Fe2+、Cl-中能与I-大量共存的离子是
您最近一年使用:0次
5 . Ⅰ、实 验室可以用KMnO4固体和浓盐酸反应制取少量Cl2,反应的化学方程式为:2KMnO4+16HCl(浓)═2KCl+2MnCl2+5Cl2↑+8H2O回答下列问题:
验室可以用KMnO4固体和浓盐酸反应制取少量Cl2,反应的化学方程式为:2KMnO4+16HCl(浓)═2KCl+2MnCl2+5Cl2↑+8H2O回答下列问题:
(1)该反应中被氧化的元素是__________ .
(2)氧化性:KMnO4__________ Cl2(填“>”、“<”或“= ”)
”)
(3)该反应中氧化 剂和氧化产物的物质的量之比为
剂和氧化产物的物质的量之比为__________ .
(4)用双线桥法表示该反应中电子转移的方向和数目:_________
2KMnO4+16HCl(浓)═2KCl+2MnCl2+5Cl2↑+8H2O
(5)每生成标准状况下2.24L Cl2,反应中转移电子的物质的量为__________ .
Ⅱ、实验室常用以下方法制取氯气:MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O请你根据所学知识回答下列问题:
MnCl2+Cl2↑+2H2O请你根据所学知识回答下列问题:
(1)把氯气通入紫色石蕊试液中,可以观察到的现象是:________________ ,请你解释其中的原因 __________________________________________________
(2)为保证实验安全,常用NaOH溶液吸收多余的氯气。写出反应的化学方程式__________________________________ ;
 验室可以用KMnO4固体和浓盐酸反应制取少量Cl2,反应的化学方程式为:2KMnO4+16HCl(浓)═2KCl+2MnCl2+5Cl2↑+8H2O回答下列问题:
验室可以用KMnO4固体和浓盐酸反应制取少量Cl2,反应的化学方程式为:2KMnO4+16HCl(浓)═2KCl+2MnCl2+5Cl2↑+8H2O回答下列问题:(1)该反应中被氧化的元素是
(2)氧化性:KMnO4
 ”)
”)(3)该反应中氧化
 剂和氧化产物的物质的量之比为
剂和氧化产物的物质的量之比为(4)用双线桥法表示该反应中电子转移的方向和数目:
2KMnO4+16HCl(浓)═2KCl+2MnCl2+5Cl2↑+8H2O
(5)每生成标准状况下2.24L Cl2,反应中转移电子的物质的量为
Ⅱ、实验室常用以下方法制取氯气:MnO2+4HCl(浓)
 MnCl2+Cl2↑+2H2O请你根据所学知识回答下列问题:
MnCl2+Cl2↑+2H2O请你根据所学知识回答下列问题:(1)把氯气通入紫色石蕊试液中,可以观察到的现象是:
(2)为保证实验安全,常用NaOH溶液吸收多余的氯气。写出反应的化学方程式
您最近一年使用:0次
2018-01-25更新
|
221次组卷
|
5卷引用:山东省桓台县2017-2018学年高一上学期期末考试化学试题
山东省桓台县2017-2018学年高一上学期期末考试化学试题山东省桓台第二中学2017-2018学年高一上学期期末考试化学试题辽宁省抚顺中学2017-2018学年高一上学期期末考试化学试题黑龙江省牡丹江中学2017-2018学年高一上学期期末考试化学试题(已下线)【艺体生百日捷进提升系列-技能方法】专题3.12 卤族方面试题的解题方法与技巧



