名校
1 . 工业上利用反应: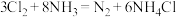 检查氯气管道是否漏气。下列说法不正确的是
检查氯气管道是否漏气。下列说法不正确的是
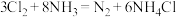 检查氯气管道是否漏气。下列说法不正确的是
检查氯气管道是否漏气。下列说法不正确的是| A.将浓氨水接近管道,若产生白烟说明管道漏气 |
B.N2的电子式为: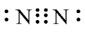 |
| C.NH4Cl中只含有离子键 |
| D.该反应中氧化剂和还原剂的物质的量之比为2∶3 |
您最近一年使用:0次
2 . 下列方程式正确的是
A.铁溶于稀硝酸,溶液变黄: |
B. 发生催化氧化反应: 发生催化氧化反应: |
C.铁和硫加热条件下反应: |
D.“气肥”要低温保存,因为碳酸氢铵受热分解: |
您最近一年使用:0次
名校
解题方法
3 . 下列物质的生产流程不正确的是
A.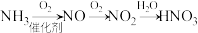 |
B.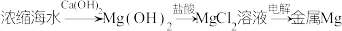 |
C.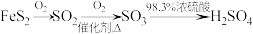 |
D.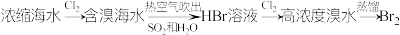 |
您最近一年使用:0次
解题方法
4 . 氨气的用途非常广泛,下列是氨气的部分转化关系图。______ (用化学式表示)。
(2)N2H4又称联氨,为二元弱碱,不如氨气稳定。
①从分子结构角度分析,N2H4不如氨气稳定的原因是______ 。
②N2H4在水中的电离与氨相似;25℃时,N2H4第一步电离平衡常数Kb1的值为______ 。
(已知:N2H4+H+ N2H
N2H K=8.7×107)
K=8.7×107)
(3)NH3在无水环境下与CO2反应生成化合物B(不稳定),继续与NH3反应生成C。已知化合物C中含有铵根离子,可完全水解,其水解产物有NH4HCO3,,下列说法正确的是______ 。
(4)实验中在加热条件下,通入过量的NH3与CuO反应,请设计实验验证尾气中比较活泼的两种气体______ 。
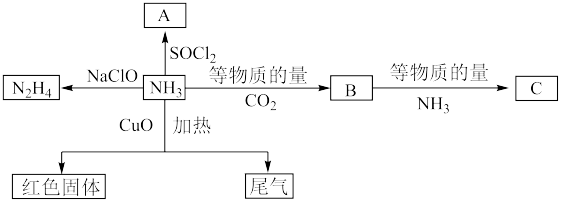
(2)N2H4又称联氨,为二元弱碱,不如氨气稳定。
①从分子结构角度分析,N2H4不如氨气稳定的原因是
②N2H4在水中的电离与氨相似;25℃时,N2H4第一步电离平衡常数Kb1的值为
(已知:N2H4+H+
 N2H
N2H K=8.7×107)
K=8.7×107)(3)NH3在无水环境下与CO2反应生成化合物B(不稳定),继续与NH3反应生成C。已知化合物C中含有铵根离子,可完全水解,其水解产物有NH4HCO3,,下列说法正确的是
| A.化合物B的化学式为NH2COOH | B.化合物B属于氨基酸 |
| C.化合物C水解生成两种盐 | D.化合物C可用于制备尿素 |
(4)实验中在加热条件下,通入过量的NH3与CuO反应,请设计实验验证尾气中比较活泼的两种气体
您最近一年使用:0次
5 . 某同学拟在实验室中用下列仪器和必需药品对 与
与 的反应进行探究。C是纯净干燥的氯气与氨气反应的装置。
的反应进行探究。C是纯净干燥的氯气与氨气反应的装置。___________ 。
(2)装置B中盛放的药品是___________ ,装置E中盛放的药品是___________ 。
(3)装置D的作用是___________ 。
(4)写出A中发生反应的化学方程式___________ 。
(⑤)反应开始后,装置C内出现大量的白烟并在内壁凝结,另一生成物是空气中主要成分之一,该反应的化学方程式为___________ 。
(6)虚线框内可选用下列装置中的___________ 装置(填字母)。
 与
与 的反应进行探究。C是纯净干燥的氯气与氨气反应的装置。
的反应进行探究。C是纯净干燥的氯气与氨气反应的装置。
(2)装置B中盛放的药品是
(3)装置D的作用是
(4)写出A中发生反应的化学方程式
(⑤)反应开始后,装置C内出现大量的白烟并在内壁凝结,另一生成物是空气中主要成分之一,该反应的化学方程式为
(6)虚线框内可选用下列装置中的

您最近一年使用:0次
解题方法
6 . 氯气管道发生泄漏可用浓氨水检验: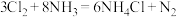 ,下列说法
,下列说法不正确 的是( 为阿伏加德罗常数的值)
为阿伏加德罗常数的值)
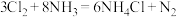 ,下列说法
,下列说法 为阿伏加德罗常数的值)
为阿伏加德罗常数的值)A.生成 时转移电子为 时转移电子为 |
| B.若产生白烟,说明此处有氯气泄漏 |
C. 仅表现氧化剂, 仅表现氧化剂, 仅表现还原性 仅表现还原性 |
D. 也有一定的氧化性,但氧化性比 也有一定的氧化性,但氧化性比 弱 弱 |
您最近一年使用:0次
名校
解题方法
7 . 不能正确描述其反应的方程式是
A.泡沫灭火器原理: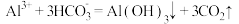 |
B.热碱去油污: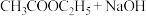  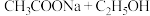 |
C.浓氨水检验氯气管道是否泄漏: |
D. 溶液遇到闪锌矿转变为铜蓝: 溶液遇到闪锌矿转变为铜蓝: |
您最近一年使用:0次
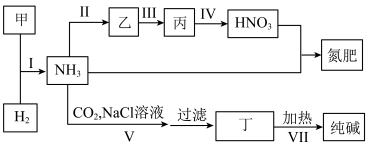
8 . 合成氨及其相关工业中,部分物质间的转化关系如图所示。回答下列问题: 的电子式:
的电子式:___________ ,反应I的化学方程式为___________ 。
(2)写出反应Ⅳ的离子方程式:___________ 。
(3)反应Ⅵ产生的___________ (填化学式)可以在流程V中被循环利用。
(4)硝酸是无色、易挥发、有刺激性气味的液体。浓硝酸一般将其保存在棕色试剂瓶中,并放置在阴凉处,说明浓硝酸具有___________ 性,用化学方程式表示该操作的原因:___________ 。
(5)乙是污染性气体,可以在催化剂加热条件下用 来处理,生成对环境没有污染的产物,写出用
来处理,生成对环境没有污染的产物,写出用 处理乙的化学方程式:
处理乙的化学方程式:___________ 。
 的电子式:
的电子式:(2)写出反应Ⅳ的离子方程式:
(3)反应Ⅵ产生的
(4)硝酸是无色、易挥发、有刺激性气味的液体。浓硝酸一般将其保存在棕色试剂瓶中,并放置在阴凉处,说明浓硝酸具有
(5)乙是污染性气体,可以在催化剂加热条件下用
 来处理,生成对环境没有污染的产物,写出用
来处理,生成对环境没有污染的产物,写出用 处理乙的化学方程式:
处理乙的化学方程式:
您最近一年使用:0次
名校
9 .  可用于生产铵盐、硝酸等。
可用于生产铵盐、硝酸等。 与
与 都可用作火箭的燃料,下列物质结构与性质或物质性质与用途具有对应关系的是
都可用作火箭的燃料,下列物质结构与性质或物质性质与用途具有对应关系的是
 可用于生产铵盐、硝酸等。
可用于生产铵盐、硝酸等。 与
与 都可用作火箭的燃料,下列物质结构与性质或物质性质与用途具有对应关系的是
都可用作火箭的燃料,下列物质结构与性质或物质性质与用途具有对应关系的是A. 极易溶于水,液氨可用作制冷剂 极易溶于水,液氨可用作制冷剂 |
B. 具有还原性,可用作火箭的燃料 具有还原性,可用作火箭的燃料 |
C. 易分解,可用作化肥 易分解,可用作化肥 |
D. 共价键数目大于 共价键数目大于 , , 的热稳定性比 的热稳定性比 的高 的高 |
您最近一年使用:0次
解题方法
10 . 研究氮及其化合物的性质对改善人类的生存环境具有重要意义。回答下列问题:
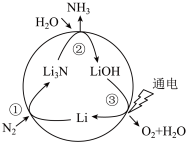
(1)一种新型人工固氮的原理如图。该转化过程①②③反应中为氧化还原反应的是___________ (填编号)。假设每一步均完全转化,每生成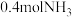 ,同时生成
,同时生成___________ 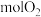 。
。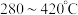 的烟气中喷入氨可使工厂废气中的氮氧化物转化为无污染的物质。写出
的烟气中喷入氨可使工厂废气中的氮氧化物转化为无污染的物质。写出 消除
消除 的化学反应方程式:
的化学反应方程式:___________ 。
(3)废水中氮的主要存在形态是硝态氮(以 存在)和氨氮(以
存在)和氨氮(以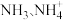 存在),还原法和氧化法是去除废水中氮的重要方法。
存在),还原法和氧化法是去除废水中氮的重要方法。
①还原法:控制其他条件相同,去除 的某含氮废水(废水中总氮
的某含氮废水(废水中总氮 )中的硝态氮,图1为只加过量
)中的硝态氮,图1为只加过量 、图2为同时加过量
、图2为同时加过量 粉与
粉与 时废水中含氮微粒的浓度随时间变化的图像。
时废水中含氮微粒的浓度随时间变化的图像。 的离子方程式为
的离子方程式为___________ ;图2中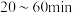 内发生主要反应的离子方程式为
内发生主要反应的离子方程式为___________ 。
②氧化法:利用 将水体中氨氮氧化为
将水体中氨氮氧化为 。已知氧化性:
。已知氧化性: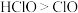 。研究发现,控制其他条件相同,当废水
。研究发现,控制其他条件相同,当废水 为
为 范围内,氨氮去除率随
范围内,氨氮去除率随 降低而升高,分析原因是
降低而升高,分析原因是___________ 。
(1)一种新型人工固氮的原理如图。该转化过程①②③反应中为氧化还原反应的是
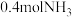 ,同时生成
,同时生成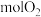 。
。
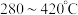 的烟气中喷入氨可使工厂废气中的氮氧化物转化为无污染的物质。写出
的烟气中喷入氨可使工厂废气中的氮氧化物转化为无污染的物质。写出 消除
消除 的化学反应方程式:
的化学反应方程式:(3)废水中氮的主要存在形态是硝态氮(以
 存在)和氨氮(以
存在)和氨氮(以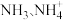 存在),还原法和氧化法是去除废水中氮的重要方法。
存在),还原法和氧化法是去除废水中氮的重要方法。①还原法:控制其他条件相同,去除
 的某含氮废水(废水中总氮
的某含氮废水(废水中总氮 )中的硝态氮,图1为只加过量
)中的硝态氮,图1为只加过量 、图2为同时加过量
、图2为同时加过量 粉与
粉与 时废水中含氮微粒的浓度随时间变化的图像。
时废水中含氮微粒的浓度随时间变化的图像。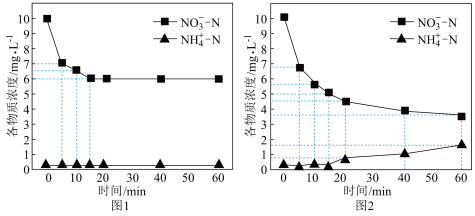
 的离子方程式为
的离子方程式为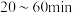 内发生主要反应的离子方程式为
内发生主要反应的离子方程式为②氧化法:利用
 将水体中氨氮氧化为
将水体中氨氮氧化为 。已知氧化性:
。已知氧化性: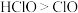 。研究发现,控制其他条件相同,当废水
。研究发现,控制其他条件相同,当废水 为
为 范围内,氨氮去除率随
范围内,氨氮去除率随 降低而升高,分析原因是
降低而升高,分析原因是
您最近一年使用:0次



