名校
解题方法
1 . 某小组设计如图所示装置(夹持装置略去)模拟侯氏制碱工艺制备 ,回答下列问题。
,回答下列问题。

(1)下列说法不正确的是______
A.③、⑤中可分别盛放饱和食盐水和浓氨水
B.C处装置的作用是防止倒吸
C.④装置中的碱石灰可换成浓硫酸
(2)想要停止①装置中反应的操作是_______ ,饱和碳酸氢钠的作用是_______ 。
(3)将下列实验操作排序:_______ 。
A.打开夹子B和⑤的分液漏斗的活塞,通气一段时间
B.检查装置气密性后加入相应药品,连接装置
C.打开夹子A,通气一段时间
D.过滤、洗涤、干燥
(4)写出③中发生的总反应的化学方程式_______ 。
(5)完成检验 溶液中的
溶液中的 的实验方案:取少量溶液于试管,加入浓氢氧化钠并加热,
的实验方案:取少量溶液于试管,加入浓氢氧化钠并加热,_______ 。
 ,回答下列问题。
,回答下列问题。
(1)下列说法不正确的是
A.③、⑤中可分别盛放饱和食盐水和浓氨水
B.C处装置的作用是防止倒吸
C.④装置中的碱石灰可换成浓硫酸
(2)想要停止①装置中反应的操作是
(3)将下列实验操作排序:
A.打开夹子B和⑤的分液漏斗的活塞,通气一段时间
B.检查装置气密性后加入相应药品,连接装置
C.打开夹子A,通气一段时间
D.过滤、洗涤、干燥
(4)写出③中发生的总反应的化学方程式
(5)完成检验
 溶液中的
溶液中的 的实验方案:取少量溶液于试管,加入浓氢氧化钠并加热,
的实验方案:取少量溶液于试管,加入浓氢氧化钠并加热,
您最近一年使用:0次
2021高三·全国·专题练习
解题方法
2 . 下列关于氨的说法正确的是
A.氨气是非电解质,氨水是电解质,NH 具有金属阳离子的一些性质 具有金属阳离子的一些性质 |
| B.氨气溶于水后,氨大部分是以NH3分子形式存在,所以氨水显弱碱性 |
| C.用碱石灰代替消石灰与氯化铵固体加热制取氨气,可使反应速率加快 |
| D.用玻璃棒蘸取浓氨水靠近浓盐酸、浓硝酸和浓硫酸都可看到有白烟生成 |
您最近一年使用:0次
解题方法
3 . 实验室制取并收集氨气的装置如图所示(部分夹持装置略),下列说法不正确 的是
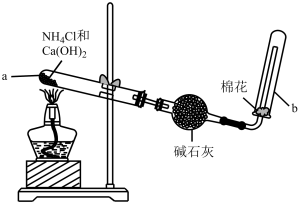

| A.加热前无需对a试管预热 |
| B.碱石灰的作用是干燥氨气 |
| C.b试管口下的原因是氨气的密度比空气大 |
D.a试管中发生的主要反应为Ca(OH)2+2NH4Cl CaCl2+2NH3↑+2H2O CaCl2+2NH3↑+2H2O |
您最近一年使用:0次
20-21高三下·浙江·阶段练习
4 . 合成氨工业是人工固氮的重要途径,氨气是工农业生产中的重要物质。请回答以下问题:
(1)下列说法不正确的是___________
A.实验室制备氨气时,可以用CaCl2固体干燥氨气
B.在浓氨水中加入生石灰可制备少量氨气
C.合成氨塔中,需要有热交换装置,便于能量的有效利用
D.合成氨工业中,可将氨气液化,并不断将液氨移去,利于提高NH3的产率
(2)氨是制取硝酸的重要原料。氨的催化氧化过程主要有以下两个反应:
I.4NH3(g)+5O2(g) 4NO(g)+6H2O(g) ΔHI
4NO(g)+6H2O(g) ΔHI
II.4NH3(g)+3O2(g) 2N2(g)+6H2O(g) ΔHII
2N2(g)+6H2O(g) ΔHII
不同温度下氨氧化的平衡常数如下(p=0.1013Mpa):
①下列说法正确的是___________
A.ΔHI>0,ΔHII>0
B.如果对反应不加控制,氨和氧气反应的最终产物主要是N2
C.为使反应有利于朝生成更多的NO方向进行,不必关注热力学问题(平衡移动问题),需要关注动力学问题(反应速率问题)
D.在实际生产中,需采用高压氧化,以利于提高NO的产率
E.反应中需控制氨氧比、选择性催化剂的形状、气固相接触时间等
②在实际工业生产中,温度一般需要在750℃~850℃左右,其主要原因是___________
(3)已知可通过下列方法合成尿素:
第一步:2NH3(1)+CO2(g) H2NCOONH4(1) ΔH=-159.5kJ/mol
H2NCOONH4(1) ΔH=-159.5kJ/mol
第二步:H2NCOONH4(1) CO(NH2)2(1)+H2O(1) ΔH=+28.5kJ/mol
CO(NH2)2(1)+H2O(1) ΔH=+28.5kJ/mol
在体积为5L的密闭容器中加入1molCO2和4molNH3,在一定条件下反应进行到10min时,测得CO2和尿素的物质的量均为0.25mol,如图所示。
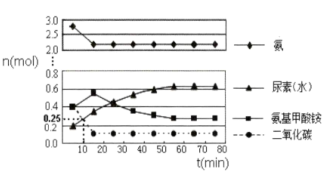
①若用单位时间内物质的量的变化来表示固体或纯液体的反应速率,则10min内第一步反应中生成H2NCOONH4(1)[氨基甲酸铵]的平均反应速率为___________
②反应进行15分钟后,随着时间的变化,尿素和氨基甲酸铵的物质的量变化比较明显,但氨气和二氧化碳的变化很小,其主要原因是___________ 。
(1)下列说法不正确的是
A.实验室制备氨气时,可以用CaCl2固体干燥氨气
B.在浓氨水中加入生石灰可制备少量氨气
C.合成氨塔中,需要有热交换装置,便于能量的有效利用
D.合成氨工业中,可将氨气液化,并不断将液氨移去,利于提高NH3的产率
(2)氨是制取硝酸的重要原料。氨的催化氧化过程主要有以下两个反应:
I.4NH3(g)+5O2(g)
 4NO(g)+6H2O(g) ΔHI
4NO(g)+6H2O(g) ΔHIII.4NH3(g)+3O2(g)
 2N2(g)+6H2O(g) ΔHII
2N2(g)+6H2O(g) ΔHII不同温度下氨氧化的平衡常数如下(p=0.1013Mpa):
| 温度(℃) | 300 | 500 | 700 | 900 | 1100 |
| 反应I(KI) | 6.3×1041 | 1.1×1026 | 2.1×1019 | 3.8×1015 | 3.4×1011 |
| 反应II(KII) | 7.3×1056 | 7.1×1034 | 2.6×1025 | 1.5×1020 | 6.7×1016 |
A.ΔHI>0,ΔHII>0
B.如果对反应不加控制,氨和氧气反应的最终产物主要是N2
C.为使反应有利于朝生成更多的NO方向进行,不必关注热力学问题(平衡移动问题),需要关注动力学问题(反应速率问题)
D.在实际生产中,需采用高压氧化,以利于提高NO的产率
E.反应中需控制氨氧比、选择性催化剂的形状、气固相接触时间等
②在实际工业生产中,温度一般需要在750℃~850℃左右,其主要原因是
(3)已知可通过下列方法合成尿素:
第一步:2NH3(1)+CO2(g)
 H2NCOONH4(1) ΔH=-159.5kJ/mol
H2NCOONH4(1) ΔH=-159.5kJ/mol第二步:H2NCOONH4(1)
 CO(NH2)2(1)+H2O(1) ΔH=+28.5kJ/mol
CO(NH2)2(1)+H2O(1) ΔH=+28.5kJ/mol在体积为5L的密闭容器中加入1molCO2和4molNH3,在一定条件下反应进行到10min时,测得CO2和尿素的物质的量均为0.25mol,如图所示。

①若用单位时间内物质的量的变化来表示固体或纯液体的反应速率,则10min内第一步反应中生成H2NCOONH4(1)[氨基甲酸铵]的平均反应速率为
②反应进行15分钟后,随着时间的变化,尿素和氨基甲酸铵的物质的量变化比较明显,但氨气和二氧化碳的变化很小,其主要原因是
您最近一年使用:0次
解题方法
5 . 硫氰化钾(KSCN)俗称玫瑰红酸钾,是一种用途广泛的化学药品。实验室模拟工业制备硫氰化钾的实验装置如图所示:
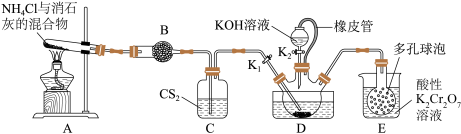
已知:①CS2不溶于水,密度比水的大;②NH3不溶于CS2;③三颈烧瓶内盛放有CS2、水和催化剂,滴加KOH溶液前,发生反应CS2+3NH3 NH4SCN+NH4HS。下列说法错误的是
NH4SCN+NH4HS。下列说法错误的是

已知:①CS2不溶于水,密度比水的大;②NH3不溶于CS2;③三颈烧瓶内盛放有CS2、水和催化剂,滴加KOH溶液前,发生反应CS2+3NH3
 NH4SCN+NH4HS。下列说法错误的是
NH4SCN+NH4HS。下列说法错误的是A.装置A中的反应为2NH4Cl+Ca(OH)2 CaCl2+2NH3↑+2H2O CaCl2+2NH3↑+2H2O |
| B.装置B中的药品为无水氯化钙 |
| C.装置D中水的作用是溶解氨气和生成的产物 |
| D.装置E的作用是吸收尾气,防止污染 |
您最近一年使用:0次
名校
解题方法
6 . 实验室模拟“侯氏制碱法”制取NaHCO3,下列说法错误的是
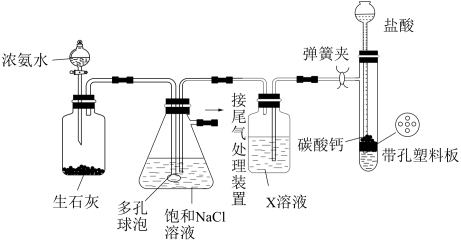
| A.X溶液为饱和碳酸钠溶液,作用是吸收二氧化碳中的氯化氢 |
| B.装置中使用“多孔球泡”可增大NH3的吸收速率 |
| C.实验时,先向饱和NaCl溶液中通入较多的NH3,再通入足量CO2 |
| D.利用锥形瓶所得分散系制备Na2CO3固体,还需经历过滤、洗涤、干燥及焙烧等过程 |
您最近一年使用:0次
2021-11-08更新
|
714次组卷
|
6卷引用:辽宁省沈阳市重点高中协作校2021-2022学年高一上学期期中测试化学试题
7 . 关于下列装置的说法正确的是
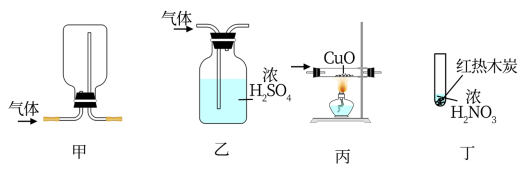

| A.可用装置甲收集NH3 |
| B.装置乙可用于干燥NH3和NO |
| C.用装置丙可验证NH3具有还原性 |
| D.若装置丁中出现红棕色气体,即可表明木炭与浓硝酸反应生成了NO2 |
您最近一年使用:0次
8 . 下列说法正确 的是
| A.工业制玻璃和陶瓷都是以石英砂为主要原料 |
| B. SO2和Cl2混合使用有更强的漂白性 |
| C.浓硫酸有吸水性,所以可以干燥H2、CO、SO2等气体 |
| D.在实验室中,可加热NH4Cl固体制取NH3 |
您最近一年使用:0次
2022-07-19更新
|
293次组卷
|
2卷引用:辽宁省协作校2021-2022学年高一下学期期末考试化学试题



