名校
解题方法
1 . 某同学设计实验验证 能还原CuO,装置(部分夹持仪器已省略)如图所示:
能还原CuO,装置(部分夹持仪器已省略)如图所示:
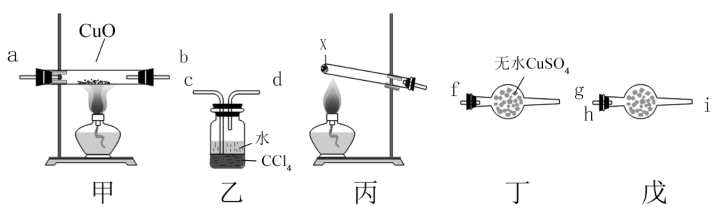
下列说法错误的是
 能还原CuO,装置(部分夹持仪器已省略)如图所示:
能还原CuO,装置(部分夹持仪器已省略)如图所示:
下列说法错误的是
A.试剂X可能是 和 和 的固体混合物 的固体混合物 |
| B.戊盛放的试剂可能是碱石灰,目的是防止空气进入装置 |
| C.装置按合理顺序连接为e→h→i→a→b→f→g→c |
D.证明 能还原CuO的实验现象是甲中黑色粉末变为红色,丁中白色固体变为蓝色 能还原CuO的实验现象是甲中黑色粉末变为红色,丁中白色固体变为蓝色 |
您最近一年使用:0次
2022-02-18更新
|
369次组卷
|
4卷引用:河北省桐柏县第一高级中学2021-2022学年高三上学期10月质量检测化学试题
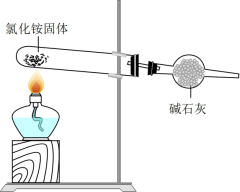
2 . 下列关于硫和氮及其化合物的说法正确的是

| A.NO2和SO2均为有刺激性气味的气体,是酸雨的主要成因 |
| B.SO2气体有还原性,故不能用浓硫酸干燥 |
| C.向浓HNO3中插入红热的炭,产生红棕色气体,证明炭可与浓HNO3反应生成NO2 |
| D.实验室可用如图装置制取氨气 |
您最近一年使用:0次
2021-10-22更新
|
262次组卷
|
2卷引用:山东省潍坊第四中学2022届高三上学期收心考试化学试题
名校
3 . 基础知识填空
(1)目前用途最广、使用量最大的合金是___________ 。
(2)重晶石的化学式为___________ 。
(3)除去 粉末中混有的少量
粉末中混有的少量 所涉及的反应的化学方程式为
所涉及的反应的化学方程式为___________ 。
(4)实验室中制备气体 的化学方程式为
的化学方程式为___________ ; 与氧气在红热的铂丝作用下的化学方程式为
与氧气在红热的铂丝作用下的化学方程式为___________ 。
(5)规范叙述-用实验方法证明某种白色晶体是
___________ 。
(6)将适量铁粉放入 溶液中,完全反应后,溶液中的
溶液中,完全反应后,溶液中的 和
和 浓度相等。则未反应的
浓度相等。则未反应的 和已反应的
和已反应的 的物质的量之比是
的物质的量之比是___________ 。
(1)目前用途最广、使用量最大的合金是
(2)重晶石的化学式为
(3)除去
 粉末中混有的少量
粉末中混有的少量 所涉及的反应的化学方程式为
所涉及的反应的化学方程式为(4)实验室中制备气体
 的化学方程式为
的化学方程式为 与氧气在红热的铂丝作用下的化学方程式为
与氧气在红热的铂丝作用下的化学方程式为(5)规范叙述-用实验方法证明某种白色晶体是

(6)将适量铁粉放入
 溶液中,完全反应后,溶液中的
溶液中,完全反应后,溶液中的 和
和 浓度相等。则未反应的
浓度相等。则未反应的 和已反应的
和已反应的 的物质的量之比是
的物质的量之比是
您最近一年使用:0次
4 . 各装置图的叙述中,正确的是
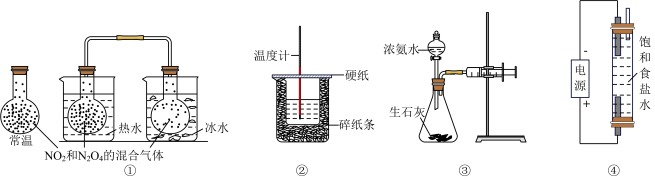

| A.①图证明温度对平衡移动的影响 |
| B.②装置能测定中和热 |
| C.③注射器活塞向右移,说明该反应为放热反应 |
| D.④装置用于制备含NaClO的消毒液 |
您最近一年使用:0次
2023-11-18更新
|
205次组卷
|
2卷引用:福建省漳州市十校2023-2024学年高二上学期期中联考化学试题
解题方法
5 . 同学们用下列装置制取并收集干燥的氨气。(某些夹持仪器和导管已略去)
(1)A中发生反应的化学方程式是_____ ,检查A中装置气密性的方法是_____ 。
(2)按气流方向,各装置接口的正确连接顺序是①→_______→_______→_______。_____
(3)B的作用是______ ,C中棉花的作用是______ 。
(4)证明氨气已收集满的方法是_____ ,所利用的氨气性质是_____ (用化学方程式表示)。
(5)实验结束后,为防止剩余氨气污染空气,可将蘸有_____ 的棉花放在A的导管口。

(1)A中发生反应的化学方程式是
(2)按气流方向,各装置接口的正确连接顺序是①→_______→_______→_______。
(3)B的作用是
(4)证明氨气已收集满的方法是
(5)实验结束后,为防止剩余氨气污染空气,可将蘸有
您最近一年使用:0次
6 . 下列实验操作能达到实验目的的是
| 选项 | 实验目的 | 实验操作 |
| A | 制备并收集 | 加热试管中的 固体,并用向下排空气法收集气体 固体,并用向下排空气法收集气体 |
| B | 证明 被氧化为 被氧化为 | 向双氧水中通入 气体,再向反应后的溶液中滴加氯化钡溶液 气体,再向反应后的溶液中滴加氯化钡溶液 |
| C | 检验淀粉是否完全水解 | 向淀粉溶液中滴加稀硫酸,充分加热一段时间后,加入过量氢氧化钠溶液,再滴入几滴碘水 |
| D | 证明酸性:苯酚<碳酸 | 将盐酸与碳酸氢钠混合产生的气体直接通入苯酚钠溶液中 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
7 . 镓(Ga)被誉为“电子工业脊梁”,性质与铝相似。氮化镓(GaN)在5G基站和互联网系统建设等方面用途广泛。以砷化镓废料(主要成分是GaAs,含Fe2O3、Al2O3和CaCO3等杂质)制备GaN和Na3AsO4∙12H2O的流程如下:

请回答下列问题:
(1)滤渣2的主要成分是_______ (填化学式)。
(2)“碱浸”中发生主要反应的化学方程式为_______ ,在该反应中氧化剂和还原剂的物质的量之比为_______ 。
(3)“调pH2”时通入过量CO2,写出离子方程式:_______ 。操作a包括蒸发浓缩、降温结晶、过滤、洗涤、低温干燥,“低温干燥”的目的是_______ 。
(4)制备氮化镓时生成一种气体,它是_______ (填化学式)。
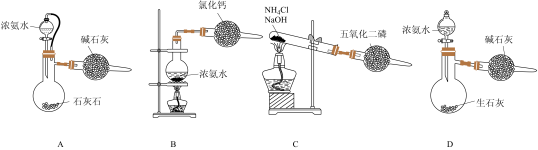
(5)制备氮化镓需要纯氨气,实验室制备氨气宜选择的装置是_______ (填字母)。
(6)设计简单实验证明滤液1是否含Fe3+:_______ 。

请回答下列问题:
(1)滤渣2的主要成分是
(2)“碱浸”中发生主要反应的化学方程式为
(3)“调pH2”时通入过量CO2,写出离子方程式:
(4)制备氮化镓时生成一种气体,它是
(5)制备氮化镓需要纯氨气,实验室制备氨气宜选择的装置是

(6)设计简单实验证明滤液1是否含Fe3+:
您最近一年使用:0次
8 . HNO3是极其重要的化工原料,在工业、农业、医药、军事等领域有着广泛的应用。
(1)工业上曾使用浓硫酸和智利硝石(主要成分NaNO3)制硝酸,但该法耗酸量大,设备腐蚀严重,现基本停止使用。此方法常用于实验室制取少量硝酸,则该反应的原理是______ 。
(2)现代工业上制备HNO3通常采用NH3催化氧化法,利用如图装置,模拟氨的催化氧化法制备硝酸。

其中,甲为氨气的发生装置。且甲中所用试剂只能从下列物质选取:
A.浓氨水 B.NH4Cl C.NH4NO3 D.CaO
①若只用一种试剂制取氨气,则该试剂的最佳选择为______ (选填试剂标号),此时,甲中空白处所需装置应为______ (选填下列标号)。

②写出装置丙中主要发生的反应化学方程式______ 。
③若装置戊中产生了大量的白烟,其成分是______ (填化学式),如何有效地抑制该现象的发生______ 。
④用上述方法制备的HNO3为稀HNO3,将它用水稀释或蒸馏、浓缩可制得不同浓度的HNO3。实验证明:不同浓度的HNO3与同一金属反应可生成不同的还原产物。例如镁与硝酸反应实验中,测得其气相产物有H2、N2、NO、NO2,液相中有Mg(NO3)2、NH4NO3和H2O。各气体产物成分及含量随HNO3的浓度变化曲线如图所示。若有48gMg与0.50L4.0mol/L的HNO3充分反应,收集到11.2L气体(标况)。则反应后液相中Mg(NO3)2与NH4NO3的浓度之比为______ 。

(1)工业上曾使用浓硫酸和智利硝石(主要成分NaNO3)制硝酸,但该法耗酸量大,设备腐蚀严重,现基本停止使用。此方法常用于实验室制取少量硝酸,则该反应的原理是
(2)现代工业上制备HNO3通常采用NH3催化氧化法,利用如图装置,模拟氨的催化氧化法制备硝酸。

其中,甲为氨气的发生装置。且甲中所用试剂只能从下列物质选取:
A.浓氨水 B.NH4Cl C.NH4NO3 D.CaO
①若只用一种试剂制取氨气,则该试剂的最佳选择为

②写出装置丙中主要发生的反应化学方程式
③若装置戊中产生了大量的白烟,其成分是
④用上述方法制备的HNO3为稀HNO3,将它用水稀释或蒸馏、浓缩可制得不同浓度的HNO3。实验证明:不同浓度的HNO3与同一金属反应可生成不同的还原产物。例如镁与硝酸反应实验中,测得其气相产物有H2、N2、NO、NO2,液相中有Mg(NO3)2、NH4NO3和H2O。各气体产物成分及含量随HNO3的浓度变化曲线如图所示。若有48gMg与0.50L4.0mol/L的HNO3充分反应,收集到11.2L气体(标况)。则反应后液相中Mg(NO3)2与NH4NO3的浓度之比为

您最近一年使用:0次
9 . 某实验小组拟制取银氨溶液,并探究银镜反应。
Ⅰ.氨气的制备
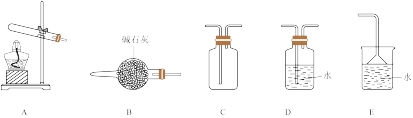
(1)利用上图装置,实验室制取氨气的化学方程式为_______ 。
(2)用上述方法制取干燥纯净的氨气,其所选装置的连接顺序为:A→_______→_______→_______(按气流方向,用英文字母表示)。_______
Ⅱ.银氨溶液制备
(3)将制得的氨气溶于水,稀释至质量分数约为2%,选用甲基橙做指示剂,用标准盐酸滴定其物质的量浓度,达到滴定终点的现象为_______ 。
(4)取上述新制氨水,进行如下实验。已知:白色AgOH沉淀不稳定,极易分解生成棕褐色 ;
; 溶于浓氨水生成
溶于浓氨水生成 。
。
①步骤a中产生沉淀的离子方程式_______ 。
②取步骤b中制得的银氨溶液,进行如下实验,

通过对溶液A的检验,可证明银氨溶液中溶质主要为 ,而不是
,而不是 。请将实验方案和现象补充完整:
。请将实验方案和现象补充完整:
取少量溶液A于试管中,测定其pH约为10(查资料得知同浓度的 ,pH在13左右);
,pH在13左右);
另取少量溶液A于试管中,加入过量盐酸酸化后滤去沉淀,再向滤液中加入_______ (试剂名称),充分反应后若出现_______ ,则证明溶质为 。
。
Ⅲ.银镜反应:
已知:随 降低,
降低, 氧化性减弱,银氨溶液中存在平衡
氧化性减弱,银氨溶液中存在平衡 。
。
(5)分析实验,推测实验d中未见银镜的原因可能是_______ 。
Ⅰ.氨气的制备
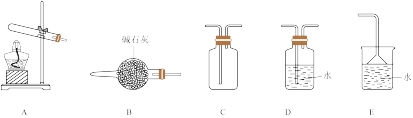
(1)利用上图装置,实验室制取氨气的化学方程式为
(2)用上述方法制取干燥纯净的氨气,其所选装置的连接顺序为:A→_______→_______→_______(按气流方向,用英文字母表示)。
Ⅱ.银氨溶液制备
(3)将制得的氨气溶于水,稀释至质量分数约为2%,选用甲基橙做指示剂,用标准盐酸滴定其物质的量浓度,达到滴定终点的现象为
(4)取上述新制氨水,进行如下实验。已知:白色AgOH沉淀不稳定,极易分解生成棕褐色
 ;
; 溶于浓氨水生成
溶于浓氨水生成 。
。| 实验装置 | 步骤 | 实验操作 | 实验现象 |
 | a | 向试管中滴加2~3滴2%氨水,并不断振荡 | 产生棕褐色沉淀 |
| b | 继续向试管中逐滴加入2%氨水,并不断振荡,至沉淀恰好完全溶解,停止滴加氨水。 | 沉淀消失 |
②取步骤b中制得的银氨溶液,进行如下实验,

通过对溶液A的检验,可证明银氨溶液中溶质主要为
 ,而不是
,而不是 。请将实验方案和现象补充完整:
。请将实验方案和现象补充完整:取少量溶液A于试管中,测定其pH约为10(查资料得知同浓度的
 ,pH在13左右);
,pH在13左右);另取少量溶液A于试管中,加入过量盐酸酸化后滤去沉淀,再向滤液中加入
 。
。Ⅲ.银镜反应:
已知:随
 降低,
降低, 氧化性减弱,银氨溶液中存在平衡
氧化性减弱,银氨溶液中存在平衡 。
。| 实验装置 | 步骤 | 实验操作 | 实验现象 |
 | c | 取步骤b中得到的银氨溶液于试管中,加入3滴新开瓶的40%的乙醛溶液;水浴加热3分钟 | 试管内壁出现光亮的银镜 |
| d | 取步骤b中得到银氨溶液的试管中滴加浓氨水,无明显现象,加入新开瓶的40%的乙醛溶液,振荡,水浴加热3分钟 | 闻到刺激性气味,溶液略显灰色,试管壁未见银镜 |
您最近一年使用:0次
2022-12-28更新
|
490次组卷
|
3卷引用:广东省汕头市普通高中2022-2023学年高三上学期教学质量检测化学试题
名校
10 . 教材中设计了很多制取物质或检验物质的性质的实验,下列实验装置可以达到实验目的的是


| A.图一用于实验室制取和收集氨气 |
| B.图二用于证明干燥的氯气没有漂白性 |
| C.图三用于证明铜的金属性比锌弱 |
| D.图四用于制取蒸馏水 |
您最近一年使用:0次
2021-11-06更新
|
86次组卷
|
2卷引用:湘豫名校2021-2022学年高三上学期联考(11月)化学试题



