1 . 氮是自然界各种生命活动不可缺少的重要元素。
I.自然界中氮的循环(如图所示)

(1)豆科植物的根瘤进行固氮的过程属于______ (填“化学”或“物理)变化;通过雷电作用进行固氮过程中,第一步反应的化学方程式为______ 。
(2)某氮肥厂产生的氨氮废水中的氮元素多以 和
和 的形式存在,设计如下处理流程:
的形式存在,设计如下处理流程:

①过程I:加NaOH溶液,调节pH至9后,升温至30℃,通入空气将氨赶出并回收。加入NaOH溶液时,所发生反应的离子方程式为______ 。
②过程II:在微生物作用下实现 的转化,称为硝化过程。在碱性条件下,
的转化,称为硝化过程。在碱性条件下, 被氧气氧化为
被氧气氧化为 的总反应的离子方程式为
的总反应的离子方程式为______ 。
II.实验室制氨气
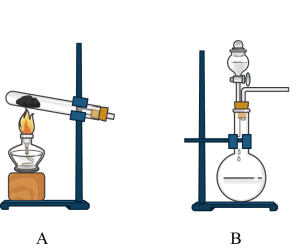
(3)实验室制备氨气可以选择A或B装置,如果选择A装置,则发生反应的化学方程式为______ ;如果选择B装置,则分液漏斗中盛装的物质为______ (填名称):干燥氨气时,可选用的干燥剂为______ ;收集氨气采用______ 法。
III.浓硝酸和稀硝酸氧化性强弱比较
(4)按如图所示装置进行实验(加持装置已略去),实验证明浓硝酸的氧化性强于稀硝酸,依据为浓硝酸能将NO氧化为NO2,而稀硝酸不能。
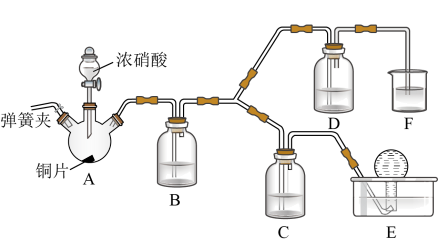
已知:NaOH溶液不与NO反应,能与NO2反应。
①浓硝酸应保存在棕色试剂瓶中,用化学方程式解释其原因为______ 。
②装置A中发生反应的化学方程式为______ ;装置B的作用为______ 。
③装置D中的现象为______ ;C中盛放的试剂为______ 。
I.自然界中氮的循环(如图所示)

(1)豆科植物的根瘤进行固氮的过程属于
(2)某氮肥厂产生的氨氮废水中的氮元素多以
 和
和 的形式存在,设计如下处理流程:
的形式存在,设计如下处理流程:
①过程I:加NaOH溶液,调节pH至9后,升温至30℃,通入空气将氨赶出并回收。加入NaOH溶液时,所发生反应的离子方程式为
②过程II:在微生物作用下实现
 的转化,称为硝化过程。在碱性条件下,
的转化,称为硝化过程。在碱性条件下, 被氧气氧化为
被氧气氧化为 的总反应的离子方程式为
的总反应的离子方程式为II.实验室制氨气
(3)实验室制备氨气可以选择A或B装置,如果选择A装置,则发生反应的化学方程式为

III.浓硝酸和稀硝酸氧化性强弱比较
(4)按如图所示装置进行实验(加持装置已略去),实验证明浓硝酸的氧化性强于稀硝酸,依据为浓硝酸能将NO氧化为NO2,而稀硝酸不能。

已知:NaOH溶液不与NO反应,能与NO2反应。
①浓硝酸应保存在棕色试剂瓶中,用化学方程式解释其原因为
②装置A中发生反应的化学方程式为
③装置D中的现象为
您最近一年使用:0次
2 . 下列因果关系叙述正确的是
A. 具有漂白性,故可使酸性 具有漂白性,故可使酸性 溶液褪色 溶液褪色 |
B.浓硝酸中的 见光会分解,故有时在实验室看到的浓硝酸呈黄色 见光会分解,故有时在实验室看到的浓硝酸呈黄色 |
C.Na的金属性比Mg强,故可用Na与 溶液反应制取Mg 溶液反应制取Mg |
D. 有还原性,浓硫酸有强氧化性,故不能用浓硫酸干燥 有还原性,浓硫酸有强氧化性,故不能用浓硫酸干燥 |
您最近一年使用:0次
解题方法
3 . 硝酸是一种具有强氧化性、腐蚀性的强酸,其还原产物因硝酸浓度的不同而有变化,从总体上说,硝酸浓度越高,平均每分子硝酸得到的电子数越少,浓硝酸的还原产物 主要为 NO2、稀硝酸的还原产物为 NO。实验室中,常用 Cu 与浓 HNO3 反应制取 NO2,用 Cu与稀 HNO3 反应制取 NO。
(1)浓硝酸具有以下性质:
①强氧化性 ②酸性 ③还原性 ④不稳定性 ⑤挥发性
下列反应或者现象主要体现了硝酸的什么性质:
①久置浓硝酸显黄色_______ (填序号,下同)。
②用稀硝酸清洗试管壁上的银_______ 。
③稀硝酸清洗石灰水试剂瓶壁上的固体_______ 。
(2)请写出实验室中用 Cu 与稀 HNO3 反应制取 NO 的化学方程式_______ 。
(3)64gCu 与适量的浓 HNO3 反应,铜全部作用后,共收集到 22.4L 气体(标准状况下),反应中消耗HNO3 的物质的量是_______(填字母代号)。
(1)浓硝酸具有以下性质:
①强氧化性 ②酸性 ③还原性 ④不稳定性 ⑤挥发性
下列反应或者现象主要体现了硝酸的什么性质:
①久置浓硝酸显黄色
②用稀硝酸清洗试管壁上的银
③稀硝酸清洗石灰水试剂瓶壁上的固体
(2)请写出实验室中用 Cu 与稀 HNO3 反应制取 NO 的化学方程式
(3)64gCu 与适量的浓 HNO3 反应,铜全部作用后,共收集到 22.4L 气体(标准状况下),反应中消耗HNO3 的物质的量是_______(填字母代号)。
| A.0.5mol | B.1.0mol | C.2.0mol | D.3.0mol |
您最近一年使用:0次
名校
解题方法
4 . 某化学兴趣小组用如图装置验证NO2的氧化性和NO的还原性,请回答下列问题:

(1)打开盛有浓硝酸的试剂瓶,瓶口会出现白雾,说明浓硝酸具有_______ 性;久置的浓硝酸呈黄色的原因:_______ (用化学方程式表示)。
(2)向锥形瓶中加入一定量的浓硝酸,若开始时生成的是红棕色气体,则甲中反应的化学方程式为_______ ,根据该化学方程式说明硝酸具有_______ (填字母)。
A.酸性 B.还原性 C.氧化性 D.不稳定性 E.漂白性
(3)说明NO2具有氧化性的现象是_______ ,但有同学指出该处实验设计存在不足之处,他的理由是_______ 。
(4)说明NO具有还原性的操作和现象是_______ 。
(5)往含有0.5 mol H2SO4、0.2 mol HNO3的混合酸稀溶液中加入32 g铜粉,充分反应后能收集到标准状况下_______ L NO气体。

(1)打开盛有浓硝酸的试剂瓶,瓶口会出现白雾,说明浓硝酸具有
(2)向锥形瓶中加入一定量的浓硝酸,若开始时生成的是红棕色气体,则甲中反应的化学方程式为
A.酸性 B.还原性 C.氧化性 D.不稳定性 E.漂白性
(3)说明NO2具有氧化性的现象是
(4)说明NO具有还原性的操作和现象是
(5)往含有0.5 mol H2SO4、0.2 mol HNO3的混合酸稀溶液中加入32 g铜粉,充分反应后能收集到标准状况下
您最近一年使用:0次
5 . 对下列事实的解释错误的是
| A.浓硝酸在光照下颜色变黄,说明浓硝酸的不稳定性 |
| B.从氨气喷泉实验可知氨气易溶于水且其水溶液显碱性 |
| C.蓝色石蕊试纸上滴加浓硝酸,试纸先变红再褪色,说明浓硝酸有酸性和强氧化性 |
| D.常温下,铝制品可盛放浓硝酸,说明浓硝酸与铝不反应 |
您最近一年使用:0次
6 . 对下列事实的解释错误的是
| A.浓硝酸在光照下颜色变黄,说明浓硝酸的不稳定性 |
| B.常温下,铝制品可盛放浓硝酸,说明浓硝酸与铝不反应 |
| C.蓝色石蕊试纸上滴入浓硝酸,试纸先变红再褪色,说明浓硝酸有酸性和强氧化性 |
| D.从氨气喷泉实验可知氨气易溶于水且其水溶液显碱性 |
您最近一年使用:0次
7 . 将硝酸表现出的性质填在下列各反应操作或现象后:
A.氧化性 B.酸性 C.还原性 D.不稳定性
(1)久置的浓硝酸变黄色___ 。
(2)用硝酸浸洗附有银的试管___ 。
(3)常温下用铁制或铝制容器贮存、运输浓HNO3___ 。
(4)用稀HNO3浸洗久置石灰水试剂瓶上的固体___ 。
(5)用Cu和稀HNO3制NO气体___ 。
(6)浓HNO3中滴入石蕊溶液并微热,石蕊溶液先变红后褪色___ 。
A.氧化性 B.酸性 C.还原性 D.不稳定性
(1)久置的浓硝酸变黄色
(2)用硝酸浸洗附有银的试管
(3)常温下用铁制或铝制容器贮存、运输浓HNO3
(4)用稀HNO3浸洗久置石灰水试剂瓶上的固体
(5)用Cu和稀HNO3制NO气体
(6)浓HNO3中滴入石蕊溶液并微热,石蕊溶液先变红后褪色
您最近一年使用:0次
2021-06-10更新
|
285次组卷
|
3卷引用:吉林省延边朝鲜族自治州延边二中北校区2020-2021学年高一下学期第一次月考化学试题
名校
解题方法
8 . 按要求填空
(1)浓硫酸具有如下的性质:A.酸性B.强氧化性C.吸水性D.脱水性,E难挥发性。下列事实主要表现浓硫酸的什么性质(填字母序号)。
①浓硫酸使蔗糖变黑___________
②碳投入热的浓硫酸中溶解___________
③浓硫酸与氧化铜反应___________
④浓硫酸干燥氢气___________
(2)浓硝酸具有如下的性质:A.酸性B.强氧化性C.不稳定性,下列事实主要表现浓硝酸的什么性质(填字母序号)。
①浓硝酸需避光保存___________
②常温下可用铝或者铁遇浓硝酸钝化___________
(3)二氧化硫气体在下列反应中表现的性质填写在横线上。
A.氧化性B.漂白性C.还原性D.酸性氧化物的性质
①SO2+2OH-= +H2O
+H2O___________
②SO2+2H2S=3S↓+2H2O___________
③SO2+Ca(OH)2=CaSO3↓+H2O___________
④SO2+Cl2+2H2O=2HCl+H2SO4___________
(1)浓硫酸具有如下的性质:A.酸性B.强氧化性C.吸水性D.脱水性,E难挥发性。下列事实主要表现浓硫酸的什么性质(填字母序号)。
①浓硫酸使蔗糖变黑
②碳投入热的浓硫酸中溶解
③浓硫酸与氧化铜反应
④浓硫酸干燥氢气
(2)浓硝酸具有如下的性质:A.酸性B.强氧化性C.不稳定性,下列事实主要表现浓硝酸的什么性质(填字母序号)。
①浓硝酸需避光保存
②常温下可用铝或者铁遇浓硝酸钝化
(3)二氧化硫气体在下列反应中表现的性质填写在横线上。
A.氧化性B.漂白性C.还原性D.酸性氧化物的性质
①SO2+2OH-=
 +H2O
+H2O②SO2+2H2S=3S↓+2H2O
③SO2+Ca(OH)2=CaSO3↓+H2O
④SO2+Cl2+2H2O=2HCl+H2SO4
您最近一年使用:0次
9 . 将硝酸表现出的性质填在下列各反应操作或现象后:
A.氧化性 B.酸性 C.还原性 D.不稳定性
(1)用硝酸浸洗附有银的试管___ 。
(2)常温下用铁制或铝制容器贮存、运输浓HNO3__ 。
(3)久置的浓硝酸变黄色__ 。
A.氧化性 B.酸性 C.还原性 D.不稳定性
(1)用硝酸浸洗附有银的试管
(2)常温下用铁制或铝制容器贮存、运输浓HNO3
(3)久置的浓硝酸变黄色
您最近一年使用:0次
名校
解题方法
10 . 下列反应或者现象主要体现了硝酸的什么性质?久置浓硝酸显黄色________ (填序号,下同),用稀硝酸清洗试管壁上的银________ ,稀硝酸清洗石灰水试剂瓶壁上的固体________ ,用浓硝酸清洗积碳的试管________ 。
①(强)氧化性 ②酸性 ③还原性 ④不稳定性 ⑤挥发性 ⑥脱水性 ⑦吸水性
①(强)氧化性 ②酸性 ③还原性 ④不稳定性 ⑤挥发性 ⑥脱水性 ⑦吸水性
您最近一年使用:0次
2020-09-29更新
|
121次组卷
|
2卷引用:河南省许昌市长葛市第一高级中学2020-2021学年高一上学期9月月考化学试题



