名校
解题方法
1 . 下列反应的离子方程式书写正确的是
| A.盐酸除铁锈:6H+ + Fe2O3 = 2Fe3++3H2O |
B.Na2O2与CO2反应制备O2:Na2O2+CO2=2Na++CO +O2↑ +O2↑ |
C.向碳酸氢铵溶液中加过量石灰水并加热: +OH- +OH- NH3↑+H2O NH3↑+H2O |
D.用酸化的高锰酸钾溶液氧化双氧水:2 +6H++H2O2=2Mn2++3O2↑+4H2O +6H++H2O2=2Mn2++3O2↑+4H2O |
您最近一年使用:0次
21-22高三上·上海杨浦·期中
名校
解题方法
2 . 下列指定反应的离子方程式正确的是
A.用过量氨水吸收工业尾气中的 ; ;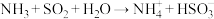 |
B. 溶液中加入少量 溶液中加入少量 溶液: 溶液: |
C.等物质的量的 、 、 、 、 三种溶液混合: 三种溶液混合: |
D. 溶液与少量 溶液与少量 溶液反应: 溶液反应: |
您最近一年使用:0次
2021-11-26更新
|
1566次组卷
|
4卷引用:一轮巩固卷3-【赢在高考·黄金20卷】备战2022年高考化学模拟卷(湖北专用)
(已下线)一轮巩固卷3-【赢在高考·黄金20卷】备战2022年高考化学模拟卷(湖北专用)上海市复旦大学附属中学2021-2022学年高三上学期期中考试化学试题(已下线)3.3 氮的循环-2021-2022学年高一化学课后培优练(鲁科版2019必修第一册)福建省泉州市两校2021-2022学年高一下学期期中联考化学试题
解题方法
3 . 工业以黄铁矿为原料生产硫酸,吸收塔排出的尾气先用氨水吸收,再用浓硫酸处理,得到较高浓度的SO2和铵盐。为测定该铵盐中氮元素的质量分数,将不同质量的铵盐分别加入到50.00mL相同浓度的NaOH溶液中,沸水浴加热至气体全部逸出(此温度下铵盐不分解)。该气体经干燥后用浓硫酸吸收完全,测定浓硫酸增加的质量。部分测定结果如下表:
计算:该铵盐中氮元素的质量分数_______ (计算结果保留两位小数)
| 铵盐的质量(g) | 10.00 | 20.00 | 30.00 | 50.00 |
| 浓硫酸增加的质量(g) | m | m | 1.29 | 0 |
计算:该铵盐中氮元素的质量分数
您最近一年使用:0次
名校
4 . 如图是某元素的化合价——物质类型二维图。其中X是一种常见的强碱,G为正盐,通常条件下Z是无色液体,D的相对分子质量比C小16,各物质的转化关系如图所示。下列说法正确的是
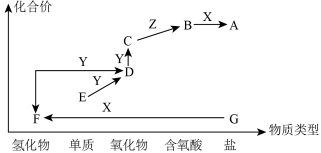

| A.E可以是金属也可以是非金属 |
| B.C和D两种大气污染物,都能用排水法收集 |
| C.B的浓溶液具有吸水性,可用来干燥气体 |
| D.实验室制备F时,可以将其浓溶液滴入碱石灰中进行制取 |
您最近一年使用:0次
2021-05-20更新
|
769次组卷
|
8卷引用:湖北省巴东第三高级中学2021-2022学年高一下学期第一次月考化学试题
解题方法
5 . 工业制得的氮化铝(AlN)产品中常含有少量Al4C3、Al2O3、C等杂质。某同学设计如下实验分别测定氮化铝(AlN)样品中AlN和Al4C3的质量分数。已知①Al4C3与硫酸反应可生成CH4;②AlN溶于强酸产生铵盐,溶于强碱生成氨气(忽略NH3在强碱性溶液中的溶解);③该实验条件下的气体摩尔体积为VmL/mol,实验装置如下(量气管为碱式滴定管改装)
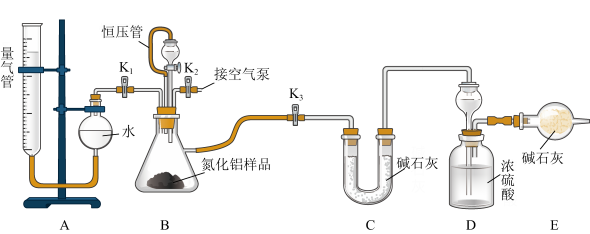
实验过程:连好装置后,检验装置的气密性;称得装置D的初始质量为ag;称取bg AlN样品置于装置B的锥形瓶中,各装置中加入相应药品,重新连好装置;读取量气管中液面的初始读数为x mL(量气装置左右液面相平)。
(1)①若先测量Al4C3质量分数,对K1、K2、K3三个活塞的操作是关闭活塞______ ,打开活塞______ 。
②当_____ 时,说明反应已经结束。读取读数之前,应对量气管进行的操作为____________ ;若量气管中的液面高于右侧球形容器中的液面,所测气体体积______ (填“偏大”、“偏小”或“无影响”)。
③记录滴定管的读数为y mL,则Al4C3的质量分数为_________ (用可能含a、b、x、y、Vm的代数式表示)。
④若无恒压管,对所测Al4C3质量分数的影响是______ (填“偏大”、“偏小”或“无影响”)。
(2)若先测量AlN质量分数:首先关闭活塞K1,打开活塞K3,通过分液漏斗加入过量的某物质,写出AlN与过量的某物质发生反应的离子方程式为__________ ;反应完成后,__________ (填该步应进行的操作),最后称得装置D的质量为cg,进而测量AlN的质量分数。

实验过程:连好装置后,检验装置的气密性;称得装置D的初始质量为ag;称取bg AlN样品置于装置B的锥形瓶中,各装置中加入相应药品,重新连好装置;读取量气管中液面的初始读数为x mL(量气装置左右液面相平)。
(1)①若先测量Al4C3质量分数,对K1、K2、K3三个活塞的操作是关闭活塞
②当
③记录滴定管的读数为y mL,则Al4C3的质量分数为
④若无恒压管,对所测Al4C3质量分数的影响是
(2)若先测量AlN质量分数:首先关闭活塞K1,打开活塞K3,通过分液漏斗加入过量的某物质,写出AlN与过量的某物质发生反应的离子方程式为
您最近一年使用:0次
解题方法
6 . 某混合溶液中可能大量含有的离子如下表所示:
为探究其成分,某同学将Na2O2逐渐加入到上述混合溶液中并微热,产生沉淀和气体的物质的量与加入Na2O2的物质的量的关系分别如图所示。
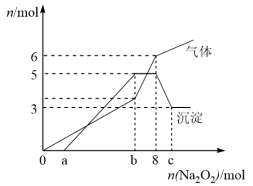
(1)该溶液中一定含有的阳离子是________________________________ ,其对应物质的量浓度之比为 ____________ ,溶液中一定不存在的阴离子是_______________________ 。
(2)写出沉淀减少的离子方程式________________________________________________ 。
| 阳离子 | H+、K+、Al3+、NH4+、Mg2+ |
| 阴离子 | Cl-、OH-、CO32-、AlO2- |

(1)该溶液中一定含有的阳离子是
(2)写出沉淀减少的离子方程式
您最近一年使用:0次
名校
解题方法
7 . 从某些性质来看,NH3和H2O、NH4+和H+、NH2-和OH-、N3-和O2-两两类似。据此判断,下列反应中正确的是
①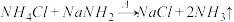
②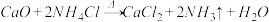
③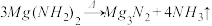
①
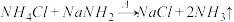
②
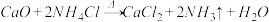
③
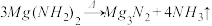
| A.仅①正确 | B.②③正确 | C.①③正确 | D.全部正确 |
您最近一年使用:0次
2017-05-05更新
|
479次组卷
|
4卷引用:湖北省荆门市龙泉中学2021-2022学年高一上学期11月月考(实验班)化学试题
湖北省荆门市龙泉中学2021-2022学年高一上学期11月月考(实验班)化学试题上海市复旦大学附中浦东分校2016-2017学年高一下学期期中考试化学试题江西省上高二中2017-2018学年高一第四次月考化学试题(已下线)小题必刷13 镁及其化合物——2021年高考化学一轮复习小题必刷(通用版)
名校
解题方法
8 . 下列指定反应的离子方程式正确的是
| A.用CH3COOH溶解CaCO3:CaCO3+2H+=Ca2++H2O+CO2↑ |
| B.Cu溶于稀硝酸:Cu+2H++NO3-=Cu2++NO2↑+H2O |
| C.(NH4)2Fe(SO4)2溶液与过量NaOH溶液反应制Fe(OH)2:Fe2++2OH-=Fe(OH)2↓ |
D.向NaAlO2溶液中通入过量CO2:CO2+AlO +2H2O=Al(OH)3↓+HCO +2H2O=Al(OH)3↓+HCO |
您最近一年使用:0次
2016-12-09更新
|
694次组卷
|
2卷引用:2014-2015学年湖北省荆门市高一下学期期末质量检测化学试卷



