名校
解题方法
1 . 如图1所示,某同学利用 和
和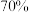 的
的 溶液制取
溶液制取 并探究其性质。
并探究其性质。
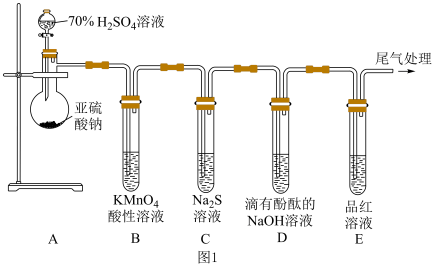
(1)装置B中发生反应的离子方程式为______________ 。
(2)装置C中的实验现象是______________ ,该实验现象说明 具有
具有_______ (填“氧化”或“还原”)性。
(3)装置 的目的是探究
的目的是探究 与品红作用的可逆性,请写出实验操作及现象:
与品红作用的可逆性,请写出实验操作及现象:______________ 。
(4)探究 的酸性强于
的酸性强于 ,该同学用如图2所示装置达成实验目的。
,该同学用如图2所示装置达成实验目的。
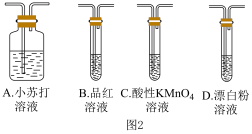
①装置的连接顺序为_______ ,D中产生白色沉淀,则反应的离子方程式为_______ 。
纯净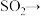 _______
_______ _______
_______ _______
_______ _______(填字母),
_______(填字母),
②可证明 的酸性强于
的酸性强于 的实验现象是
的实验现象是______________ 。
 和
和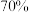 的
的 溶液制取
溶液制取 并探究其性质。
并探究其性质。
(1)装置B中发生反应的离子方程式为
(2)装置C中的实验现象是
 具有
具有(3)装置
 的目的是探究
的目的是探究 与品红作用的可逆性,请写出实验操作及现象:
与品红作用的可逆性,请写出实验操作及现象:(4)探究
 的酸性强于
的酸性强于 ,该同学用如图2所示装置达成实验目的。
,该同学用如图2所示装置达成实验目的。
①装置的连接顺序为
纯净
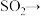 _______
_______ _______
_______ _______
_______ _______(填字母),
_______(填字母),②可证明
 的酸性强于
的酸性强于 的实验现象是
的实验现象是
您最近半年使用:0次
2024-01-13更新
|
365次组卷
|
3卷引用:河南省百师联考2023-2024学年高一上学期1月期末化学试题
2 . 实验室可用如图装置(略去部分夹持仪器)制取 并验证其性质。
并验证其性质。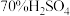 溶液的仪器名称为
溶液的仪器名称为_______ 。
(2)装置 的作用之一是通过观察产生气泡的多少判断
的作用之一是通过观察产生气泡的多少判断 生成的快慢,其中的液体最好选择_______(填字母)。
生成的快慢,其中的液体最好选择_______(填字母)。
(3) 试管中的试剂可以验证二氧化硫的氧化性,现象为
试管中的试剂可以验证二氧化硫的氧化性,现象为_______ 。经测定,产物中还有一种相对分子质量为104的酸式盐,则该反应的离子方程式为_______ 。
(4)为验证二氧化硫的还原性,充分反应后,取试管 中的溶液分成三份,分别进行如下实验:
中的溶液分成三份,分别进行如下实验:
方案Ⅰ:向第一份溶液中加入 溶液,有白色沉淀生成;
溶液,有白色沉淀生成;
方案Ⅱ:向第二份溶液中加入品红溶液,红色褪去;
方案Ⅲ:向第三份溶液中加入 溶液,产生白色沉淀。
溶液,产生白色沉淀。
上述方案中能达到实验目的的是方案_______ (填“Ⅰ”“Ⅱ”或“Ⅲ”);试管 中
中 发生反应的离子方程式为
发生反应的离子方程式为_______ 。
(5)装置 的作用是
的作用是_______ 。装置 中为
中为_______ 溶液。
 并验证其性质。
并验证其性质。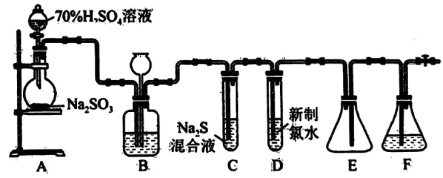
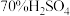 溶液的仪器名称为
溶液的仪器名称为(2)装置
 的作用之一是通过观察产生气泡的多少判断
的作用之一是通过观察产生气泡的多少判断 生成的快慢,其中的液体最好选择_______(填字母)。
生成的快慢,其中的液体最好选择_______(填字母)。| A.蒸馏水 | B.饱和 溶液 溶液 | C.饱和 溶液 溶液 | D.饱和 溶液 溶液 |
 试管中的试剂可以验证二氧化硫的氧化性,现象为
试管中的试剂可以验证二氧化硫的氧化性,现象为(4)为验证二氧化硫的还原性,充分反应后,取试管
 中的溶液分成三份,分别进行如下实验:
中的溶液分成三份,分别进行如下实验:方案Ⅰ:向第一份溶液中加入
 溶液,有白色沉淀生成;
溶液,有白色沉淀生成;方案Ⅱ:向第二份溶液中加入品红溶液,红色褪去;
方案Ⅲ:向第三份溶液中加入
 溶液,产生白色沉淀。
溶液,产生白色沉淀。上述方案中能达到实验目的的是方案
 中
中 发生反应的离子方程式为
发生反应的离子方程式为(5)装置
 的作用是
的作用是 中为
中为
您最近半年使用:0次
名校
解题方法
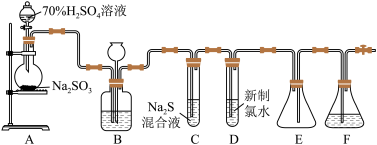
3 . 实验室可用如图装置(略去部分夹持仪器)制取SO2并验证其性质。____ 。
(2)装置B的作用之一是通过观察产生气泡的多少判断SO2生成的快慢,其中的液体最好选择______ (填代号)。
a.蒸馏水 b.饱和NaHCO3溶液 c.饱和NaHSO3溶液 d.饱和NaOH溶液
(3)C试管中的试剂可以验证二氧化硫的氧化性,现象为_______ 。
(4)为验证二氧化硫的还原性,充分反应后,取试管D中的溶液分成三份,分别进行如下实验:
方案Ⅰ:向第一份溶液中加入AgNO3溶液,有白色沉淀生成;
方案Ⅱ:向第二份溶液中加入品红溶液,红色褪去;
方案Ⅲ:向第三份溶液中加入BaCl2溶液,产生白色沉淀。
上述方案中能达到实验目的的是方案____ (填“Ⅰ”“Ⅱ”或“Ⅲ”);试管D中发生反应的离子方程式为_____ 。
(5)装置E的作用是______ 。装置F中为_____ 溶液。
(2)装置B的作用之一是通过观察产生气泡的多少判断SO2生成的快慢,其中的液体最好选择
a.蒸馏水 b.饱和NaHCO3溶液 c.饱和NaHSO3溶液 d.饱和NaOH溶液
(3)C试管中的试剂可以验证二氧化硫的氧化性,现象为
(4)为验证二氧化硫的还原性,充分反应后,取试管D中的溶液分成三份,分别进行如下实验:
方案Ⅰ:向第一份溶液中加入AgNO3溶液,有白色沉淀生成;
方案Ⅱ:向第二份溶液中加入品红溶液,红色褪去;
方案Ⅲ:向第三份溶液中加入BaCl2溶液,产生白色沉淀。
上述方案中能达到实验目的的是方案
(5)装置E的作用是
您最近半年使用:0次
名校
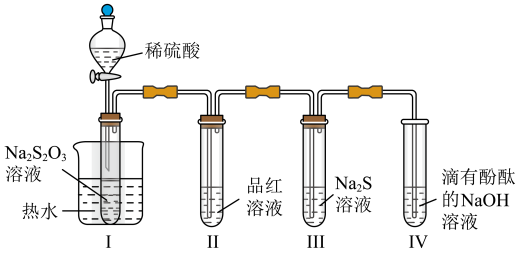
4 . 按图装置进行实验。将稀硫酸全部加入Ⅰ中的试管,关闭活塞。
回答下列问题:
(1)盛放稀硫酸的仪器名称是___________ 。
(2)Ⅰ中试管内反应的离子方程式是___________ 。
(3)撤掉水浴,重做实验,Ⅱ中品红溶液褪色___________ (填“加快”“减慢”“无变化” “无法确定”)。
(4)试管Ⅳ中滴有酚酞的NaOH 溶液的作用是___________ 。
(5)试管Ⅲ的Na2S溶液若换为Na2S和Na2CO3混合溶液,先会变浑浊,后又变澄清(生成Na2S2O3溶液)。此浑浊物是___________ ,此过程总反应的化学方程式为:___________ 。
(6)实验已经验证SO2的部分化学性质,请设计实验验证SO2的其它化学性质___________ (包括实验目的、实验原理、操作现象)。

回答下列问题:
(1)盛放稀硫酸的仪器名称是
(2)Ⅰ中试管内反应的离子方程式是
(3)撤掉水浴,重做实验,Ⅱ中品红溶液褪色
(4)试管Ⅳ中滴有酚酞的NaOH 溶液的作用是
(5)试管Ⅲ的Na2S溶液若换为Na2S和Na2CO3混合溶液,先会变浑浊,后又变澄清(生成Na2S2O3溶液)。此浑浊物是
(6)实验已经验证SO2的部分化学性质,请设计实验验证SO2的其它化学性质
您最近半年使用:0次
名校
解题方法
5 . 某校合作学习小组的同学设计实验验证Na2SO4与焦炭高温加热后的产物。回答下列问题。
(1)Na2SO4与焦炭反应的实验装置如下图所示:
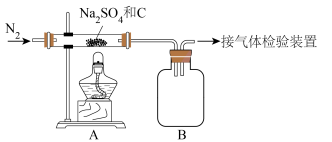
①先通入N2,然后加热,直至反应结束,整个过程中N2的作用是___________ 。
②装置B的作用是___________ 。
(2)该小组推测气体产物中含有CO2、CO及SO2,并进行验证。选用上述实验中的装置A、B和下图所示的部分装置(可以重复选用)进行实验。经过查找资料,得到如下信息:
a.SO2与碱的反应和CO2与碱的反应类似;
b.SO2可以使品红溶液褪色,该反应可用来检验SO2;
c.KMnO4可以被SO2还原成Mn2+;
d.氧化还原反应中化合价发生变化的元素,化合价升降总数相等,例如CuO+H2=Cu+H2O中,Cu降价总数为2,一个H升1价,1个H2总共升1×2价。

①实验装置连接的合理顺序为A、B、___________ 。
②能证明产物中有CO的现象是___________ 。
③除去SO2时,发生反应的化学方程式为___________ (已知产物中只有盐和酸)。
(3)G装置中去掉一个洗气瓶后仍然可以达到实验目的,则可以去掉的洗气瓶为___________ (填“①”、“②”或“③”);去掉该洗气瓶后证明SO2已除尽的现象为___________ 。
(1)Na2SO4与焦炭反应的实验装置如下图所示:

①先通入N2,然后加热,直至反应结束,整个过程中N2的作用是
②装置B的作用是
(2)该小组推测气体产物中含有CO2、CO及SO2,并进行验证。选用上述实验中的装置A、B和下图所示的部分装置(可以重复选用)进行实验。经过查找资料,得到如下信息:
a.SO2与碱的反应和CO2与碱的反应类似;
b.SO2可以使品红溶液褪色,该反应可用来检验SO2;
c.KMnO4可以被SO2还原成Mn2+;
d.氧化还原反应中化合价发生变化的元素,化合价升降总数相等,例如CuO+H2=Cu+H2O中,Cu降价总数为2,一个H升1价,1个H2总共升1×2价。

①实验装置连接的合理顺序为A、B、
②能证明产物中有CO的现象是
③除去SO2时,发生反应的化学方程式为
(3)G装置中去掉一个洗气瓶后仍然可以达到实验目的,则可以去掉的洗气瓶为
您最近半年使用:0次
名校
解题方法
6 . 甲、乙两同学为探究SO2与可溶性钡的强酸盐能否反应生成白色BaSO3沉淀,用下图所示装置进行实验(夹持装置和A中加热装置已略,气密性已检验)
已知:在酸性条件下硝酸根离子具有氧化性。
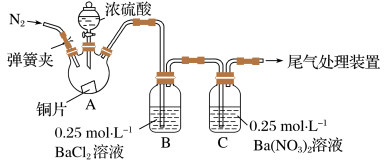
实验操作和现象:
(1)A中反应的化学方程式是___________ 。
(2)C中白色沉淀是___________ (填化学式,下同)。
(3)分析B中不溶于稀盐酸的沉淀产生的原因,甲认为是空气参与反应,乙认为是白雾参与反应。
①为证实各自的观点,在原实验基础上:甲在原有操作之前增加一步操作,该操作是___________ ;乙在A、B间增加洗气瓶D,D中盛放的试剂是___________ 。
②进行实验,B中现象:
检验白色沉淀,发现均不溶于稀盐酸,请写出乙中产生少量白色沉淀的离子方程式:___________ 。
(4)合并(3)中两同学的方案进行试验。B中无沉淀生成,而C中产生白色沉淀,根据甲、乙同学的实验目的可得出的结论是___________ 。
已知:在酸性条件下硝酸根离子具有氧化性。

实验操作和现象:
| 操作 | 现象 |
| 关闭弹簧夹,滴加一定量浓硫酸,加热 | A中有白雾生成,铜片表面产生气泡 B中有气泡冒出,产生大量白色沉淀 C中产生白色沉淀,液面上方略显浅棕色并逐渐消失 |
| 打开弹簧夹,通入N2,停止加热,一段时间后关闭 | |
| 从B、C中分别取少量白色沉淀,加稀盐酸 | 尚未发现白色沉淀溶解 |
(1)A中反应的化学方程式是
(2)C中白色沉淀是
(3)分析B中不溶于稀盐酸的沉淀产生的原因,甲认为是空气参与反应,乙认为是白雾参与反应。
①为证实各自的观点,在原实验基础上:甲在原有操作之前增加一步操作,该操作是
②进行实验,B中现象:
| 甲 | 大量白色沉淀 |
| 乙 | 少量白色沉淀 |
(4)合并(3)中两同学的方案进行试验。B中无沉淀生成,而C中产生白色沉淀,根据甲、乙同学的实验目的可得出的结论是
您最近半年使用:0次
名校
解题方法
7 . 近年我国某些城市酸雨污染较为严重,主要是因为大量燃烧含硫量高的煤。
【实验目的】通过实验证明煤中含有碳元素和硫元素。
(1)查阅资料知,二氧化硫能使酸性高锰酸钾溶液褪色,该反应体现出SO2的___________ 性;
(2)根据上述资料,甲同学和丙同学分别设计实验方案进行探究。
【实验操作】甲同学进行了如图所示A、B两步实验。
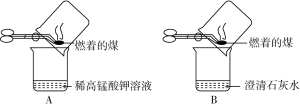
【实验现象】A中稀高锰酸钾溶液褪色,B中澄清石灰水变浑浊。
【得出结论】煤燃烧生成二氧化硫和二氧化碳,证明煤中含有碳元素和硫元素。
①乙同学认为甲同学的方案不合理,其理由是___________ 。
【实验操作】丙同学进行了如图所示实验。
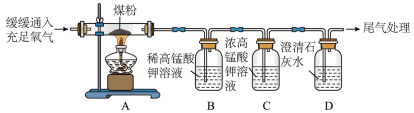
②C装置的作用是___________ ;
③证明煤中含有碳元素和硫元素的现象是___________ 。
④C装置中的浓高锰酸钾溶液也可以替换为___________ (填标号)。
A.足量I2的淀粉溶液 B.足量饱和NaHCO3溶液
C.足量NaHSO3溶液 D.足量溴水
【实验目的】通过实验证明煤中含有碳元素和硫元素。
(1)查阅资料知,二氧化硫能使酸性高锰酸钾溶液褪色,该反应体现出SO2的
(2)根据上述资料,甲同学和丙同学分别设计实验方案进行探究。
【实验操作】甲同学进行了如图所示A、B两步实验。

【实验现象】A中稀高锰酸钾溶液褪色,B中澄清石灰水变浑浊。
【得出结论】煤燃烧生成二氧化硫和二氧化碳,证明煤中含有碳元素和硫元素。
①乙同学认为甲同学的方案不合理,其理由是
【实验操作】丙同学进行了如图所示实验。

②C装置的作用是
③证明煤中含有碳元素和硫元素的现象是
④C装置中的浓高锰酸钾溶液也可以替换为
A.足量I2的淀粉溶液 B.足量饱和NaHCO3溶液
C.足量NaHSO3溶液 D.足量溴水
您最近半年使用:0次
8 . 实验室用浓硫酸、硝酸与铜丝反应探究物质性质和进行物质制备。
(1)回答实验甲问题:
① 试管中发生反应的化学方程式为
试管中发生反应的化学方程式为______ 。
② 中现象说明
中现象说明 具有
具有______ 作用。
③iv中制备 反应的离子方程式为
反应的离子方程式为______ 。
④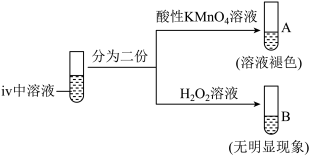
 中溶液褪色,说明
中溶液褪色,说明 具有
具有______ 性;B中无明显现象,某同学通过检测 的生成证明
的生成证明 和
和 发生了反应:取
发生了反应:取 中溶液于试管中,
中溶液于试管中,______ (填试剂和操作),产生白色沉淀。
(2)回答实验乙问题:
实验Ⅰ、Ⅱ中的红棕色气体均是 。
。
(1)实验Ⅰ产生 的化学方程式是
的化学方程式是______ 。
(2)实验Ⅱ产生 的化学方程式是
的化学方程式是______ 。
| 实验编号 | 实验目的 | 实验装置 | 操作及现象 |
| 甲 | 用浓硫酸与铜丝加热生成的 制备少量 制备少量 并检验性质 并检验性质 | 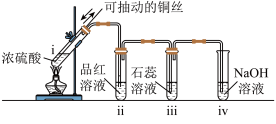 | 点燃酒精灯,i试管中有白雾生成,铜丝表面产生气泡;试管ii中溶液红色褪去,试管iii中溶液变红,一段时间后,将铜丝抽离硫酸并停止加热。 |
| 乙 | 探究铜与浓或稀硝酸反应 |  | (I)试剂a为4mL浓硝酸:铜片完全溶解,溶液变绿,出现大量红棕色气体。 (II)试剂a为4mL稀硝酸:铜片完全溶解,溶液变蓝,液面上方气体呈浅红棕色。 |
①
 试管中发生反应的化学方程式为
试管中发生反应的化学方程式为②
 中现象说明
中现象说明 具有
具有③iv中制备
 反应的离子方程式为
反应的离子方程式为④

 中溶液褪色,说明
中溶液褪色,说明 具有
具有 的生成证明
的生成证明 和
和 发生了反应:取
发生了反应:取 中溶液于试管中,
中溶液于试管中,(2)回答实验乙问题:
实验Ⅰ、Ⅱ中的红棕色气体均是
 。
。(1)实验Ⅰ产生
 的化学方程式是
的化学方程式是(2)实验Ⅱ产生
 的化学方程式是
的化学方程式是
您最近半年使用:0次
名校
9 . I.实验室可用如图装置(略去部分夹持仪器)制取SO2并验证其性质。
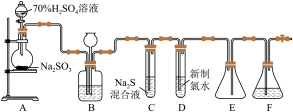
(1)盛装70% H2SO4溶液的仪器名称为___________ 。
(2)装置B的作用之一是通过观察产生气泡的多少判断SO2生成的快慢,其中的液体最好选择___________ (填代号)。
a.蒸馏水 b.饱和NaHCO3溶液 c.饱和NaHSO3溶液 d.饱和NaOH溶液
(3)C试管中的试剂可以验证二氧化硫的氧化性,现象为___________ 。
(4)为验证二氧化硫的还原性,充分反应后,取试管D中的溶液分成三份,分别进行如下实验:
方案Ⅰ:向第一份溶液中加入AgNO3溶液,有白色沉淀生成;
方案Ⅱ:向第二份溶液中加入品红溶液,红色褪去;
方案Ⅲ:向第三份溶液中加入BaCl2溶液,产生白色沉淀。
上述方案中能达到实验目的的是方案___________ (填“Ⅰ”“Ⅱ”或“Ⅲ”);试管D中发生反应的离子方程式为___________ 。
(5)装置E的作用是___________ 。装置F中为___________ 溶液。
(6)二氧化硫可作为食品添加剂。
查阅资料:国家食品添加剂使用标准中二氧化硫最大使用量如下表
说明在严格控制用量的情况下,二氧化硫可被添加到食品中作为漂白剂、防腐剂和___________ (填“氧化剂”或“抗氧化剂”)。
II.利用下图所示装置进行铜与硝酸反应的实验,得到的实验现象如下表:
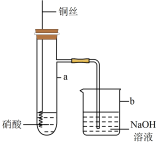
(7)组装好装置后进行实验之前需先进行___________ 。
(8)写出实验Ⅰ中产生的无色气体化学式___________ 。
(9)写出实验Ⅱ中铜与浓硝酸反应的离子方程式___________ 。
(10)装置中采用可拉动铜丝的优点是___________ (写一点)。
(11)针对Ⅰ中溶液呈蓝色,Ⅱ中溶液呈绿色。甲同学推测溶液的颜色与硝酸铜的质量分数有关,而乙同学推测Ⅱ中溶液呈绿色的原因是NO2在硝酸铜溶液中达到饱和所致。同学们分别设计了以下4个实验来判断两种看法是否正确。这些方案中可行的是___________。

(1)盛装70% H2SO4溶液的仪器名称为
(2)装置B的作用之一是通过观察产生气泡的多少判断SO2生成的快慢,其中的液体最好选择
a.蒸馏水 b.饱和NaHCO3溶液 c.饱和NaHSO3溶液 d.饱和NaOH溶液
(3)C试管中的试剂可以验证二氧化硫的氧化性,现象为
(4)为验证二氧化硫的还原性,充分反应后,取试管D中的溶液分成三份,分别进行如下实验:
方案Ⅰ:向第一份溶液中加入AgNO3溶液,有白色沉淀生成;
方案Ⅱ:向第二份溶液中加入品红溶液,红色褪去;
方案Ⅲ:向第三份溶液中加入BaCl2溶液,产生白色沉淀。
上述方案中能达到实验目的的是方案
(5)装置E的作用是
(6)二氧化硫可作为食品添加剂。
查阅资料:国家食品添加剂使用标准中二氧化硫最大使用量如下表
| 食品名称 | 食糖 | 葡萄酒 | 水果干类 |
| SO2最大使用量 | 0.1g•kg-1 | 0.25g•kg-1 | 1g•kg-1 |
II.利用下图所示装置进行铜与硝酸反应的实验,得到的实验现象如下表:

| 序号 | 实验试剂(20℃) | 实验现象 |
| Ⅰ | 铜丝、2mL稀硝酸 | 铜丝逐渐变细,有气泡产生,a中先产生无色气体后略有红棕色,溶液变蓝 |
| Ⅱ | 铜丝、2mL浓硝酸 | 反应剧烈,铜丝逐渐变细,a中上方出现红棕色气体,溶液变绿 |
(8)写出实验Ⅰ中产生的无色气体化学式
(9)写出实验Ⅱ中铜与浓硝酸反应的离子方程式
(10)装置中采用可拉动铜丝的优点是
(11)针对Ⅰ中溶液呈蓝色,Ⅱ中溶液呈绿色。甲同学推测溶液的颜色与硝酸铜的质量分数有关,而乙同学推测Ⅱ中溶液呈绿色的原因是NO2在硝酸铜溶液中达到饱和所致。同学们分别设计了以下4个实验来判断两种看法是否正确。这些方案中可行的是___________。
| A.加热绿色溶液,观察颜色变化 |
| B.加水稀释绿色溶液,观察颜色变化 |
| C.向绿色溶液中通入氮气,观察颜色变化 |
| D.向饱和硝酸铜溶液中通入浓硝酸与铜反应产生的气体,观察颜色变化 |
您最近半年使用:0次
名校
解题方法
10 . 根据要求完成下列各小题实验目的。a、b为弹簧夹,(加热及固定装置已略去)
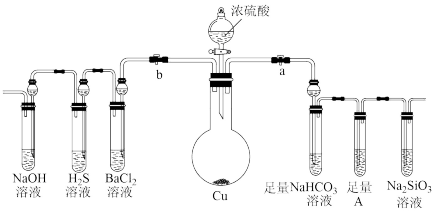
(1)验证碳、硅非金属性的相对强弱。(已知酸性:亚硫酸>碳酸)
①连接仪器、_______ 、加药品后,打开a关闭b,打开分液漏斗旋转活塞,然后滴入浓硫酸,发现硫酸滴入几滴,就不再滴下,原因是_______ ,当顺利滴入时加热。
②铜与浓硫酸反应的化学方程式是_______ 。装置A中试剂可以是_______ 。(用a,b,c填空)
a.品红溶液 b.氢氧化钠溶液 c.酸性高锰酸钾溶液
③能说明碳的非金属性比硅强的实验现象是_______ 。
(2)验证 的氧化性、还原性和酸性氧化物的通性。
的氧化性、还原性和酸性氧化物的通性。
①在(1)操作后打开b,关闭a。
②一段时间后, 溶液中的现象是
溶液中的现象是_______ ,化学方程式是_______ 。
(3) 溶液中无明显现象,将其分成两份,分别滴加下列溶液,将产生的沉淀的化学式填入下表相应位置。
溶液中无明显现象,将其分成两份,分别滴加下列溶液,将产生的沉淀的化学式填入下表相应位置。

(1)验证碳、硅非金属性的相对强弱。(已知酸性:亚硫酸>碳酸)
①连接仪器、
②铜与浓硫酸反应的化学方程式是
a.品红溶液 b.氢氧化钠溶液 c.酸性高锰酸钾溶液
③能说明碳的非金属性比硅强的实验现象是
(2)验证
 的氧化性、还原性和酸性氧化物的通性。
的氧化性、还原性和酸性氧化物的通性。①在(1)操作后打开b,关闭a。
②一段时间后,
 溶液中的现象是
溶液中的现象是(3)
 溶液中无明显现象,将其分成两份,分别滴加下列溶液,将产生的沉淀的化学式填入下表相应位置。
溶液中无明显现象,将其分成两份,分别滴加下列溶液,将产生的沉淀的化学式填入下表相应位置。| 滴加的溶液 | 氯水 | 氨水 |
| 沉淀的化学式 |
您最近半年使用:0次
2023-01-21更新
|
371次组卷
|
2卷引用:吉林省长春市第十一高中2022-2023高一上学期期末考试化学试题



