解题方法
1 . 硫酸亚铁可用于治疗缺铁性贫血症。某兴趣小组为探究硫酸亚铁的分解产物,设计实验方案如下:
①先按要求搭配好装置再检查装置的气密性;
②打开弹簧夹K1和K2,向装置中缓缓通入N2一段时间后,加热装有15.20g FeSO4的硬质玻璃管;
③观察到的实验现象:A装置中有红棕色固体出现,B中有白色沉淀生成,C中品红溶液褪色;
④冷却后A装置中剩余固体的质量为10.88g。
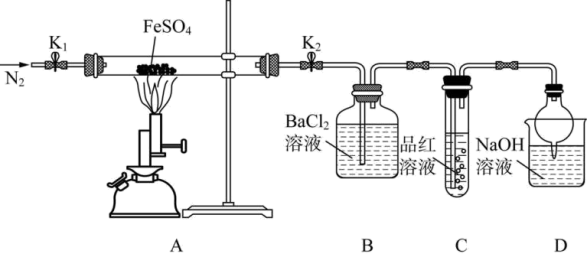
(1)根据B装置中的实验现象可推测分解产物中含有______ 。
(2)将装置B、C顺序颠倒能否达到原来的实验目的___ (填“能”或“不能”),原因是___ 。
(3)D装置中发生的主要反应的化学方程式是______ 。
(4)通过计算确定已分解的FeSO4物质的量,写出计算过程_______ 。
①先按要求搭配好装置再检查装置的气密性;
②打开弹簧夹K1和K2,向装置中缓缓通入N2一段时间后,加热装有15.20g FeSO4的硬质玻璃管;
③观察到的实验现象:A装置中有红棕色固体出现,B中有白色沉淀生成,C中品红溶液褪色;
④冷却后A装置中剩余固体的质量为10.88g。

(1)根据B装置中的实验现象可推测分解产物中含有
(2)将装置B、C顺序颠倒能否达到原来的实验目的
(3)D装置中发生的主要反应的化学方程式是
(4)通过计算确定已分解的FeSO4物质的量,写出计算过程
您最近一年使用:0次
名校
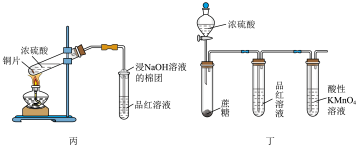
2 . 某化学兴趣小组为探究 和
和 的性质,按如图所示装置进行实验(省略部分夹持装置)。
的性质,按如图所示装置进行实验(省略部分夹持装置)。
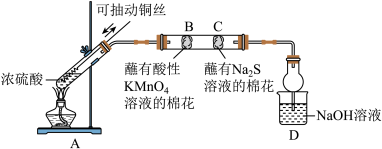
回答下列问题:
(1)A中发生反应的化学方程式为___________ 。
(2)使用可抽动铜丝的优点是___________ 。
(3)B处的实验现象是___________ ,由此推测硫元素从 价变为
价变为 价。
价。
(4)C处观察到蘸有 溶液的棉花上出现黄色固体,该反应的氧化剂为
溶液的棉花上出现黄色固体,该反应的氧化剂为______ (填化学式)。
(5)D装置的作用是___________ 。
(6)将A中产生的气体通入 溶液中,生成的白色沉淀为
溶液中,生成的白色沉淀为___________ (填化学式)。
(7)探究 的酸性强于
的酸性强于 ,该小组同学用下图所示装置达成实验目的。
,该小组同学用下图所示装置达成实验目的。
a. b.
b. c.
c. d.
d.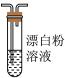
装置的连接顺序为:纯净SO2→___________ (填标号)。
(8)SO2也可用 和浓硫酸反应制得,该制备反应
和浓硫酸反应制得,该制备反应___________ (填“是”或“不是”)氧化还原反应。
 和
和 的性质,按如图所示装置进行实验(省略部分夹持装置)。
的性质,按如图所示装置进行实验(省略部分夹持装置)。
回答下列问题:
(1)A中发生反应的化学方程式为
(2)使用可抽动铜丝的优点是
(3)B处的实验现象是
 价变为
价变为 价。
价。(4)C处观察到蘸有
 溶液的棉花上出现黄色固体,该反应的氧化剂为
溶液的棉花上出现黄色固体,该反应的氧化剂为(5)D装置的作用是
(6)将A中产生的气体通入
 溶液中,生成的白色沉淀为
溶液中,生成的白色沉淀为(7)探究
 的酸性强于
的酸性强于 ,该小组同学用下图所示装置达成实验目的。
,该小组同学用下图所示装置达成实验目的。a.
 b.
b. c.
c. d.
d.
装置的连接顺序为:纯净SO2→
(8)SO2也可用
 和浓硫酸反应制得,该制备反应
和浓硫酸反应制得,该制备反应
您最近一年使用:0次
解题方法
3 . 实验室可用如下装置(略去部分夹持仪器)制取SO2并验证其性质.
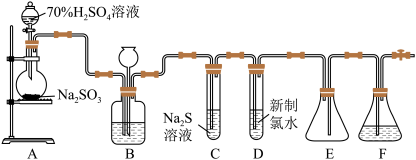
(1)盛装硫酸的仪器名称为_____________ ,若将亚硫酸钠改为铜片制取二氧化硫,还缺少的仪器是_______________ ,用铜片制取二氧化硫的化学方程式_______________ 。
(2)装置B的作用之一是通过观察产生气泡的多少判断SO2生成的快慢,其中的液体最好选择___________ (填代号)。
a.饱和Na2CO3溶液 b.饱和Na2SO3溶液
c.饱和NaHCO3溶液 d.饱和NaHSO3溶液
(3)验证二氧化硫的氧化性的装置是__________ ,现象为____________ 。
(4)充分反应后,取试管D中的溶液分成三份,分别进行如下实验:
方案I:向第一份溶液中加入AgNO3溶液,有白色沉淀生成;
方案Ⅱ:向第二份溶液中加入品红溶液,红色褪去;
方案Ⅲ:向第三份溶液中加入BaCl2溶液,产生白色沉淀.
上述方案中能验证SO2具有还原性的是________ (填“I”、“Ⅱ”或“Ⅲ”);为达到实验目的,还可以将试管D中的新制氯水改为_______________ (填写试剂名称)
(5)装置E的作用是_______________ 。

(1)盛装硫酸的仪器名称为
(2)装置B的作用之一是通过观察产生气泡的多少判断SO2生成的快慢,其中的液体最好选择
a.饱和Na2CO3溶液 b.饱和Na2SO3溶液
c.饱和NaHCO3溶液 d.饱和NaHSO3溶液
(3)验证二氧化硫的氧化性的装置是
(4)充分反应后,取试管D中的溶液分成三份,分别进行如下实验:
方案I:向第一份溶液中加入AgNO3溶液,有白色沉淀生成;
方案Ⅱ:向第二份溶液中加入品红溶液,红色褪去;
方案Ⅲ:向第三份溶液中加入BaCl2溶液,产生白色沉淀.
上述方案中能验证SO2具有还原性的是
(5)装置E的作用是
您最近一年使用:0次
名校
解题方法
4 . 硅酸是不溶于水的白色固体。硫酸是中学阶段常见的强酸之一,实验小组同学利用硫酸进行下列实验,下列实验操作不能达到实验目的的是
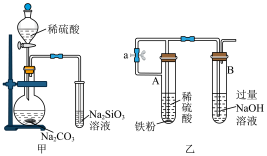


A.装置甲:验证非金属性: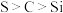 |
B.装置乙:制备 |
| C.装置丙:向铜与浓硫酸反应后的溶液中直接加水,可观察到溶液呈蓝色 |
D.装置丁:验证浓硫酸具有脱水性、强氧化性, 具有漂白性、还原性 具有漂白性、还原性 |
您最近一年使用:0次
2023-05-04更新
|
378次组卷
|
3卷引用:江西省宜丰中学2022-2023学年高二下学期7月期末考试化学试题
5 . 用如图所示的装置进行实验(夹持仪器略去,必要时可加热),能达到相应实验目的的是
| 选项 | a | b | c | 实验目的 | 装置 |
| A | 浓氨水 | 生石灰 | 浓硫酸 | 制备并干燥氨气 |  |
| B | 浓HNO3 | Cu片 | KI淀粉溶液 | 验证NO2的氧化性 | |
| C | 稀硫酸 | 溶液X | 澄清石灰水 | 验证X中是否有CO | |
| D | 70%硫酸 | Na2SO3 | 品红溶液 | 验证SO2具有漂白性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
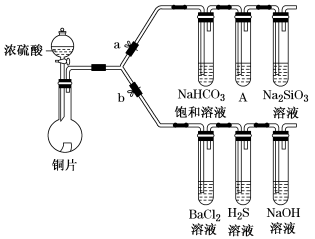
6 . 根据要求完成下列各小题实验目的。(a、b为弹簧夹,加热及固定装置已略去)
① 连接仪器、________ 、加药品后,打开a关闭b,然后滴入浓硫酸,加热。
② 铜与浓硫酸反应的化学方程式是_______ 。装置A中试剂是_______ 。
③ 能说明碳的非金属性比硅强的实验现象是_________ 。
(2)验证SO2的氧化性、还原性和酸性氧化物的通性。
① 在(1)①操作后打开b,关闭a。
② H2S溶液中有浅黄色浑浊出现,化学方程式是____ 。
③ BaCl2溶液中无明显现象,将其分成两份,分别滴加下列溶液,将产生的沉淀的化学式填入下表相应位置。
写出其中SO2显示还原性生成沉淀的离子方程式_________ 。
① 连接仪器、
② 铜与浓硫酸反应的化学方程式是
③ 能说明碳的非金属性比硅强的实验现象是
(2)验证SO2的氧化性、还原性和酸性氧化物的通性。
① 在(1)①操作后打开b,关闭a。
② H2S溶液中有浅黄色浑浊出现,化学方程式是
③ BaCl2溶液中无明显现象,将其分成两份,分别滴加下列溶液,将产生的沉淀的化学式填入下表相应位置。
| 滴加的溶液 | 氯水 | 氨水 |
| 沉淀的化学式 |
您最近一年使用:0次
2020-03-06更新
|
145次组卷
|
5卷引用:河南省郑州市第一中学2018-2019学年高二上学期入学测试化学试题
名校
解题方法
7 . 下列装置能达到相应实验目的的是
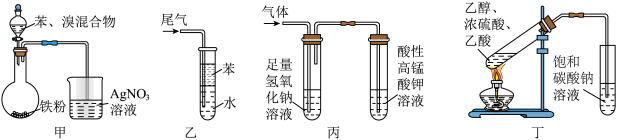

A.利用甲装置可制备溴苯并验证有 生成 生成 | B.利用乙装置可吸收 并防倒吸 并防倒吸 |
C.利用丙装置可检验含有 杂质的乙烯 杂质的乙烯 | D.利用丁装置可制备并收集乙酸乙酯 |
您最近一年使用:0次
解题方法
8 . 化学是一门以实验为基础的学科。用下列实验装置进行相应实验,能达到实验目的的是
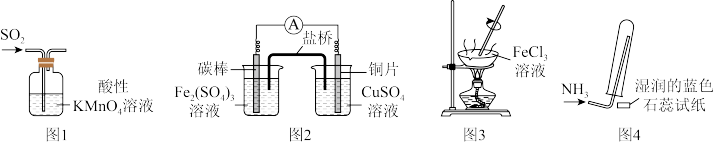

A.图1装置可验证 的漂白性 的漂白性 |
B.图2装置可验证氧化性: |
C.图3装置可制备无水 |
| D.图4装置可验证氨水呈碱性 |
您最近一年使用:0次
9 . CuSO4常用作农业杀菌剂、分析试剂、媒染剂和防腐剂等。实验室利用废铜屑制备CuSO4有三种途径:一是将废铜屑与浓硫酸共热,此方法会产生污染性气体SO2;二是先将废铜屑加热氧化成CuO,然后再用稀硫酸溶解,该方法耗能较多;三是在常温下用H2O2和H2SO4的混合溶液浸取废铜屑获得CuSO4,该方法绿色环保且节能,反应为Cu(s)+ H2O2(l) + 2H+ (aq)= Cu2+(aq)+ 2H2O(1) ΔH =-319.68 kJ·mol-1。实验室利用废铜屑与浓硫酸反应制备CuSO4并进行有关实验时,下列装置能达到相应实验目的的是
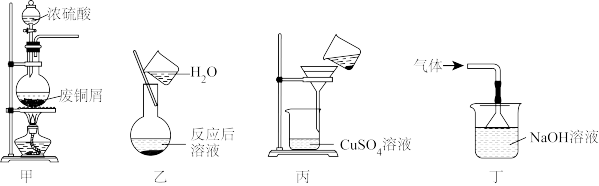

| A.用装置甲制取CuSO4 |
| B.用装置乙观察CuSO4溶液的颜色 |
| C.用装置丙过滤得到CuSO4溶液。 |
| D.用装置丁吸收多余的SO2 |
您最近一年使用:0次
名校
10 . 实验室制备SO2时,下列装置能达到相应实验目的的是
A. 生成SO2 生成SO2 | B.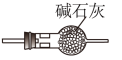 干燥SO2 干燥SO2 |
C. 收集SO2 收集SO2 | D. 吸收SO2尾气 吸收SO2尾气 |
您最近一年使用:0次
2021-02-27更新
|
669次组卷
|
3卷引用:江苏省溧水高级中学2020-2021学年高二下学期4月调研化学试题



