名校
解题方法
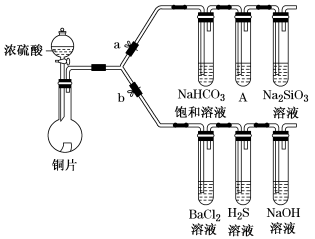
1 . 根据要求完成下列各小题实验目的。(a、b为弹簧夹,加热及固定装置已略去)
① 连接仪器、________ 、加药品后,打开a关闭b,然后滴入浓硫酸,加热。
② 铜与浓硫酸反应的化学方程式是_______ 。装置A中试剂是_______ 。
③ 能说明碳的非金属性比硅强的实验现象是_________ 。
(2)验证SO2的氧化性、还原性和酸性氧化物的通性。
① 在(1)①操作后打开b,关闭a。
② H2S溶液中有浅黄色浑浊出现,化学方程式是____ 。
③ BaCl2溶液中无明显现象,将其分成两份,分别滴加下列溶液,将产生的沉淀的化学式填入下表相应位置。
写出其中SO2显示还原性生成沉淀的离子方程式_________ 。
① 连接仪器、
② 铜与浓硫酸反应的化学方程式是
③ 能说明碳的非金属性比硅强的实验现象是
(2)验证SO2的氧化性、还原性和酸性氧化物的通性。
① 在(1)①操作后打开b,关闭a。
② H2S溶液中有浅黄色浑浊出现,化学方程式是
③ BaCl2溶液中无明显现象,将其分成两份,分别滴加下列溶液,将产生的沉淀的化学式填入下表相应位置。
| 滴加的溶液 | 氯水 | 氨水 |
| 沉淀的化学式 |
您最近一年使用:0次
2020-03-06更新
|
147次组卷
|
6卷引用:河南省郑州市第一中学2018-2019学年高二上学期入学测试化学试题
名校
解题方法
2 . 某化学兴趣小组在实验室中利用下图装置制备SO2并进行相关性质的探究。回答下列问题:

I.A与B相连时
(1)滴加浓硫酸之前,先通一段时间的N2,目的是
(2)装置A中反应的化学方程式是
(3)通入足量SO2后②中仍无明显现象,将其分成甲、乙两份,甲中加入氯水,乙中加入氨水,均产生白色沉淀。产生沉淀的化学式是:甲
Ⅱ.A与C相连时,可用来探究碳、硅元素的非金属性的相对强弱。
(4)装置⑤的作用为
您最近一年使用:0次
2023-05-11更新
|
84次组卷
|
2卷引用:河南省济源高级中学2023-2024学年高二上学期开学考试 化学试题
名校
解题方法
3 . 摩尔盐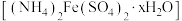 比一般的亚铁盐更稳定,是一种重要的定量分析化学试剂。回答下列问题:
比一般的亚铁盐更稳定,是一种重要的定量分析化学试剂。回答下列问题:
(1)制备摩尔盐采用的方法是先在封闭体系中利用铁和稀硫酸反应制备硫酸亚铁溶液,再用新制的硫酸亚铁溶液和硫酸按饱和溶液反应制得。配制硫酸按饱和溶液的蒸馏水,需经煮沸并迅速冷却后再使用,目的是___________ 。
(2)可以采用热重分析法测定摩尔盐样品中所含结晶水的个数,加热其晶体需要使用的实验仪器除了玻璃棒、三脚架、泥三角、酒精灯外,还需要的仪器有___________ 。取样品 加热至两次质量恒重为
加热至两次质量恒重为 (假设减少的质量仅仅是晶体失水),则x的表达式为
(假设减少的质量仅仅是晶体失水),则x的表达式为___________ (用含a、b的代数式表示)。
(3)利用摩尔盐分解产生的 ,可制取氯化亚砜
,可制取氯化亚砜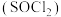 :
: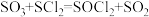 。已知
。已知 是一种液态化合物,遇水产生白雾和一种刺激性气体。利用如图装置制取
是一种液态化合物,遇水产生白雾和一种刺激性气体。利用如图装置制取 并检验生成的
并检验生成的 。
。
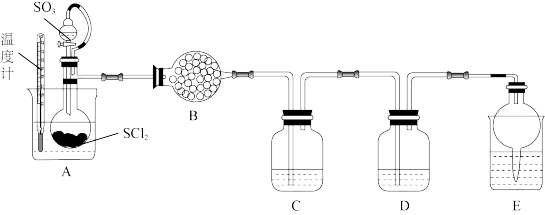
①装置B为无水 ,其作用是
,其作用是___________ 。
②装置C和装置D中的试剂分别是___________ 、___________ (填小写字母)。
a. 溶液 b.
溶液 b. 和
和 溶液 c.
溶液 c. 溶液 d.饱和的
溶液 d.饱和的 溶液
溶液
(4)利用摩尔盐分解产生的 ,设计实验探究亚硫酸与次氯酸的酸性强弱。
,设计实验探究亚硫酸与次氯酸的酸性强弱。
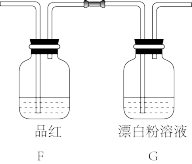
①将少量 气体直接通入装置G中,不能根据装置G中现象判断亚硫酸与次氯酸的酸性强弱,理由是
气体直接通入装置G中,不能根据装置G中现象判断亚硫酸与次氯酸的酸性强弱,理由是___________ (用化学反应方程式表示)。
②为了验证亚硫酸与次氯酸的酸性强弱,需要制备一种中间酸,装置F中另一种试剂是___________ ,其作用是___________ ,通过___________ (填现象)即可证明亚硫酸的酸性强于次氯酸。
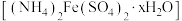 比一般的亚铁盐更稳定,是一种重要的定量分析化学试剂。回答下列问题:
比一般的亚铁盐更稳定,是一种重要的定量分析化学试剂。回答下列问题:(1)制备摩尔盐采用的方法是先在封闭体系中利用铁和稀硫酸反应制备硫酸亚铁溶液,再用新制的硫酸亚铁溶液和硫酸按饱和溶液反应制得。配制硫酸按饱和溶液的蒸馏水,需经煮沸并迅速冷却后再使用,目的是
(2)可以采用热重分析法测定摩尔盐样品中所含结晶水的个数,加热其晶体需要使用的实验仪器除了玻璃棒、三脚架、泥三角、酒精灯外,还需要的仪器有
 加热至两次质量恒重为
加热至两次质量恒重为 (假设减少的质量仅仅是晶体失水),则x的表达式为
(假设减少的质量仅仅是晶体失水),则x的表达式为(3)利用摩尔盐分解产生的
 ,可制取氯化亚砜
,可制取氯化亚砜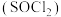 :
: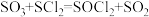 。已知
。已知 是一种液态化合物,遇水产生白雾和一种刺激性气体。利用如图装置制取
是一种液态化合物,遇水产生白雾和一种刺激性气体。利用如图装置制取 并检验生成的
并检验生成的 。
。
①装置B为无水
 ,其作用是
,其作用是②装置C和装置D中的试剂分别是
a.
 溶液 b.
溶液 b. 和
和 溶液 c.
溶液 c. 溶液 d.饱和的
溶液 d.饱和的 溶液
溶液(4)利用摩尔盐分解产生的
 ,设计实验探究亚硫酸与次氯酸的酸性强弱。
,设计实验探究亚硫酸与次氯酸的酸性强弱。
①将少量
 气体直接通入装置G中,不能根据装置G中现象判断亚硫酸与次氯酸的酸性强弱,理由是
气体直接通入装置G中,不能根据装置G中现象判断亚硫酸与次氯酸的酸性强弱,理由是②为了验证亚硫酸与次氯酸的酸性强弱,需要制备一种中间酸,装置F中另一种试剂是
您最近一年使用:0次
2022-07-15更新
|
303次组卷
|
2卷引用:河南省开封市五县2021-2022学年高二下学期期末考试化学试题
4 . 某课题组设计实验探究SO2的性质。
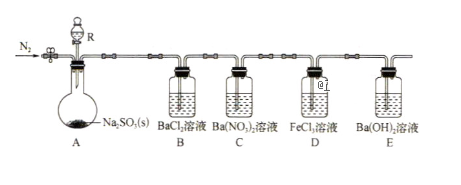
实验现象:B中无沉淀生成,C中有白色沉淀,D中溶液颜色变浅,E中产生白色沉淀.
(1)仪器R的名称是__________ .
(2)实验室在常温下用80%的硫酸与亚硫酸钠粉末反应制备SO2,写出A中反应的化学方程式:__________ .
(3)部分实验步骤如下:连接装置、检查气密性、装药品,向装置中通入一段时间N2,然后启动A中反应。“通入一段时间的N2"的目的是____ .
(4)探究装置C中通入SO2的量与产物的关系。
①他们提出如下猜想:
猜想1:通入过量的SO2,则发生反应的离子方程式为Ba2++2NO3-+3SO2+2H2O=BaSO4+2SO42-+2NO+4H+
猜想2:通入少量的SO2,则发生反应的离子方程式为__________ 。
② 请你帮他们设计实验证明猜想1和猜想2哪个合理,完成下列实验:
提供试剂:溴水、铜粉、Ba(NO3)2溶液、BaCl2溶液、Na2CO3溶液
(5)下列可检验装置D反应后溶液中是否有Fe2+的最佳试剂是(填字母)( )
A.KSCN溶液B.NaOH溶液C.K3[Fe(CN)6]溶液D.KSCN溶液和双氧水
(6)常温下,实验完毕后,分离、提纯装置E中白色固体M,取适量M于试管中,滴少量盐酸(M剩余),所得溶液的pH__________ 7(填“>”“<”或“=”)。

实验现象:B中无沉淀生成,C中有白色沉淀,D中溶液颜色变浅,E中产生白色沉淀.
(1)仪器R的名称是
(2)实验室在常温下用80%的硫酸与亚硫酸钠粉末反应制备SO2,写出A中反应的化学方程式:
(3)部分实验步骤如下:连接装置、检查气密性、装药品,向装置中通入一段时间N2,然后启动A中反应。“通入一段时间的N2"的目的是
(4)探究装置C中通入SO2的量与产物的关系。
①他们提出如下猜想:
猜想1:通入过量的SO2,则发生反应的离子方程式为Ba2++2NO3-+3SO2+2H2O=BaSO4+2SO42-+2NO+4H+
猜想2:通入少量的SO2,则发生反应的离子方程式为
② 请你帮他们设计实验证明猜想1和猜想2哪个合理,完成下列实验:
提供试剂:溴水、铜粉、Ba(NO3)2溶液、BaCl2溶液、Na2CO3溶液
| 实验步骤 | 实验现象及结论 |
| 取少量C中反应后溶液于试管中, |
A.KSCN溶液B.NaOH溶液C.K3[Fe(CN)6]溶液D.KSCN溶液和双氧水
(6)常温下,实验完毕后,分离、提纯装置E中白色固体M,取适量M于试管中,滴少量盐酸(M剩余),所得溶液的pH
您最近一年使用:0次
2017-05-13更新
|
200次组卷
|
3卷引用:河南省新乡市延津县高级中学2016-2017学年高二(卫星班)下学期期末考试理综化学试题
河南省新乡市延津县高级中学2016-2017学年高二(卫星班)下学期期末考试理综化学试题(已下线)解密06 非金属及其化合物(教师版)——备战2018年高考化学之高频考点解密山东省新泰市第二中学2019届高三上学期阶段性测试(三)理科综合化学试题
5 . 下列实验设计能达到实验目的的是
| 选项 | 实验目的 | 实验设计 |
| A | 除去 中的HCl 中的HCl | 通过饱和 溶液 溶液 |
| B | 检验溶液中是否含 | 取少量待检验溶液于试管中,加入浓NaOH溶液,加热,用湿润的红色石蕊试纸检验 |
| C | 检验次氯酸是否是弱酸 | 用pH试纸测定 溶液的pH 溶液的pH |
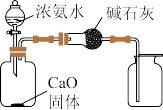
| D | 实验室制备少量 | 在浓氨水中加入石灰石 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
6 . 实验是学习化学的重要途径。下列装置或操作能达到实验目的的是
A | B | C | D |
|
|
|
|
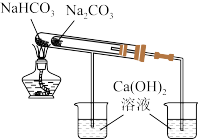
比较 和 和 的热稳定性 的热稳定性 | 验证浓硫酸的脱水性、强氧化性 的漂白性、还原性 的漂白性、还原性 | 制取并收集干燥纯净的 | 用氢氧化钠标准液测定盐酸的浓度 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-05-29更新
|
138次组卷
|
2卷引用:河南省部分学校2021-2022学年高二下学期5月联考化学试题
名校
解题方法
7 . 用如图所示装置进行下列实验,装置正确并能达到实验目的的是
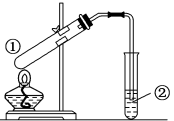

| 选项 | ①中试剂 | 2中溶液 | 实验目的 |
| A | 浓硫酸、无水乙醇(沸石) | 酸性高锰酸钾溶液 | 检验有乙烯气体生成 |
| B | Cu、浓硫酸 | 溴水 | 验证 的还原性 的还原性 |
| C | 乙醇、乙酸、浓硫酸 | 饱和碳酸钠溶液 | 制取乙酸乙酯 |
| D | 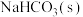 | 澄清石灰水 | 验证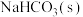 的热稳定性 的热稳定性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-05-31更新
|
463次组卷
|
5卷引用:河南省信阳高级中学2022-2023学年高二上学期期末考试化学试题
河南省信阳高级中学2022-2023学年高二上学期期末考试化学试题海南省海口市2022届高三学生学科能力诊断(二)化学试题(已下线)第九章 化学实验基础及综合实验(测)-2023年高考化学一轮复习讲练测(全国通用)黑龙江省牡丹江市第一高级中学2022-2023学年高三上学期期末考试化学试题(已下线)黑龙江省牡丹江市第一高级中学2022-2023学年高三上学期期末考试变式汇编(11-20)
8 . 下列实验装置或操作正确且能达到实验目的的是
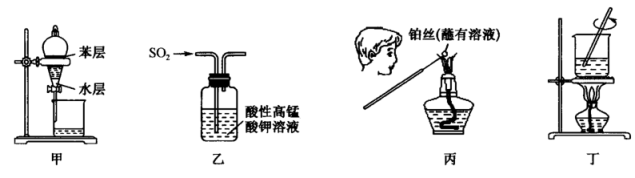

| A.用装置甲从碘水中萃取碘 |
B.用装置乙验证 的漂白性 的漂白性 |
C.用装置丙检验溶液中是否有 |
D.用装置丁从 溶液获得 溶液获得 固体 固体 |
您最近一年使用:0次
解题方法
9 . 利用下图装置和下表内的物质,进气方向正确,且能达到相应实验目的的是
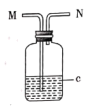

| 选项 | 实验目的 | c中的物质 | 进气方向 |
| A | 收集氨气 | 饱和 溶液 溶液 |  |
| B | 证明 具有漂白性 具有漂白性 | 溴水 |  |
| C | 除去 中的 中的 | 饱和 溶液 溶液 |  |
| D | 证明 具有氧化性 具有氧化性 |  溶液 溶液 |  |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
22-23高二下·陕西宝鸡·期末
名校
解题方法
10 . 硫酸是重要的化工原料,用于生产化肥、农药、炸药、染料和盐类等。
某实验小组采用下图装置模拟硫酸工业的接触室,并测定 催化氧化为
催化氧化为 的转化率。
的转化率。

已知:
(1)反应开始时,打开 ,关闭
,关闭 ,使
,使 和氧气一起通过装置
和氧气一起通过装置 进入
进入 中发生反应,反应后的气体进入装置
中发生反应,反应后的气体进入装置 ,装置
,装置 的作用为
的作用为___________ ;若将装置 换为如图所示装置,实验测得
换为如图所示装置,实验测得 的转化率会偏大,原因为
的转化率会偏大,原因为___________ (用化学反应方程式解释)。

(2)装置F中___________ 现象说明气体吸收完全。
(3)实验结束后的操作顺序为___________ (填序号)。
①待 充分反应后,熄灭
充分反应后,熄灭 处的酒精灯
处的酒精灯
②停止通入
③停止滴加浓硫酸,关闭 ,打开
,打开
(4)装置B中发生的离子反应方程式为___________ ,装置B中试剂可替换为___________ (填字母)。
A.水 B. 溶液
溶液
C. 溶液 D.饱和
溶液 D.饱和 溶液
溶液
(5)反应结束后测得装置 质量增加mg,装置
质量增加mg,装置 质量增加ng,则该条件下
质量增加ng,则该条件下 的转化率为
的转化率为___________ (用字母表示)。
某实验小组采用下图装置模拟硫酸工业的接触室,并测定
 催化氧化为
催化氧化为 的转化率。
的转化率。
已知:
 |  | |
| 熔点/℃ | 16.8 | -72.7 |
| 沸点/℃ | 44.8 | -10 |
 ,关闭
,关闭 ,使
,使 和氧气一起通过装置
和氧气一起通过装置 进入
进入 中发生反应,反应后的气体进入装置
中发生反应,反应后的气体进入装置 ,装置
,装置 的作用为
的作用为 换为如图所示装置,实验测得
换为如图所示装置,实验测得 的转化率会偏大,原因为
的转化率会偏大,原因为
(2)装置F中
(3)实验结束后的操作顺序为
①待
 充分反应后,熄灭
充分反应后,熄灭 处的酒精灯
处的酒精灯②停止通入

③停止滴加浓硫酸,关闭
 ,打开
,打开
(4)装置B中发生的离子反应方程式为
A.水 B.
 溶液
溶液C.
 溶液 D.饱和
溶液 D.饱和 溶液
溶液(5)反应结束后测得装置
 质量增加mg,装置
质量增加mg,装置 质量增加ng,则该条件下
质量增加ng,则该条件下 的转化率为
的转化率为
您最近一年使用:0次