名校
解题方法
1 . 二氧化硫是形成酸雨的主要气体。为了有效控制酸雨,目前国务院已批准了《酸雨控制区和二氧化硫污染控制区划分方案》等法规。现有雨水样品1份,每隔一段时间测定该雨水样品的pH,所得数据如下表:
(1)此雨水样品是否属于酸雨_______ (填是或否),pH值变小的主要原因是_______ (用化学方程式表示)。
(2)用氨水可以吸收SO2制取铵盐,用足量氨水吸收SO2的化学方程式为_______ 。
(3)下列措施不能达到二氧化硫减排目的的是_______。
(4)向品红溶液中通入SO2气体后红色消失,该反应中SO2表现出_______。
(5)如果将刚取样的上述雨水和自来水(含有余氯)相混合,酸性将变_______ (填“强”或“弱”),其原因是_______ (用化学方程式表示)。
(6)调查表明,氮氧化物也会造成酸雨。柴油机主要排放物为颗粒状物质和氮氧化合物,其中NO约占90%。SCR(选择性催化)技术可以利用尿素溶液热分解生成的NH3有效降低氮氧化合物的排放。_______ ,空气中氮气能够稳定存在的原因是_______ 。
(7)虽然NO2、SO2会形成酸雨,但是硫和氮及其化合物对人类生存和社会发展意义重大,下列说法正确的是_______。
| 测定时间(小时) | 0 | 1 | 2 | 4 | 8 |
| 雨水的pH值 | 4.73 | 4.62 | 4.56 | 4.55 | 4.55 |
(1)此雨水样品是否属于酸雨
(2)用氨水可以吸收SO2制取铵盐,用足量氨水吸收SO2的化学方程式为
(3)下列措施不能达到二氧化硫减排目的的是_______。
| A.燃料脱硫 | B.尾气除硫 | C.能源替代 | D.植树造林 |
(4)向品红溶液中通入SO2气体后红色消失,该反应中SO2表现出_______。
| A.还原性 | B.漂白性 | C.酸性 | D.氧化性 |
(5)如果将刚取样的上述雨水和自来水(含有余氯)相混合,酸性将变
(6)调查表明,氮氧化物也会造成酸雨。柴油机主要排放物为颗粒状物质和氮氧化合物,其中NO约占90%。SCR(选择性催化)技术可以利用尿素溶液热分解生成的NH3有效降低氮氧化合物的排放。

(7)虽然NO2、SO2会形成酸雨,但是硫和氮及其化合物对人类生存和社会发展意义重大,下列说法正确的是_______。
| A.雷雨天气有助于空气中的N2转化为可供植物吸收的HNO3 |
B.PM2.5(微粒直径约为 )含氮的分散质分散在空气中形成胶体,能产生丁达尔效应 )含氮的分散质分散在空气中形成胶体,能产生丁达尔效应 |
| C.二氧化硫有毒,严禁将其添加到任何食品和饮品中 |
| D.酸雨是由大气中的碳、氮、硫的氧化物溶于雨水造成的 |
您最近一年使用:0次
2022高一·上海·专题练习
解题方法
2 . 硫是生物必需的大量营养元素之一,下图是自然界中硫的循环图,在循环过程中价态变化在-2价至+6价之间,以不同的状态(或形态)发生一系列的变化,请分析此图并回答有关问题。
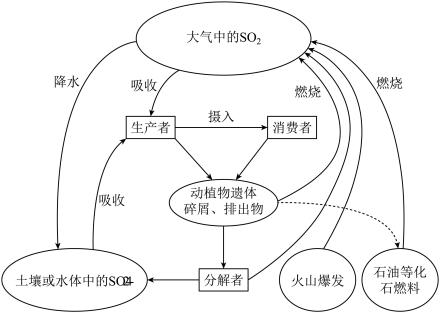
(1)分解者可将含硫有机物分解为硫化氢,硫黄细菌和硫化细菌可将硫化氢进一步转变为元素硫或硫酸盐,下列关于硫化氢说法正确的是_______
A.硫化氢分子很稳定,受热难分解
B.硫化氢分子中所有原子的最外层都达到8电子结构
C.将硫化氢通入硫酸亚铁溶液,产生沉淀
D.硫化氢中硫元素为-2价,因此只有还原性,没有氧化性
E.硫化氢是一种无色臭鸡蛋气味的有毒气体
(2)大气中的SO2经过一系列转化最终生成H2SO4,导致降水具有较强酸性,称为酸雨。收集某次酸雨样品,发现8小时内,样品pH一直在较小,其原因可能是_______ 。(用化学方程式表示)
(3)研究发现,空气其中少量的NO2也能参与硫酸型酸雨的形成,反应过程如下:
①SO2+NO2→SO3+NO
②SO3+H2O→H2SO4
③2NO+O2→2NO2
NO2在上述过程中的作用,与H2SO4在下列变化中的作用不同的是_______ 。
A.潮湿的氯气通过盛有浓H2SO4的洗气瓶
B.硫化氢通入浓H2SO4中
C.向盐酸中加入浓硫酸产生白雾
(4)为了防治酸雨,工业上常采用“钙基固硫法”即将生石灰和含硫的煤混合后燃烧,燃烧时硫、氧气和生石灰共同作用,使硫元素转移到炉渣中,大部分硫元素最终转化为固体盐是_______ 。
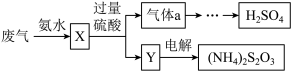
(5)若采用如图所示的流程处理则气体a是_______ ,Y一定含有_______ 。(填化学式)

(1)分解者可将含硫有机物分解为硫化氢,硫黄细菌和硫化细菌可将硫化氢进一步转变为元素硫或硫酸盐,下列关于硫化氢说法正确的是
A.硫化氢分子很稳定,受热难分解
B.硫化氢分子中所有原子的最外层都达到8电子结构
C.将硫化氢通入硫酸亚铁溶液,产生沉淀
D.硫化氢中硫元素为-2价,因此只有还原性,没有氧化性
E.硫化氢是一种无色臭鸡蛋气味的有毒气体
(2)大气中的SO2经过一系列转化最终生成H2SO4,导致降水具有较强酸性,称为酸雨。收集某次酸雨样品,发现8小时内,样品pH一直在较小,其原因可能是
(3)研究发现,空气其中少量的NO2也能参与硫酸型酸雨的形成,反应过程如下:
①SO2+NO2→SO3+NO
②SO3+H2O→H2SO4
③2NO+O2→2NO2
NO2在上述过程中的作用,与H2SO4在下列变化中的作用不同的是
A.潮湿的氯气通过盛有浓H2SO4的洗气瓶
B.硫化氢通入浓H2SO4中
C.向盐酸中加入浓硫酸产生白雾
(4)为了防治酸雨,工业上常采用“钙基固硫法”即将生石灰和含硫的煤混合后燃烧,燃烧时硫、氧气和生石灰共同作用,使硫元素转移到炉渣中,大部分硫元素最终转化为固体盐是
(5)若采用如图所示的流程处理则气体a是

您最近一年使用:0次
名校
解题方法
3 . 硫是生物必需的大量营养元素之一,下图是自然界中硫的循环图,请分析此图并回答有关问题。
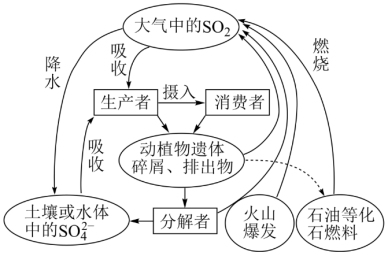
(1)氮循环和硫循环是自然界中两种重要的元素循环过程,下列关于这两种循环的说法正确的是________ 。
(2)分解者可将含硫有机物分解为H2S,硫磺细菌和硫化细菌可将H2S进一步变为硫单质或硫酸盐,下列关于硫化氢说法正确的是_______ 。
A.H2S分子很稳定,受热难分解
B. H2S分子中所有原子的最外层都达到8电子结构
C.将H2S通入FeSO4溶液,产生沉淀
D.H2S中硫元素为-2价,因此H2S只有还原性,没有氧化性
E.H2S是一种无色臭鸡蛋气味的有毒气体
(3)大气中的SO2经过一系列转化最终生成H2SO4,导致降水具有较强酸性,称为酸雨。检验某次降雨是否为酸雨的方法是_________________ ,收集某次酸雨样品,发现8小时内,样品pH一直在减小,其原因可能是________________ 。(用化学方程式表示)
(4)为了防治酸雨,工业上常采用“钙基固硫法”即将生石灰和含硫的煤混合后燃烧,燃烧时硫、氧气和生石灰共同作用,使硫元素转移到炉渣中,大部分硫元素最终转化为固体盐是_______ (填化学式)。

(1)氮循环和硫循环是自然界中两种重要的元素循环过程,下列关于这两种循环的说法正确的是
| 选项 | 比较 | 氮循环 | 硫循环 |
| A | 异 | 氮元素会进入大气 | 硫元素不会进入大气 |
| B | 氮循环过程有生物圈参与 | 硫循环过程无生物圈参与 | |
| C | 同 | 人类活动对氮循环和硫循环都造成巨大影响 | |
| D | 氮循环和硫循环对环境的影响是都能导致温室效应 | ||
A.H2S分子很稳定,受热难分解
B. H2S分子中所有原子的最外层都达到8电子结构
C.将H2S通入FeSO4溶液,产生沉淀
D.H2S中硫元素为-2价,因此H2S只有还原性,没有氧化性
E.H2S是一种无色臭鸡蛋气味的有毒气体
(3)大气中的SO2经过一系列转化最终生成H2SO4,导致降水具有较强酸性,称为酸雨。检验某次降雨是否为酸雨的方法是
(4)为了防治酸雨,工业上常采用“钙基固硫法”即将生石灰和含硫的煤混合后燃烧,燃烧时硫、氧气和生石灰共同作用,使硫元素转移到炉渣中,大部分硫元素最终转化为固体盐是
您最近一年使用:0次
解题方法
4 . 硫是生物必需的大量营养元素之一,下图是自然界中硫的循环图,在循环过程中价态变化在-2价至+6价之间,以不同的状态(或形态)发生一系列的变化,请分析此图并回答有关问题,
(1)硫循环与氮循环是自然界中两种重要的元素循环过程,下列关于这两种循环的说法正确的是_____
(2)分解者可将含硫有机物分解为硫化氢,硫黄细菌和硫化细菌可将硫化氢进一步转变为元素硫或硫酸盐,下列关于硫化氢说法正确的是_____________
A.硫化氢分子很稳定,受热难分解
B.硫化氢分子中所有原子的最外层都达到8电子结构
C.将硫化氢通入硫酸亚铁溶液,产生沉淀
D.硫化氢中硫元素为-2价,因此只有还原性,没有氧化性
E.硫化氢是一种无色臭鸡蛋气味的有毒气体
(3)硫化氢虽然有毒,但有研究发现人体心肺血管中存在微量硫化氢,它对调节心血管功能具有重要作用,请再举出一例类似硫化氢“亦正亦邪”物质的实证______________________ 。
(4)大气中的SO2经过一系列转化最终生成H2SO4,导致降水具有较强酸性,称为酸雨。收集某次酸雨样品,发现8小时内,样品pH一直在较小,其原因可能是_____________________ 。(用化学方程式表示)
(5)研究发现,空气其中少量的NO2也能参与硫酸型酸雨的形成,反应过程如下:
①SO2+NO2→SO3+NO ②SO3+H2O→H2SO4 ③2NO+O2→2NO2
NO2在上述过程中的作用,与H2SO4在下列变化中的作用不符的是___________ (多选)
A.潮湿的氯气通过盛有浓H2SO4的洗气瓶
B.硫化氢通入浓H2SO4中
C.浓H2SO4滴入萤石中,加热
D.向盐酸中加入浓硫酸产生白雾
(6)为了防治酸雨,工业上常采用“钙基固硫法”即将生石灰和含硫的煤混合后燃烧,燃烧时硫、氧气和生石灰共同作用,使硫元素转移到炉渣中,大部分硫元素最终转化为固体盐是_______ 。
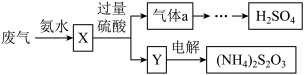
(7)若采用如图所示的流程处理则气体a是_______________ ,Y一定含有______________ 。(填化学式)
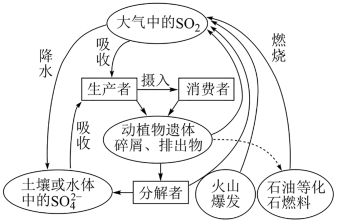
(1)硫循环与氮循环是自然界中两种重要的元素循环过程,下列关于这两种循环的说法正确的是
| 选项 | 比较 | 氮循环 | 硫循环 |
| A | 异 | 氮元素会进入大气 | 硫元素不会进入大气 |
| B | 碳循环过程有生物圈参与 | 硫循环过程无生物圈参与 | |
| C | 同 | 人类活动对氮循环和硫循环都造成巨大影响 | |
| D | 氮循环和硫循环对环境的影响是都能导致温室效应 | ||
(2)分解者可将含硫有机物分解为硫化氢,硫黄细菌和硫化细菌可将硫化氢进一步转变为元素硫或硫酸盐,下列关于硫化氢说法正确的是
A.硫化氢分子很稳定,受热难分解
B.硫化氢分子中所有原子的最外层都达到8电子结构
C.将硫化氢通入硫酸亚铁溶液,产生沉淀
D.硫化氢中硫元素为-2价,因此只有还原性,没有氧化性
E.硫化氢是一种无色臭鸡蛋气味的有毒气体
(3)硫化氢虽然有毒,但有研究发现人体心肺血管中存在微量硫化氢,它对调节心血管功能具有重要作用,请再举出一例类似硫化氢“亦正亦邪”物质的实证
(4)大气中的SO2经过一系列转化最终生成H2SO4,导致降水具有较强酸性,称为酸雨。收集某次酸雨样品,发现8小时内,样品pH一直在较小,其原因可能是
(5)研究发现,空气其中少量的NO2也能参与硫酸型酸雨的形成,反应过程如下:
①SO2+NO2→SO3+NO ②SO3+H2O→H2SO4 ③2NO+O2→2NO2
NO2在上述过程中的作用,与H2SO4在下列变化中的作用不符的是
A.潮湿的氯气通过盛有浓H2SO4的洗气瓶
B.硫化氢通入浓H2SO4中
C.浓H2SO4滴入萤石中,加热
D.向盐酸中加入浓硫酸产生白雾
(6)为了防治酸雨,工业上常采用“钙基固硫法”即将生石灰和含硫的煤混合后燃烧,燃烧时硫、氧气和生石灰共同作用,使硫元素转移到炉渣中,大部分硫元素最终转化为固体盐是

(7)若采用如图所示的流程处理则气体a是
您最近一年使用:0次
5 . 某研究性学习小组同学拟分析某市空气的质量情况,测定该市空气中SO2的含量并制定下列研究方案:
Ⅰ.资料表明,SO2具有较强的还原性,能与高锰酸钾酸性溶液发生反应:5SO2+2 +2H2O=5
+2H2O=5 +2Mn2++4H+。
+2Mn2++4H+。
Ⅱ.设计实验方案:利用SO2的还原性使SO2和已知浓度及体积的高锰酸钾酸性溶液反应。
Ⅲ.选择分析地点:某工业区、某公园、某居民小区、某商业区、某交通枢纽。
Ⅳ.选择分析时间:晴天、风速较小时;晴天、风速较大时;雨前;雨后。
Ⅴ.对测定的结果进行初步分析并向相关单位提出建议。
(1)该小组同学拟用如图所示装置定量分析空气中SO2的含量。

①通入空气前应进行的实验操作是________________________________ ;
②当观察到实验的现象为________________________________________ 时,应停止通空气;
③实验过程中需测量并记录的数据是_________________________________ 。
(2)如图表示该小组同学根据实验测得的该市不同地区空气中SO2的含量。

①工厂区、交通枢纽SO2含量明显高于其他地区的原因是_____________ ;
②请向当地有关部门提出一条减少工厂区SO2排放的建议:__________________________ 。
(3)下表是该小组同学测得的不同天气情况下的城市空气中SO2的平均含量。请分析雨后或风速较大时SO2平均含量较低的原因:
①_____________________________________________________ ;
②_____________________________________________________ 。
Ⅰ.资料表明,SO2具有较强的还原性,能与高锰酸钾酸性溶液发生反应:5SO2+2
 +2H2O=5
+2H2O=5 +2Mn2++4H+。
+2Mn2++4H+。Ⅱ.设计实验方案:利用SO2的还原性使SO2和已知浓度及体积的高锰酸钾酸性溶液反应。
Ⅲ.选择分析地点:某工业区、某公园、某居民小区、某商业区、某交通枢纽。
Ⅳ.选择分析时间:晴天、风速较小时;晴天、风速较大时;雨前;雨后。
Ⅴ.对测定的结果进行初步分析并向相关单位提出建议。
(1)该小组同学拟用如图所示装置定量分析空气中SO2的含量。

①通入空气前应进行的实验操作是
②当观察到实验的现象为
③实验过程中需测量并记录的数据是
(2)如图表示该小组同学根据实验测得的该市不同地区空气中SO2的含量。

①工厂区、交通枢纽SO2含量明显高于其他地区的原因是
②请向当地有关部门提出一条减少工厂区SO2排放的建议:
(3)下表是该小组同学测得的不同天气情况下的城市空气中SO2的平均含量。请分析雨后或风速较大时SO2平均含量较低的原因:
| 天气情况 | 平均风速(m·s−1) | 空气中SO2的平均含量(mg·L−1) |
| 雨前 | 2.0 | 0.03 |
| 雨后 | 2.2 | 0.01 |
| 晴 | 23 | 0.015 |
| 晴 | 0.9 | 0.03 |
①
②
您最近一年使用:0次
2018-08-09更新
|
317次组卷
|
7卷引用:3.3.1 硫循环-【帮课堂】2022-2023学年高一化学同步精品讲义(沪科版2020必修第一册)
(已下线)3.3.1 硫循环-【帮课堂】2022-2023学年高一化学同步精品讲义(沪科版2020必修第一册)2018年高一化学(人教版)必修1综合题型练习卷:非金属及其化合物(已下线)2018年12月3日——《每日一题》高一人教必修1-二氧化硫和二氧化氮对大气的污染及其防治(已下线)2019年12月2日 《每日一题》人教版(必修1)——二氧化硫和二氧化氮对大气的污染及其防治(已下线)考点11 硫及其化合物-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点11 硫及其化合物-备战2022年高考化学一轮复习考点帮(浙江专用)(已下线)考点10 硫及其化合物-备战2023年高考化学一轮复习考点帮(全国通用)
解题方法
6 . 回答下列问题。
I.酸雨是指 pH<5.6 的降水。
(1)下列气体中,与形成酸雨无关的是___________ 。
A.CO2 B.SO2 C.NOx
(2)从硫元素的化合价看,下列物质不具有氧化性的是___________。
Ⅱ.揭开浓硫酸的“神秘面纱”。
(3)在化工生产的过程中,一些试剂需要特殊的运输方式,比如具有强氧化性、强还原性、强腐蚀性等性质的试剂。通常情况下,下列物质可用铁制槽车装运的是___________。
I.酸雨是指 pH<5.6 的降水。
(1)下列气体中,与形成酸雨无关的是
A.CO2 B.SO2 C.NOx
(2)从硫元素的化合价看,下列物质不具有氧化性的是___________。
| A.Na2S | B.S | C.SO2 | D.H2SO4 |
Ⅱ.揭开浓硫酸的“神秘面纱”。
(3)在化工生产的过程中,一些试剂需要特殊的运输方式,比如具有强氧化性、强还原性、强腐蚀性等性质的试剂。通常情况下,下列物质可用铁制槽车装运的是___________。
| A.浓盐酸 | B.浓硫酸 | C.稀硫酸 | D.浓氢氧化钠溶液 |
您最近一年使用:0次
名校
解题方法
7 . 在“价—类”二维图中融入“杠杆模型”,可直观辨析部分物质转化及其定量关系。如图中的字母分别代表硫及其常见化合物,相关推断不合理的是
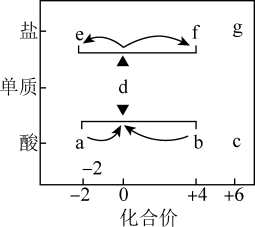
| A.b既具有氧化性又具有还原性 |
| B.硫酸型酸雨的形成过程涉及b到c的转化 |
| C.a溶液与b溶液反应过程中有淡黄色沉淀生成 |
| D.d在加热下与强碱溶液反应生成e和f,且n(e):n(f)=1:2 |
您最近一年使用:0次
2022-04-23更新
|
1474次组卷
|
8卷引用:上海市复兴高级中学2022-2023学年高三上学期10月月考化学试题
8 . 含硫的物质与人们的生活密切相关。已知硫元素常见的化合价有-2、0、+4、+6四种,其不同价态的物质间可相互转化,完成下列填空:
(1)写出硫与铁反应的化学方程式_____________________ ,所得产物的颜色为_________ 。
(2)将硫化氢气体与二氧化硫气体在集气瓶中混合发生反应,现象是___________ ,硫化氢呈现______ (选填“氧化性”、“还原性”)。
(3)二氧化硫是形成酸雨的“元凶”之一,由二氧化硫形成的酸雨的主要成分是_________ 。
(4)硫酸盐的种类很多,且应用广泛,医疗上采用____ 作X射线透视肠胃的内服药剂。
(1)写出硫与铁反应的化学方程式
(2)将硫化氢气体与二氧化硫气体在集气瓶中混合发生反应,现象是
(3)二氧化硫是形成酸雨的“元凶”之一,由二氧化硫形成的酸雨的主要成分是
(4)硫酸盐的种类很多,且应用广泛,医疗上采用
您最近一年使用:0次
名校
9 . 酸雨是全球三大环境危害之一,根据其所带的酸性物质不同,酸雨分为硫酸型酸雨和硝酸型酸雨。
(1)酸雨的标准是:降水的pH_______ 。测得某地雨水样本中的硫酸浓度为 ,计算pH=
,计算pH=_______ (计算结果保留一位小数)。
(2)写出硫酸型酸雨形成过程的两种途径(用化学方程式表示):①_______ 、_______ ;②_______ 、_______ 。
(3)有人提出了一种利用氯碱工业产品处理含二氧化硫废气的方法,具体流程如下:

写出装置C中反应的离子方程式_______ 。该流程中可以循环利用的物质是_______ (填写化学式)。
(4)还有学者提出利用 、
、 等离子的催化作用,常温下将
等离子的催化作用,常温下将 氧化成
氧化成 而实现
而实现 的回收利用。某研究性学习小组据此设计了如下方案,在实验室条件下测定转化器中
的回收利用。某研究性学习小组据此设计了如下方案,在实验室条件下测定转化器中 氧化成
氧化成 的转化率。(转化率=
的转化率。(转化率= ×100%)
×100%)

该小组采用下图装置在实验室测定模拟烟气中 的体积分数,X溶液可以是_______。
的体积分数,X溶液可以是_______。

(5)若上述实验是在标准状况下进行的,欲测定转化器中 氧化成
氧化成 的转化率。已知气体流速,还需测定的数据有
的转化率。已知气体流速,还需测定的数据有_______ 、_______ 。
(1)酸雨的标准是:降水的pH
 ,计算pH=
,计算pH=(2)写出硫酸型酸雨形成过程的两种途径(用化学方程式表示):①
(3)有人提出了一种利用氯碱工业产品处理含二氧化硫废气的方法,具体流程如下:

写出装置C中反应的离子方程式
(4)还有学者提出利用
 、
、 等离子的催化作用,常温下将
等离子的催化作用,常温下将 氧化成
氧化成 而实现
而实现 的回收利用。某研究性学习小组据此设计了如下方案,在实验室条件下测定转化器中
的回收利用。某研究性学习小组据此设计了如下方案,在实验室条件下测定转化器中 氧化成
氧化成 的转化率。(转化率=
的转化率。(转化率= ×100%)
×100%)
该小组采用下图装置在实验室测定模拟烟气中
 的体积分数,X溶液可以是_______。
的体积分数,X溶液可以是_______。
| A.碘的淀粉溶液 | B.酸性高锰酸钾溶液 |
| C.氢氧化钠溶液 | D.氯化钡溶液 |
 氧化成
氧化成 的转化率。已知气体流速,还需测定的数据有
的转化率。已知气体流速,还需测定的数据有
您最近一年使用:0次
解题方法
10 . 酸雨是全球三大环境危害之一,根据其所带的酸性物质不同,酸雨分为硫酸型酸雨和硝酸型酸雨。
(1)酸雨的标准是:降水的pH小于___________ 。
(2)写出硫酸型酸雨的形成过程(用化学方程式表示)___________ 。
(3)有人提出了一种利用氯碱工业产品处理含二氧化硫废气的方法,具体流程如下:

①写出装置C中反应的离子方程式___________ 。
②该流程中可以循环利用的物质是___________ (填写化学式)。
(4)还有学者提出利用 、
、 等离子的催化作用,常温下将
等离子的催化作用,常温下将 氧化成
氧化成 而实现
而实现 的回收利用。某研究性学习小组据此设计了如下方案,在实验室条件下测定转化器中
的回收利用。某研究性学习小组据此设计了如下方案,在实验室条件下测定转化器中 氧化成
氧化成 的转化率。
的转化率。
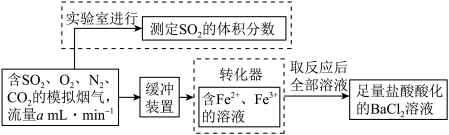
①该小组采用下图装置在实验室测定模拟烟气中 的体积分数,X溶液可以是
的体积分数,X溶液可以是___________ (选填字母)。
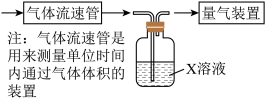
a.碘的淀粉溶液 b.酸性高锰酸钾溶液 c.氢氧化钠溶液 d.氯化钡溶液
②若上述实验是在标准状况下进行的,欲测定转化器中 氧化成
氧化成 的转化率。已知气体流速,还需测定的数据有
的转化率。已知气体流速,还需测定的数据有___________ 、___________ 。
(1)酸雨的标准是:降水的pH小于
(2)写出硫酸型酸雨的形成过程(用化学方程式表示)
(3)有人提出了一种利用氯碱工业产品处理含二氧化硫废气的方法,具体流程如下:

①写出装置C中反应的离子方程式
②该流程中可以循环利用的物质是
(4)还有学者提出利用
 、
、 等离子的催化作用,常温下将
等离子的催化作用,常温下将 氧化成
氧化成 而实现
而实现 的回收利用。某研究性学习小组据此设计了如下方案,在实验室条件下测定转化器中
的回收利用。某研究性学习小组据此设计了如下方案,在实验室条件下测定转化器中 氧化成
氧化成 的转化率。
的转化率。
①该小组采用下图装置在实验室测定模拟烟气中
 的体积分数,X溶液可以是
的体积分数,X溶液可以是
a.碘的淀粉溶液 b.酸性高锰酸钾溶液 c.氢氧化钠溶液 d.氯化钡溶液
②若上述实验是在标准状况下进行的,欲测定转化器中
 氧化成
氧化成 的转化率。已知气体流速,还需测定的数据有
的转化率。已知气体流速,还需测定的数据有
您最近一年使用:0次



