解题方法
1 . 硫和氮及其化合物对人类生存和社会发展意义重大,但硫氧化物和氮氧化物造成的环境问题也日益受到关注。回答以下问题:
图1是工业上生产 的流程图:
的流程图:
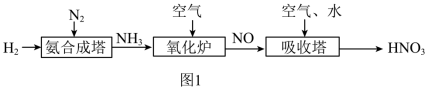
(1)与氮氧化物有关的全球性大气环境问题有___________。
(2)下列有关NH3的说法,不正确的是___________(填字母序号)。
(3)稀硝酸和铜反应的离子方程式为:___________ 。
图2是某化学兴趣小组的同学进行 的一些性质实验(加热装置略):
的一些性质实验(加热装置略):

(4)首先,验证碳、硅非金属性的相对强弱(已知酸性:亚硫酸>碳酸)。
①连接仪器、检查装置气密性、加药品后,打开a、关闭b,然后打开分液漏斗活塞,向圆底烧瓶滴入浓硫酸,加热,则圆底烧瓶中发生反应的化学方程式为:___________ 。
②装置A中试剂是___________ 。
③能说明碳的非金属性比硅强的实验现象是:___________ 。
(5)验证 的某些性质。
的某些性质。
①打开b,关闭a。
②硫化氢溶液中看到有淡黄色沉淀, 体现
体现___________ 。(选填“酸性氧化物”、“还原性”、“氧化性”)
③ 溶液中无明显现象,将其分成两份,分别滴加下列溶液,都产生了白色沉淀,将产生的沉淀的化学式填入下表相应位置。
溶液中无明显现象,将其分成两份,分别滴加下列溶液,都产生了白色沉淀,将产生的沉淀的化学式填入下表相应位置。
图1是工业上生产
 的流程图:
的流程图:
(1)与氮氧化物有关的全球性大气环境问题有___________。
| A.酸雨 | B.沙尘暴 | C.光化学烟雾 | D.白色污染 |
A.工业合成 属于人工固氮 属于人工固氮 |
B. 易液化,液氨常用作制冷剂 易液化,液氨常用作制冷剂 |
C. 可用浓硫酸或无水氯化钙干燥 可用浓硫酸或无水氯化钙干燥 |
D. 制备NO体现了 制备NO体现了 的还原性 的还原性 |
图2是某化学兴趣小组的同学进行
 的一些性质实验(加热装置略):
的一些性质实验(加热装置略):
(4)首先,验证碳、硅非金属性的相对强弱(已知酸性:亚硫酸>碳酸)。
①连接仪器、检查装置气密性、加药品后,打开a、关闭b,然后打开分液漏斗活塞,向圆底烧瓶滴入浓硫酸,加热,则圆底烧瓶中发生反应的化学方程式为:
②装置A中试剂是
③能说明碳的非金属性比硅强的实验现象是:
(5)验证
 的某些性质。
的某些性质。①打开b,关闭a。
②硫化氢溶液中看到有淡黄色沉淀,
 体现
体现③
 溶液中无明显现象,将其分成两份,分别滴加下列溶液,都产生了白色沉淀,将产生的沉淀的化学式填入下表相应位置。
溶液中无明显现象,将其分成两份,分别滴加下列溶液,都产生了白色沉淀,将产生的沉淀的化学式填入下表相应位置。| 滴加的溶液 | 氯水 | 氨水 |
| 沉淀的化学式 |
您最近一年使用:0次
解题方法
2 . 下列关于消除氮氧化物的3种方法,下列说法不正确 的是
①4NO2+O2+4Na2CO3+2H2O=4NaHCO3+4NaNO3
②6NO+4NH3 5N2+6H2O
5N2+6H2O
③2NO+2CO 2CO2+N2
2CO2+N2
①4NO2+O2+4Na2CO3+2H2O=4NaHCO3+4NaNO3
②6NO+4NH3
 5N2+6H2O
5N2+6H2O ③2NO+2CO
 2CO2+N2
2CO2+N2| A.氮氧化物会造成酸雨、光化学烟雾等污染 |
| B.①是利用Na2CO3的碱性和氧化性消除NO2 |
| C.②③的目的是将有毒的含氮物质转化为无毒的N2 |
| D.反应②中每生成1mol N2,转移电子数目为2.4 NA |
您最近一年使用:0次
名校
解题方法
3 . 下列关于硫及其化合物叙述正确的是
A.空气中排放过量 会形成酸雨,酸雨的 会形成酸雨,酸雨的 |
B. 的漂白原理与 的漂白原理与 水溶液、 水溶液、 和氯水三种物质不同 和氯水三种物质不同 |
C.浓硫酸与S反应为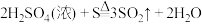 ,在此反应中浓硫酸既表现了强氧化性又表现了酸性 ,在此反应中浓硫酸既表现了强氧化性又表现了酸性 |
D.把足量的铜粉投入只含 的浓硫酸中,加热得到的气体体积在标准状况下为 的浓硫酸中,加热得到的气体体积在标准状况下为 |
您最近一年使用:0次
4 . 化学与生产、生活密切相关。下列说法正确的是
| A.雷雨天闪电时空气中有臭氧(O3)生成,O2和O3的相互转化是物理变化 |
| B.新型冠状病毒具有极强的传染性,可用84消毒液、过氧乙酸等进行环境消毒,是利用了其强氧化性 |
| C.以煤炭为主要燃料的地区,降落后的酸雨中的主要酸性物质是HNO3 |
| D.通常用石油的年产量来衡量一个国家的石油化学工业发展水平 |
您最近一年使用:0次
5 . 资料显示某地区的酸雨主要为硫酸型和盐酸型酸雨。某兴趣小组对酸雨进行实验研究。
(1)提出合理的假设:该酸雨中的溶质除H2SO4、HCl外,该小组同学根据硫酸型酸雨的形成过程,预测主要溶质还有______ 。
(2)设计实验方案验证以上假设。在答题卡上写出实验步骤、预期现象和结论。
限选试剂及仪器:盐酸、硝酸、BaC12溶液、Ba(OH)2溶液、AgNO3溶液、紫色石蕊试液、品红溶液、烧杯、试管、胶头滴管。
(3)酸雨部分组成测定:
①标准溶液配制:实验室用1.000mol·L-1较浓的碘水配制250mL0.02000mol·L-1的碘水溶液,所用的玻璃仪器除烧杯、玻璃棒和吸量管(一种能精确量取一定体积液体的仪器)外,还需要的仪器有______ 、______ 。
②滴定:准确量取25.00mL该酸雨于锥形瓶中,加入几滴______ 溶液作指示剂,将0.02000mol·L-1碘水装入50mL酸式滴定管,滴定终点现象为______ ,记录数据,重复滴定2次,平均消耗碘水VmL。
(1)提出合理的假设:该酸雨中的溶质除H2SO4、HCl外,该小组同学根据硫酸型酸雨的形成过程,预测主要溶质还有
(2)设计实验方案验证以上假设。在答题卡上写出实验步骤、预期现象和结论。
限选试剂及仪器:盐酸、硝酸、BaC12溶液、Ba(OH)2溶液、AgNO3溶液、紫色石蕊试液、品红溶液、烧杯、试管、胶头滴管。
| 实验步骤 | 预期现象和结论 |
| 步骤1:取适量酸雨于A、B两支洁净试管中,待用 | 无明显现象 |
| 步骤2:往A试管中加入过量的Ba(OH)2溶液,静置,过滤 | 有白色沉淀 |
| 步骤3:取少量步骤2得到的滤渣加入过量盐酸 | 滤渣不能完全溶解,说明酸雨中含有硫酸 |
| 步骤4:取适量步骤2得到的滤液, | |
| 步骤5:往B试管中加入 |
①标准溶液配制:实验室用1.000mol·L-1较浓的碘水配制250mL0.02000mol·L-1的碘水溶液,所用的玻璃仪器除烧杯、玻璃棒和吸量管(一种能精确量取一定体积液体的仪器)外,还需要的仪器有
②滴定:准确量取25.00mL该酸雨于锥形瓶中,加入几滴
您最近一年使用:0次
2022高一·上海·专题练习
名校
解题方法
6 . 填空。
(1)氮的氧化物是主要的大气污染物,对大气的影响之一是导致酸雨。用化学方程式表示NO2形成酸雨的原因_______ ,该反应中氧化剂和还原剂的物质的量之比为_______ 。
(2)实验室常用的几种气体发生装置如图A、B、C所示:

①实验室可以用B或C装置制取氨气,如果用C装置,通常使用的药品是_______ ;
②如图1 是某学生设计收集氨气的几种装置,其中可行的是
是某学生设计收集氨气的几种装置,其中可行的是_______ 。

(3)某兴趣小组用如图 装置制备氨气,并探究氨气的还原性并检验产物。
装置制备氨气,并探究氨气的还原性并检验产物。
①实验现象为:黑色CuO变为红色;白色无水CuSO4粉末变为蓝色;同时生成一种无色气体,该气体无污染。请写出氨气与CuO反应的化学方程式_______ 。
②该装置中碱石灰的作用是干燥氨气,无水CuSO4检验反应有水的生成,该装置存在明显缺陷,请提出改进意见_______ 。有同学认为:NH3与CuO反应生成的红色物质中可能含有Cu2O。已知:在酸性溶液中Cu2O+2H+ = Cu+Cu2++2H2O ,请你设计一个简单的实验检验该红色物质中是否含有Cu2O
,请你设计一个简单的实验检验该红色物质中是否含有Cu2O_____ 。
(1)氮的氧化物是主要的大气污染物,对大气的影响之一是导致酸雨。用化学方程式表示NO2形成酸雨的原因
(2)实验室常用的几种气体发生装置如图A、B、C所示:

①实验室可以用B或C装置制取氨气,如果用C装置,通常使用的药品是
②如图1
 是某学生设计收集氨气的几种装置,其中可行的是
是某学生设计收集氨气的几种装置,其中可行的是
(3)某兴趣小组用如图
 装置制备氨气,并探究氨气的还原性并检验产物。
装置制备氨气,并探究氨气的还原性并检验产物。①实验现象为:黑色CuO变为红色;白色无水CuSO4粉末变为蓝色;同时生成一种无色气体,该气体无污染。请写出氨气与CuO反应的化学方程式
②该装置中碱石灰的作用是干燥氨气,无水CuSO4检验反应有水的生成,该装置存在明显缺陷,请提出改进意见
 ,请你设计一个简单的实验检验该红色物质中是否含有Cu2O
,请你设计一个简单的实验检验该红色物质中是否含有Cu2O
您最近一年使用:0次
名校
解题方法
7 . 硫铁矿(含 )是一种重要的化学矿物原料,也是工业制硫酸的主要原料,其煅烧过程及产物存在如下转化关系:
)是一种重要的化学矿物原料,也是工业制硫酸的主要原料,其煅烧过程及产物存在如下转化关系:
(1)硫铁矿中 元素的化合价为
元素的化合价为___________ 。
(2)为了使反应I燃烧得更充分,可以采用的措施是___________ 。
(3)将A通入新制碘水中,发现溶液褪色,发生的离子反应方程式为______________________ 。
(4)下列关于C的说法正确的是___________。
(5)工业上为了防止污染,可以利用氧化亚铁硫杆菌(T.f)对硫铁矿进行催化脱硫,该过程如图所示: ,转移的电子的物质的量为
,转移的电子的物质的量为___________ 。
②脱硫过程中产生的 在酸性溶液中会形成淡黄色沉淀并产生刺激性气味的气体,写出其离子方程式
在酸性溶液中会形成淡黄色沉淀并产生刺激性气味的气体,写出其离子方程式___________ 。
③从氧化还原角度分析,若要制备 应选择
应选择___________ (填字母)。
A. B.
B. C.
C. D.
D.
 )是一种重要的化学矿物原料,也是工业制硫酸的主要原料,其煅烧过程及产物存在如下转化关系:
)是一种重要的化学矿物原料,也是工业制硫酸的主要原料,其煅烧过程及产物存在如下转化关系: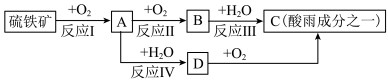
(1)硫铁矿中
 元素的化合价为
元素的化合价为(2)为了使反应I燃烧得更充分,可以采用的措施是
(3)将A通入新制碘水中,发现溶液褪色,发生的离子反应方程式为
(4)下列关于C的说法正确的是___________。
A.酸雨指的是 的雨水 的雨水 |
| B.浓硫酸可以和铁发生反应,不能用钢瓶盛装浓硫酸 |
| C.浓硫酸有强氧化性,稀硫酸没有氧化性 |
| D.稀硫酸长时间放置在空气中浓度会变高,浓硫酸长时间放置在空气中浓度会变低 |
(5)工业上为了防止污染,可以利用氧化亚铁硫杆菌(T.f)对硫铁矿进行催化脱硫,该过程如图所示:
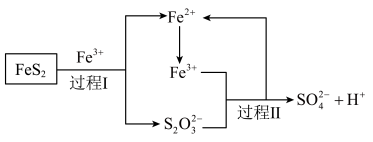
 ,转移的电子的物质的量为
,转移的电子的物质的量为②脱硫过程中产生的
 在酸性溶液中会形成淡黄色沉淀并产生刺激性气味的气体,写出其离子方程式
在酸性溶液中会形成淡黄色沉淀并产生刺激性气味的气体,写出其离子方程式③从氧化还原角度分析,若要制备
 应选择
应选择A.
 B.
B. C.
C. D.
D.
您最近一年使用:0次
2024-04-05更新
|
595次组卷
|
4卷引用:四川省成都市盐道街中学2023-2024学年高一下学期3月月考化学试卷
名校
解题方法
8 . 化学与生产、生活密切相关,下列说法正确的是
| A.煤炭燃烧过程中添加“固硫”装置,可减少二氧化碳的排放 |
| B.铝制品表面有致密的氧化膜保护层,所以可长时间盛放酸(或碱)性物质 |
| C.明矾和臭氧都可用于净水,均利用了其氧化性 |
| D.太阳能、氢能、风能由于资源丰富,没有或很少污染而备受青睐,属于可再生能源 |
您最近一年使用:0次
2023-11-30更新
|
96次组卷
|
3卷引用:四川省自贡市第一中学校2023-2024学年高二上学期期中考试化学试卷
9 . 化学与科学、技术、环境密切相关。下列说法不正确的是
| A.为加快漂白精的漂白速率,使用时可滴加几滴醋酸 |
| B.在食品袋中放入盛有硅胶和铁粉的透气小袋,可防止食物受潮、氧化变质 |
| C.用含酸性重铬酸钾的仪器检验酒驾,利用了乙醇的挥发性和还原性 |
| D.化石燃料完全燃烧不会造成大气污染 |
您最近一年使用:0次
10 . 某研究性学习小组在学习SO2 的性质时,通过查阅文献、理性分析、实验验证与CO2 的性质进行了比较。试根据研究主题和过程,回答下列问题。
(1)水溶液的酸性
①常温常压下,纯水的 pH=7,而酸雨的 pH<5.6.形成酸雨的主要物质是 SO2 和氮的氧化物。把 pH<5.6 的雨水称为酸雨,而不是 pH<7,可能的原因是___________ 。
②查阅文献知: 常温下,H2SO3 的电离常数Ka1 =1.2×10-2 ,Ka2 =6.3×10-3 ,H2CO3的电离常数 Ka1 =4.4×10-7 ,Ka2 =4.7×10-11 。选用下面的药品和装置验证 H2SO3 和H2CO3 的酸性强弱,其连接顺序:A→___________ (按气流方向用大写字母表示即可)。D装置的主要作用是___________ 。
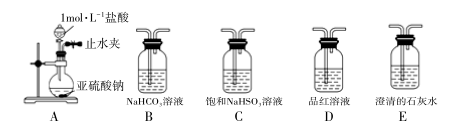
③根据②中的数据可知,配置相同物质的量浓度的NaHSO3 和NaHCO3 溶液,其pH值大小关系为pH(NaHSO3)___________ pH(NaHCO3 )(填“>”、“<”或“=”)。
(2)二氧化硫的还原性
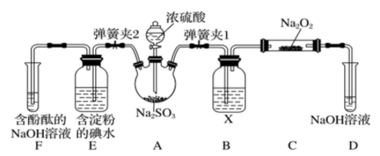
若按图示装置进行实验(部分固定装置未画出)。请你在实验前根据预设的操作,推测可能的实验现象及其对应的原因。
(1)水溶液的酸性
①常温常压下,纯水的 pH=7,而酸雨的 pH<5.6.形成酸雨的主要物质是 SO2 和氮的氧化物。把 pH<5.6 的雨水称为酸雨,而不是 pH<7,可能的原因是
②查阅文献知: 常温下,H2SO3 的电离常数Ka1 =1.2×10-2 ,Ka2 =6.3×10-3 ,H2CO3的电离常数 Ka1 =4.4×10-7 ,Ka2 =4.7×10-11 。选用下面的药品和装置验证 H2SO3 和H2CO3 的酸性强弱,其连接顺序:A→

③根据②中的数据可知,配置相同物质的量浓度的NaHSO3 和NaHCO3 溶液,其pH值大小关系为pH(NaHSO3)
(2)二氧化硫的还原性
若按图示装置进行实验(部分固定装置未画出)。请你在实验前根据预设的操作,推测可能的实验现象及其对应的原因。

| 预设的操作步骤 | 预期的实验现象 | 推测可能的原因 |
| 关闭弹簧夹2,打开弹簧夹1,将硫酸注入三颈烧瓶至浸没固体 | 若将带火星的木条放在D试管口处,木条不复燃 | SO2与Na2O2反应无O2生成,可能发生反应的化学方程式为① |
| 若将带火星的木条放在D试管口处,木条复燃 | SO2与Na2O2反应有O2生成,发生的化学反应:2SO2+2Na2O2=2Na2SO3+O2 | |
| 关闭弹簧夹1,打开弹簧夹2,残余气体进入E、F中 | E中② | E中反应的离子方程式③ |
| F中④ | F中反应为2OH- + SO2=SO + H2O + H2O |
您最近一年使用:0次



