名校
解题方法
1 . 以不同类别物质间的转化为线索,认识钠及其化合物。
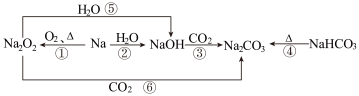
下列分析不正确 的是

下列分析
A.反应③表明 具有酸性氧化物的性质 具有酸性氧化物的性质 |
B.反应④说明 的稳定性弱于 的稳定性弱于 |
| C.反应⑤、⑥可用于潜水艇中氧气的供给 |
D.⑥说明 是碱性氧化物 是碱性氧化物 |
您最近一年使用:0次
2024-01-24更新
|
184次组卷
|
4卷引用:内蒙古科尔沁右翼前旗第二中学2023-2024学年高一上学期12月月考化学试题
名校
解题方法
2 . 现有一定量含有 杂质的
杂质的 试样,用下图的实验装置测定
试样,用下图的实验装置测定 试样的纯度。
试样的纯度。
可供选用的反应物有 固体、
固体、 盐酸、
盐酸、 硫酸和蒸馏水。
硫酸和蒸馏水。
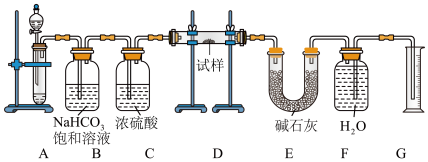
回答下列问题。
(1)装置A中液体试剂选用盐酸而不是硫酸,理由是______________ 。
(2)装置B的作用是______________ ;装置C的作用是______________ ;装置E中碱石灰的作用是______________ 。
(3)装置D中发生反应的化学方程式为______________ 、______________ 。
(4)若开始时测得样品的质量为 ,反应结束后测得气体的体积为
,反应结束后测得气体的体积为 (标准状况),则
(标准状况),则 试样的纯度为
试样的纯度为_______ 。
 杂质的
杂质的 试样,用下图的实验装置测定
试样,用下图的实验装置测定 试样的纯度。
试样的纯度。可供选用的反应物有
 固体、
固体、 盐酸、
盐酸、 硫酸和蒸馏水。
硫酸和蒸馏水。
回答下列问题。
(1)装置A中液体试剂选用盐酸而不是硫酸,理由是
(2)装置B的作用是
(3)装置D中发生反应的化学方程式为
(4)若开始时测得样品的质量为
 ,反应结束后测得气体的体积为
,反应结束后测得气体的体积为 (标准状况),则
(标准状况),则 试样的纯度为
试样的纯度为
您最近一年使用:0次
2024-01-23更新
|
186次组卷
|
2卷引用:河南省郑州市中牟县第一高级中学2023-2024学年高一上学期1月月考化学试题
名校
3 . 关于物质的相关用途,下列说法错误的是
| A.氧化铝可用于耐火材料 | B.通常状况下液氯可以用钢瓶储存运输 |
| C.金属钠着火时,可用泡沫灭火器灭火 | D.配制 溶液时加入少量的铁粉 溶液时加入少量的铁粉 |
您最近一年使用:0次
名校
4 . 过氧化钠在供氧、防腐、除臭、微量分析等多方面有着重要用途。
Ⅰ.神舟十三号载人飞船的轨道舱内安装盛有 颗粒的装置,可为宇航员供氧。
颗粒的装置,可为宇航员供氧。
(1)写出 与人体呼出气体中的酸性氧化物反应的化学方程式
与人体呼出气体中的酸性氧化物反应的化学方程式_______ 。
Ⅱ.工业生产过氧化钠的方法是先将除去二氧化碳的干燥空气通入熔融的钠(温度180~200℃)中得到氧化钠,然后增加空气流量并迅速升高温度至300~400℃即可得到过氧化钠。某化学兴趣小组在实验室模拟工业流程制备过氧化钠。
(2)结合下图所示装置写出仪器连接顺序。
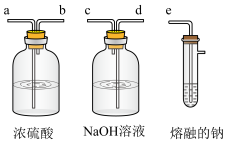
空气→_______ (填导管口字母)。
(3)下列选项中的加热方式适合该实验的是_______(填字母)。
(4)若要提高产品纯度,需在盛有熔融的钠的具支试管后添加一个装置,该装置应该是_______ ,其作用是_______ 。
(5)实验中使用钠的质量为4.600g,最终所得产品的质量为8.320g,通过仪器检测发现产品中含有少量 ,则该实验所得产品的产率为
,则该实验所得产品的产率为_______ 。
Ⅲ.研究 与水的反应。取一定量
与水的反应。取一定量 ,加入足量的水,充分反应。收集并测量生成
,加入足量的水,充分反应。收集并测量生成 的体积,发现体积小于理论计算值。某小组研究产生这一差异的原因,进行如下实验。
的体积,发现体积小于理论计算值。某小组研究产生这一差异的原因,进行如下实验。
查阅资料:
①过氧化钠与水反应的过程中还可能存在以下两个复分解反应:ⅰ.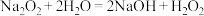 ;ⅱ.
;ⅱ.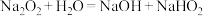 。
。
②与 类似,
类似,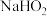 也能在
也能在 催化的条件下分解生成
催化的条件下分解生成 。
。
依据资料设计如下实验:取 与足量水反应,140s时不再产生气泡,180s时向所得溶液中加入少量
与足量水反应,140s时不再产生气泡,180s时向所得溶液中加入少量 ,立即产生无色气体。过程中溶液的体积始终约为40mL。反应过程中pH变化如图所示。已知:溶液中
,立即产生无色气体。过程中溶液的体积始终约为40mL。反应过程中pH变化如图所示。已知:溶液中 越大,溶液pH越大。
越大,溶液pH越大。
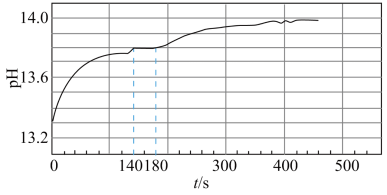
(6)小组同学根据pH的变化判断反应过程中一定发生反应ⅱ,判断的理由是_______ 。
(7)由上述实验得出收集到 的体积小于理论计算值的原因之一是
的体积小于理论计算值的原因之一是_______ 。
Ⅰ.神舟十三号载人飞船的轨道舱内安装盛有
 颗粒的装置,可为宇航员供氧。
颗粒的装置,可为宇航员供氧。(1)写出
 与人体呼出气体中的酸性氧化物反应的化学方程式
与人体呼出气体中的酸性氧化物反应的化学方程式Ⅱ.工业生产过氧化钠的方法是先将除去二氧化碳的干燥空气通入熔融的钠(温度180~200℃)中得到氧化钠,然后增加空气流量并迅速升高温度至300~400℃即可得到过氧化钠。某化学兴趣小组在实验室模拟工业流程制备过氧化钠。
(2)结合下图所示装置写出仪器连接顺序。

空气→
(3)下列选项中的加热方式适合该实验的是_______(填字母)。
| A.控温电炉(150~500℃) | B.水浴 |
| C.酒精喷灯(1000~1200℃) | D.油浴(100~260℃) |
(4)若要提高产品纯度,需在盛有熔融的钠的具支试管后添加一个装置,该装置应该是
(5)实验中使用钠的质量为4.600g,最终所得产品的质量为8.320g,通过仪器检测发现产品中含有少量
 ,则该实验所得产品的产率为
,则该实验所得产品的产率为Ⅲ.研究
 与水的反应。取一定量
与水的反应。取一定量 ,加入足量的水,充分反应。收集并测量生成
,加入足量的水,充分反应。收集并测量生成 的体积,发现体积小于理论计算值。某小组研究产生这一差异的原因,进行如下实验。
的体积,发现体积小于理论计算值。某小组研究产生这一差异的原因,进行如下实验。查阅资料:
①过氧化钠与水反应的过程中还可能存在以下两个复分解反应:ⅰ.
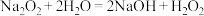 ;ⅱ.
;ⅱ.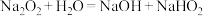 。
。②与
 类似,
类似,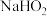 也能在
也能在 催化的条件下分解生成
催化的条件下分解生成 。
。依据资料设计如下实验:取
 与足量水反应,140s时不再产生气泡,180s时向所得溶液中加入少量
与足量水反应,140s时不再产生气泡,180s时向所得溶液中加入少量 ,立即产生无色气体。过程中溶液的体积始终约为40mL。反应过程中pH变化如图所示。已知:溶液中
,立即产生无色气体。过程中溶液的体积始终约为40mL。反应过程中pH变化如图所示。已知:溶液中 越大,溶液pH越大。
越大,溶液pH越大。
(6)小组同学根据pH的变化判断反应过程中一定发生反应ⅱ,判断的理由是
(7)由上述实验得出收集到
 的体积小于理论计算值的原因之一是
的体积小于理论计算值的原因之一是
您最近一年使用:0次
名校
5 . 按要求填空:
现有以下物质:①石墨;②铝;③乙醇;④氨气;⑤液氯;⑥碳酸氢钠固体;⑦氢氧化钡溶液;⑧纯醋酸;⑨氢氧化钠固体。
(1)属于电解质的是___________ (填写序号)。
(2)写出物质⑤在水中反应的离子方程式:___________ 。
(3)40.5g某金属氯化物MCl2中含有0.6molCl-,则该氯化物的摩尔质量为___________ 。
(4)标准状况下,体积为11.2LCO2与足量Na2O2反应,生成气体的体积为___________ L,反应转移电子数为___________ (用NA表示),Na2O2中阴、阳离子个数比为___________ 。
(5)已知P2O5为酸性氧化物,可与水反应生成磷酸(H3PO4),写出P2O5与足量NaOH溶液反应的离子方程式:___________ 。
现有以下物质:①石墨;②铝;③乙醇;④氨气;⑤液氯;⑥碳酸氢钠固体;⑦氢氧化钡溶液;⑧纯醋酸;⑨氢氧化钠固体。
(1)属于电解质的是
(2)写出物质⑤在水中反应的离子方程式:
(3)40.5g某金属氯化物MCl2中含有0.6molCl-,则该氯化物的摩尔质量为
(4)标准状况下,体积为11.2LCO2与足量Na2O2反应,生成气体的体积为
(5)已知P2O5为酸性氧化物,可与水反应生成磷酸(H3PO4),写出P2O5与足量NaOH溶液反应的离子方程式:
您最近一年使用:0次
2024-01-19更新
|
61次组卷
|
2卷引用:湖北省沙市中学2023-2024学年高一上学期11月月考化学试题
名校
解题方法
6 . 过氧化钠常用作漂白剂、杀菌剂、消毒剂,能与水和二氧化碳等物质发生反应,在空气中保存不当时容易变质。某实验小组以过氧化钠为研究对象进行了如下实验。
(1)探究一包Na2O2样品是否已经变质:取少量样品,加水将其溶解,加入_______ 溶液(填化学式),充分振荡后有白色沉淀,证明Na2O2已经变质。
(2)该实验小组为了粗略测定过氧化钠的质量分数,称取了mg样品,并设计用下图装置来测定过氧化钠的质量分数。_______ ,有同学提出该实验装置A、C装置之间没必要增加盛有饱和NaHCO3溶液的洗气瓶,该同学想法是否有道理?且说明理由:_______ 。(答“有”或“无”且说明理由)
②将仪器连接好以后,必须进行的第一步操作是_______ 。
③写出装置C中发生的主要反应的化学方程式:_______ 。
④装置D的作用是_______ ;若无装置D,样品中Na2O2的质量分数_______ (填“偏高”“偏低”或“无影响”)。
⑤实验结束后,装置F中水的体积为VmL,已知氧气的密度为ρg·mL-1,样品中Na2O2质量分数为_______ (用含ρ、m、V的代数式表示)。
(1)探究一包Na2O2样品是否已经变质:取少量样品,加水将其溶解,加入
(2)该实验小组为了粗略测定过氧化钠的质量分数,称取了mg样品,并设计用下图装置来测定过氧化钠的质量分数。
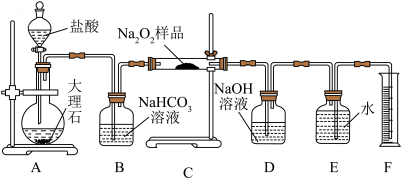
②将仪器连接好以后,必须进行的第一步操作是
③写出装置C中发生的主要反应的化学方程式:
④装置D的作用是
⑤实验结束后,装置F中水的体积为VmL,已知氧气的密度为ρg·mL-1,样品中Na2O2质量分数为
您最近一年使用:0次
2024-01-18更新
|
146次组卷
|
3卷引用:辽宁省六校协作体2023-2024学年高一上学期第三次考试化学试题
名校
解题方法
7 . 为测定某含有杂质 的
的 样品的纯度,2个小组分别设计如下方案。首先准确称量样品
样品的纯度,2个小组分别设计如下方案。首先准确称量样品 ,然后,按照以下方案进行实验,请你完成相关内容:
,然后,按照以下方案进行实验,请你完成相关内容:
[方案一]:将样品与水充分反应,使产生的 通过灼热的铜粉,测得反应后生成氧化铜的质量为
通过灼热的铜粉,测得反应后生成氧化铜的质量为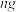 ,通过计算求出试样中
,通过计算求出试样中 的含量。
的含量。
(1) 跟水反应的离子方程式是
跟水反应的离子方程式是_______ 。
[方案二]:将样品与二氧化碳反应,通过测定反应产生氧气的体积,计算出样品中 的含量。
的含量。

(2)上图是完成该实验可能用到的实验装置,根据此实验方案,实验所使用仪器的连接次序是_______ (填写仪器编号)
(3) 跟
跟 的化学反应方程式为
的化学反应方程式为_______
(4)装置①和⑤的作用分别是_______ 和_______ 。
 的
的 样品的纯度,2个小组分别设计如下方案。首先准确称量样品
样品的纯度,2个小组分别设计如下方案。首先准确称量样品 ,然后,按照以下方案进行实验,请你完成相关内容:
,然后,按照以下方案进行实验,请你完成相关内容:[方案一]:将样品与水充分反应,使产生的
 通过灼热的铜粉,测得反应后生成氧化铜的质量为
通过灼热的铜粉,测得反应后生成氧化铜的质量为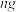 ,通过计算求出试样中
,通过计算求出试样中 的含量。
的含量。(1)
 跟水反应的离子方程式是
跟水反应的离子方程式是[方案二]:将样品与二氧化碳反应,通过测定反应产生氧气的体积,计算出样品中
 的含量。
的含量。
(2)上图是完成该实验可能用到的实验装置,根据此实验方案,实验所使用仪器的连接次序是
(3)
 跟
跟 的化学反应方程式为
的化学反应方程式为(4)装置①和⑤的作用分别是
您最近一年使用:0次
名校
8 . 取3g下列物质在氧气中完全燃烧,将其产物跟足量的过氧化钠固体完全反应,反应后固体的质量恰好也增加了3g,则下列物质中不能满足 上述结果的是
A. | B. | C. | D.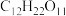 |
您最近一年使用:0次
名校
9 . 下列说法不正确 的是
| A.过氧化钠可用作呼吸面具的供氧剂 |
| B.碳酸氢钠用作食用碱 |
| C.在医疗上,纯碱是治疗胃酸过多的一种药剂 |
D.相同条件下, 的溶解度大于 的溶解度大于 |
您最近一年使用:0次
名校
10 .  是重要的化工原料,具有多种用途。回答下列问题:
是重要的化工原料,具有多种用途。回答下列问题:
(1) 可在呼吸面具和潜水艇中作为氧气的来源,请写出
可在呼吸面具和潜水艇中作为氧气的来源,请写出 与
与 反应的化学方程式
反应的化学方程式___________ 。
(2)将一定量的 固体投入到含有下列离子的溶液中:
固体投入到含有下列离子的溶液中: 、
、 、
、 、
、 ,反应完毕后,溶液中上述离子数目几乎不变的有
,反应完毕后,溶液中上述离子数目几乎不变的有___________ (填离子符号)。
(3)查阅资料知: 在一定条件下可以转化为
在一定条件下可以转化为 ,
, 易溶于水且溶解时吸热,有咸味,遇酸易放出气体,人误食会中毒。
易溶于水且溶解时吸热,有咸味,遇酸易放出气体,人误食会中毒。
①已知 能发生如下反应:
能发生如下反应: 。上述反应中氧化剂是
。上述反应中氧化剂是___________ ,氧化产物是___________ ; 在反应中体现了
在反应中体现了___________ (填性质)。
②根据上述反应鉴别 和
和 。可选用的物质有
。可选用的物质有___________ (填字母)。
A.水 B.碘化钾淀粉试纸 C.淀粉 D.白酒 E.食用白醋
(4)某学习小组以过氧化钠为原料制备出了一定量的纯碱,不小心混入了少量的 ,现欲对其纯度进行测定,将10g样品加热至质量不再发生变化,其质量变为6.9g,则该纯碱样品的纯度(即质量分数)为
,现欲对其纯度进行测定,将10g样品加热至质量不再发生变化,其质量变为6.9g,则该纯碱样品的纯度(即质量分数)为___________ 。
 是重要的化工原料,具有多种用途。回答下列问题:
是重要的化工原料,具有多种用途。回答下列问题:(1)
 可在呼吸面具和潜水艇中作为氧气的来源,请写出
可在呼吸面具和潜水艇中作为氧气的来源,请写出 与
与 反应的化学方程式
反应的化学方程式(2)将一定量的
 固体投入到含有下列离子的溶液中:
固体投入到含有下列离子的溶液中: 、
、 、
、 、
、 ,反应完毕后,溶液中上述离子数目几乎不变的有
,反应完毕后,溶液中上述离子数目几乎不变的有(3)查阅资料知:
 在一定条件下可以转化为
在一定条件下可以转化为 ,
, 易溶于水且溶解时吸热,有咸味,遇酸易放出气体,人误食会中毒。
易溶于水且溶解时吸热,有咸味,遇酸易放出气体,人误食会中毒。①已知
 能发生如下反应:
能发生如下反应: 。上述反应中氧化剂是
。上述反应中氧化剂是 在反应中体现了
在反应中体现了②根据上述反应鉴别
 和
和 。可选用的物质有
。可选用的物质有A.水 B.碘化钾淀粉试纸 C.淀粉 D.白酒 E.食用白醋
(4)某学习小组以过氧化钠为原料制备出了一定量的纯碱,不小心混入了少量的
 ,现欲对其纯度进行测定,将10g样品加热至质量不再发生变化,其质量变为6.9g,则该纯碱样品的纯度(即质量分数)为
,现欲对其纯度进行测定,将10g样品加热至质量不再发生变化,其质量变为6.9g,则该纯碱样品的纯度(即质量分数)为
您最近一年使用:0次



