名校
1 . 元素周期律反映了元素性质随原子序数递增的周期性变化规律。
(1)元素的性质,特别是化学性质取决于元素的原子结构。钠、镁、铝元素形成的最高价氧化物对应的水化物中,碱性最强的是___________ (填碱的化学式)。
(2)碱金属元素中,137Cs和133Cs之间的关系是互为___________ ,金属钾的氧化物有多种,写出K2O2与CO2反应的化学方程式:___________ 。
(3)可根据元素周期律推测元素的某些性质。如已知卤族元素的性质递变规律,可推知元素砹(At)形成的氢化物HAt的稳定性___________ HI的稳定性(填“大于”或“小于”),AgAt___________ 溶于水(填“易”或“难”)。
(1)元素的性质,特别是化学性质取决于元素的原子结构。钠、镁、铝元素形成的最高价氧化物对应的水化物中,碱性最强的是
(2)碱金属元素中,137Cs和133Cs之间的关系是互为
(3)可根据元素周期律推测元素的某些性质。如已知卤族元素的性质递变规律,可推知元素砹(At)形成的氢化物HAt的稳定性
您最近一年使用:0次
2 . 国际化学年的中国宣传口号是“化学——我们的生活,我们的未来”。
(1)宇航员常用过氧化钠作供氧剂,写出过氧化钠与二氧化碳反应的化学方程式:_______ 。
(2)厨房里小苏打常作面包和糕点的发泡剂,写出小苏打溶于水的电离方程式:_______ 。
(3)电子工业常用30%的FeCl3溶液腐蚀敷在绝缘板上的铜箔来制造印刷电路板。写出FeCl3溶液与铜发生反应的离子方程式:_______ 。
(4)化学实验中,若使某步中的有害产物作为另一步的反应物,形成一个循环,则可不再向环境排放该种有害物质。
①在如下图所示步骤中,发生氧化反应的是_______ (填序号,下同),发生还原反应的是_______ ,既没发生氧化反应又没发生还原反应的是_______ 。(提示:铬元素的化合价有+6、+3)_______ 。
_______K2Cr2O7+_______HCl=_______Cl2↑+_______KCl+_______CrCl3+_______
(5)已知方程式F:KClO3+6HCl(浓)=KCl+3H2O+3Cl2↑。
①请用双线桥法标出电子转移的方向和数目_______ 。
②上述反应中氧化产物和还原产物的质量比为_______ 。
(1)宇航员常用过氧化钠作供氧剂,写出过氧化钠与二氧化碳反应的化学方程式:
(2)厨房里小苏打常作面包和糕点的发泡剂,写出小苏打溶于水的电离方程式:
(3)电子工业常用30%的FeCl3溶液腐蚀敷在绝缘板上的铜箔来制造印刷电路板。写出FeCl3溶液与铜发生反应的离子方程式:
(4)化学实验中,若使某步中的有害产物作为另一步的反应物,形成一个循环,则可不再向环境排放该种有害物质。
①在如下图所示步骤中,发生氧化反应的是
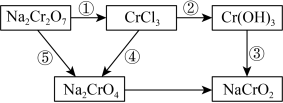
_______K2Cr2O7+_______HCl=_______Cl2↑+_______KCl+_______CrCl3+_______
(5)已知方程式F:KClO3+6HCl(浓)=KCl+3H2O+3Cl2↑。
①请用双线桥法标出电子转移的方向和数目
②上述反应中氧化产物和还原产物的质量比为
您最近一年使用:0次
解题方法
3 . 钠及其化合物在认识物质转化规律以及生产生活中均有重要应用。
Ⅰ.钠与水的反应
(1)写出钠与水反应的化学方程式________ 。
(2)若反应中生成H2的体积为1.12L(标准状况下),则参与反应的金属Na的质量是__________ 。
(3)同物质类别的金属Mg也能与水发生反应,试着调用反应规律分析Na和Mg分别与水反应的剧烈程度:Na________ Mg(填“>”“<"或“=”)。
Ⅱ.钠与氧气的反应
(4)钠与氧气反应的产物有多种可能,造成产物多样的原因是__________ 。
(5)其中产物_______ (填化学式)可用作潜水艇和呼吸面具中的供氧剂,写出其与CO2反应的化学方程式__________ 。
Ⅲ.碳酸钠、碳酸氢钠在食品加工方面有着广泛的用途。
(6)下列关于Na2CO3的认识正确的是_________ 。
a.受热易分解 b.俗称纯碱、苏打 c.属于碱 d.可与酸反应
(7)传统蒸馒头常采用酵头发面,酵头可使面团在微生物作用下产生CO2气体,从而使面团疏松,但同时也会产生乳酸、醋酸等有机酸,需要额外添加“碱面"将酸去除。等质量的Na2CO3和NaHCO3,因_____ (填“Na2CO3”或*NaHCO3")消耗酸更多,更适合作为中和发酵带来的酸味的“碱面”。
(8)若面团发得不好,面团内的气孔少,不够膨松,需添加______ (填“Na2CO3"或“NaHCO3"),继续揉面,上锅蒸后也能蒸出松软的馒头,用化学方程式表示其产气原理_____________ 。
Ⅰ.钠与水的反应
(1)写出钠与水反应的化学方程式
(2)若反应中生成H2的体积为1.12L(标准状况下),则参与反应的金属Na的质量是
(3)同物质类别的金属Mg也能与水发生反应,试着调用反应规律分析Na和Mg分别与水反应的剧烈程度:Na
Ⅱ.钠与氧气的反应
(4)钠与氧气反应的产物有多种可能,造成产物多样的原因是
(5)其中产物
Ⅲ.碳酸钠、碳酸氢钠在食品加工方面有着广泛的用途。
(6)下列关于Na2CO3的认识正确的是
a.受热易分解 b.俗称纯碱、苏打 c.属于碱 d.可与酸反应
(7)传统蒸馒头常采用酵头发面,酵头可使面团在微生物作用下产生CO2气体,从而使面团疏松,但同时也会产生乳酸、醋酸等有机酸,需要额外添加“碱面"将酸去除。等质量的Na2CO3和NaHCO3,因
(8)若面团发得不好,面团内的气孔少,不够膨松,需添加
您最近一年使用:0次
解题方法
4 . 金属钠及其化合物在人类生产、生活中起着重要作用。诸回答下列问题:
(1)向一小烧杯中分别加入等体积的水和煤油,片刻后再向该烧杯中加入黄豆粒大小的金属钠,可能观察到的现象是___________(填字母)。
过氧化钠是重要的化工原料,具有多种用途。
(2)过氧化钠是_____________ 色固体。
(3)过氧化钠可用作呼吸面具、潜水艇的供氧剂,写出 和
和 反应的化学方程式:
反应的化学方程式:__________________ ,消耗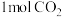 时,反应中转移的电子总数为
时,反应中转移的电子总数为__________ mol。
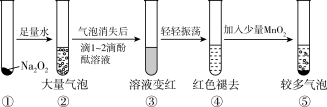
(4)某实验小组通过如图所示实验,探究 与水的反应,下列说法正确的是_________。
与水的反应,下列说法正确的是_________。
(5)向酸性 溶液中加入
溶液中加入 粉末,观察到溶液褪色,发生反应的离子方程式:
粉末,观察到溶液褪色,发生反应的离子方程式: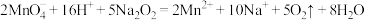
①比较氧化性强弱:
______  (选填“>”或“<”)。
(选填“>”或“<”)。
②该反应说明 具有
具有______ (选填“氧化性”或“还原性”)。
(1)向一小烧杯中分别加入等体积的水和煤油,片刻后再向该烧杯中加入黄豆粒大小的金属钠,可能观察到的现象是___________(填字母)。
A.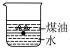 | B.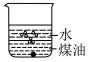 |
C.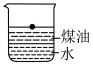 | D.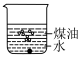 |
过氧化钠是重要的化工原料,具有多种用途。
(2)过氧化钠是
(3)过氧化钠可用作呼吸面具、潜水艇的供氧剂,写出
 和
和 反应的化学方程式:
反应的化学方程式: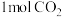 时,反应中转移的电子总数为
时,反应中转移的电子总数为(4)某实验小组通过如图所示实验,探究
 与水的反应,下列说法正确的是_________。
与水的反应,下列说法正确的是_________。
| A.②中的大量气泡主要成分是氢气 |
| B.③中溶液变红,说明有酸性物质生成 |
| C.④中现象可能是由于溶液中含有强氧化性物质造成的 |
D.⑤中 的主要作用是降低了水中氧气的溶解度 的主要作用是降低了水中氧气的溶解度 |
(5)向酸性
 溶液中加入
溶液中加入 粉末,观察到溶液褪色,发生反应的离子方程式:
粉末,观察到溶液褪色,发生反应的离子方程式: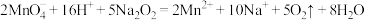
①比较氧化性强弱:

 (选填“>”或“<”)。
(选填“>”或“<”)。②该反应说明
 具有
具有
您最近一年使用:0次
解题方法
5 . 2022年11月30日,神舟十五号载人飞船与空间站组合体成功交会对接。飞船的轨道舱内安装盛有 颗粒装置,为宇航员供氧。回答下列问题:
颗粒装置,为宇航员供氧。回答下列问题:
(1)39g 中的阳离子的物质的量为
中的阳离子的物质的量为_______ 。
(2) 与
与 发生反应的化学方程式为
发生反应的化学方程式为_______ ,该反应中体现了 的性质有
的性质有_______ 。
(3) 是一种重要的工业原料,实验室需0.1mol/L的
是一种重要的工业原料,实验室需0.1mol/L的 溶液450mL,配制时应选用容量瓶的规格和称取
溶液450mL,配制时应选用容量瓶的规格和称取 的质量分别是
的质量分别是_______ (填字母)。
A.450mL,4.77g B.450mL,4.8g C.500mL,5.3g
 颗粒装置,为宇航员供氧。回答下列问题:
颗粒装置,为宇航员供氧。回答下列问题:(1)39g
 中的阳离子的物质的量为
中的阳离子的物质的量为(2)
 与
与 发生反应的化学方程式为
发生反应的化学方程式为 的性质有
的性质有(3)
 是一种重要的工业原料,实验室需0.1mol/L的
是一种重要的工业原料,实验室需0.1mol/L的 溶液450mL,配制时应选用容量瓶的规格和称取
溶液450mL,配制时应选用容量瓶的规格和称取 的质量分别是
的质量分别是A.450mL,4.77g B.450mL,4.8g C.500mL,5.3g
您最近一年使用:0次
名校
解题方法
6 . 汽车排放的尾气中一般含有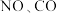 气体,两者均有毒,在催化剂作用下可以反应,生成两种无毒的气体
气体,两者均有毒,在催化剂作用下可以反应,生成两种无毒的气体 和
和 ,反应的化学方程式为
,反应的化学方程式为 (未配平)。回答下列问题:
(未配平)。回答下列问题:
(1)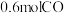 中所含原子数与
中所含原子数与_______  中所含原子数相等。
中所含原子数相等。
(2)该反应中氧化剂为_______ (填化学式),氧化产物与还原产物的质量之比为_______ (填最简整数比)。
(3)配平反应的化学方程式并用双线桥法分析反应中的电子转移:_______ 。
(4)已知:分压 总压
总压 该组分物质的量分数。标准状况
该组分物质的量分数。标准状况 下,由
下,由 和
和 组成的混合气体平均摩尔质量为
组成的混合气体平均摩尔质量为 ,则该混合气体中
,则该混合气体中 和
和 的体积比为
的体积比为_______ ,该体系中 的分压为
的分压为_______ kPa(写表达式,不需计算)。
(5)氧化还原反应可以分解成两个半反应,如 的半反应分别为
的半反应分别为还原反应  和
和氧化反应  。工业上用
。工业上用 溶液吸收
溶液吸收 尾气的离子方程式为
尾气的离子方程式为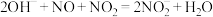 。该反应的氧化反应为
。该反应的氧化反应为_______ 。
(6)呼吸面罩中含有一种淡黄色固体,可以吸收 重新放出
重新放出 ,写出该反应的化学方程式:
,写出该反应的化学方程式:_______ 。
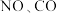 气体,两者均有毒,在催化剂作用下可以反应,生成两种无毒的气体
气体,两者均有毒,在催化剂作用下可以反应,生成两种无毒的气体 和
和 ,反应的化学方程式为
,反应的化学方程式为 (未配平)。回答下列问题:
(未配平)。回答下列问题:(1)
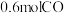 中所含原子数与
中所含原子数与 中所含原子数相等。
中所含原子数相等。(2)该反应中氧化剂为
(3)配平反应的化学方程式并用双线桥法分析反应中的电子转移:
(4)已知:分压
 总压
总压 该组分物质的量分数。标准状况
该组分物质的量分数。标准状况 下,由
下,由 和
和 组成的混合气体平均摩尔质量为
组成的混合气体平均摩尔质量为 ,则该混合气体中
,则该混合气体中 和
和 的体积比为
的体积比为 的分压为
的分压为(5)氧化还原反应可以分解成两个半反应,如
 的半反应分别为
的半反应分别为 和
和 。工业上用
。工业上用 溶液吸收
溶液吸收 尾气的离子方程式为
尾气的离子方程式为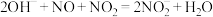 。该反应的氧化反应为
。该反应的氧化反应为(6)呼吸面罩中含有一种淡黄色固体,可以吸收
 重新放出
重新放出 ,写出该反应的化学方程式:
,写出该反应的化学方程式:
您最近一年使用:0次
名校
7 . 吸入氧气、排出二氧化碳,在遥远的太空中并不容易,因为在航天服、航天器、空间站等密闭系统中, 浓度会高得多,因此必须通过一定方法将
浓度会高得多,因此必须通过一定方法将 清除。回答下列问题:
清除。回答下列问题:
(1)我国“飞天”舱外航天服采用非再生式氢氧化锂(LiOH)吸附 生成碳酸锂。吸附时发生反应的化学方程式为
生成碳酸锂。吸附时发生反应的化学方程式为___________ 。采用 而不用
而不用 的原因是
的原因是___________ 。航天器返回地面后,用碳酸锂使 再生,该反应的化学方程式为
再生,该反应的化学方程式为___________ 。
(2)以固态胺作为吸附剂,吸附 与水蒸气。当固态胺吸附饱和后,将其暴露于真空中,破坏碳酸氢盐的化学键,释放出
与水蒸气。当固态胺吸附饱和后,将其暴露于真空中,破坏碳酸氢盐的化学键,释放出 ,从而完成吸附剂的再生。该技术大大提升了舱外航天服的续航时间。固态胺的吸附是
,从而完成吸附剂的再生。该技术大大提升了舱外航天服的续航时间。固态胺的吸附是___________ (填“化学”或“物理”)变化。
(3)早期空间站内 可用超氧化钾 (KO2)吸收,该反应的化学方程式为
可用超氧化钾 (KO2)吸收,该反应的化学方程式为___________ 。
(4)如今,空间站利用萨巴蒂尔(Sabatier)反应清除二氧化碳并再生氧气的大体流程如图所示:

①该流程的总反应方程式为___________ 。
②从元素转化角度来看,上述流程中萨巴蒂尔反应的缺点是___________ 。
 浓度会高得多,因此必须通过一定方法将
浓度会高得多,因此必须通过一定方法将 清除。回答下列问题:
清除。回答下列问题:(1)我国“飞天”舱外航天服采用非再生式氢氧化锂(LiOH)吸附
 生成碳酸锂。吸附时发生反应的化学方程式为
生成碳酸锂。吸附时发生反应的化学方程式为 而不用
而不用 的原因是
的原因是 再生,该反应的化学方程式为
再生,该反应的化学方程式为(2)以固态胺作为吸附剂,吸附
 与水蒸气。当固态胺吸附饱和后,将其暴露于真空中,破坏碳酸氢盐的化学键,释放出
与水蒸气。当固态胺吸附饱和后,将其暴露于真空中,破坏碳酸氢盐的化学键,释放出 ,从而完成吸附剂的再生。该技术大大提升了舱外航天服的续航时间。固态胺的吸附是
,从而完成吸附剂的再生。该技术大大提升了舱外航天服的续航时间。固态胺的吸附是(3)早期空间站内
 可用超氧化钾 (KO2)吸收,该反应的化学方程式为
可用超氧化钾 (KO2)吸收,该反应的化学方程式为(4)如今,空间站利用萨巴蒂尔(Sabatier)反应清除二氧化碳并再生氧气的大体流程如图所示:

①该流程的总反应方程式为
②从元素转化角度来看,上述流程中萨巴蒂尔反应的缺点是
您最近一年使用:0次
名校
8 . Ⅰ.现有下列七种物质:①CO2②过氧化钠③氧化铁 ④ 溶液 ⑤碳酸氢钠⑥
溶液 ⑤碳酸氢钠⑥ 溶液⑦次氯酸钠。请根据上述物质回答下列问题:
溶液⑦次氯酸钠。请根据上述物质回答下列问题:
(1)在上述物质中属于电解质的有_______ (填①~⑦序号)。
(2)含有0.4mol氧原子的②与足量①反应,产生气体在标准状况下的体积为_______ L。
(3)写出⑤物质的一种用途_______ 。
(4)某同学帮助水质检测站配制240mL④溶液以备使用。
①该同学应用托盘天平称取NaOH固体_______ g。
②配制过程所需的玻璃仪器有烧杯、玻璃棒、量筒、胶头滴管、_______ 。
③定容时仰视刻度线,则所配制的溶液的浓度会_______ (填“偏高”、“偏低”、“不变”)。
(5)⑤⑥两种溶液混合可以发生反应,离子方程式为_______ 。
(6)废水脱氮工艺有一种方法是在废水中加入过量⑦使 完全转化为N2,此方法可用离子方程式表示为:
完全转化为N2,此方法可用离子方程式表示为: 。用双线桥法在离子方程式上标出电子转移的方向和数目
。用双线桥法在离子方程式上标出电子转移的方向和数目_______ ;该反应中氧化剂与还原剂的物质的量之比为_______ 。
Ⅱ.神舟十三号载人飞船的成功发射离不开化学燃料。火箭分级推进所使用的燃料中含有的氧化剂主要有液氧、 和高氯酸铵
和高氯酸铵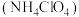 。
。
(7)写出高氯酸铵在水中的电离方程式:_______ 。
(8)载人飞船中的呼吸面具供氧剂为Na2O2,其阴、阳离子的个数比为_______ ,写出Na2O2与二氧化碳反应的化学方程式:_______ 。
 溶液 ⑤碳酸氢钠⑥
溶液 ⑤碳酸氢钠⑥ 溶液⑦次氯酸钠。请根据上述物质回答下列问题:
溶液⑦次氯酸钠。请根据上述物质回答下列问题:(1)在上述物质中属于电解质的有
(2)含有0.4mol氧原子的②与足量①反应,产生气体在标准状况下的体积为
(3)写出⑤物质的一种用途
(4)某同学帮助水质检测站配制240mL④溶液以备使用。
①该同学应用托盘天平称取NaOH固体
②配制过程所需的玻璃仪器有烧杯、玻璃棒、量筒、胶头滴管、
③定容时仰视刻度线,则所配制的溶液的浓度会
(5)⑤⑥两种溶液混合可以发生反应,离子方程式为
(6)废水脱氮工艺有一种方法是在废水中加入过量⑦使
 完全转化为N2,此方法可用离子方程式表示为:
完全转化为N2,此方法可用离子方程式表示为: 。用双线桥法在离子方程式上标出电子转移的方向和数目
。用双线桥法在离子方程式上标出电子转移的方向和数目Ⅱ.神舟十三号载人飞船的成功发射离不开化学燃料。火箭分级推进所使用的燃料中含有的氧化剂主要有液氧、
 和高氯酸铵
和高氯酸铵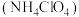 。
。(7)写出高氯酸铵在水中的电离方程式:
(8)载人飞船中的呼吸面具供氧剂为Na2O2,其阴、阳离子的个数比为
您最近一年使用:0次
名校
9 . 按要求填空:
现有以下物质:①石墨;②铝;③乙醇;④氨气;⑤液氯;⑥碳酸氢钠固体;⑦氢氧化钡溶液;⑧纯醋酸;⑨氢氧化钠固体。
(1)属于电解质的是___________ (填写序号)。
(2)写出物质⑤在水中反应的离子方程式:___________ 。
(3)40.5g某金属氯化物MCl2中含有0.6molCl-,则该氯化物的摩尔质量为___________ 。
(4)标准状况下,体积为11.2LCO2与足量Na2O2反应,生成气体的体积为___________ L,反应转移电子数为___________ (用NA表示),Na2O2中阴、阳离子个数比为___________ 。
(5)已知P2O5为酸性氧化物,可与水反应生成磷酸(H3PO4),写出P2O5与足量NaOH溶液反应的离子方程式:___________ 。
现有以下物质:①石墨;②铝;③乙醇;④氨气;⑤液氯;⑥碳酸氢钠固体;⑦氢氧化钡溶液;⑧纯醋酸;⑨氢氧化钠固体。
(1)属于电解质的是
(2)写出物质⑤在水中反应的离子方程式:
(3)40.5g某金属氯化物MCl2中含有0.6molCl-,则该氯化物的摩尔质量为
(4)标准状况下,体积为11.2LCO2与足量Na2O2反应,生成气体的体积为
(5)已知P2O5为酸性氧化物,可与水反应生成磷酸(H3PO4),写出P2O5与足量NaOH溶液反应的离子方程式:
您最近一年使用:0次
2024-01-19更新
|
61次组卷
|
2卷引用:湖北省沙市中学2023-2024学年高一上学期11月月考化学试题
名校
解题方法
10 . 为测定某含有杂质 的
的 样品的纯度,2个小组分别设计如下方案。首先准确称量样品
样品的纯度,2个小组分别设计如下方案。首先准确称量样品 ,然后,按照以下方案进行实验,请你完成相关内容:
,然后,按照以下方案进行实验,请你完成相关内容:
[方案一]:将样品与水充分反应,使产生的 通过灼热的铜粉,测得反应后生成氧化铜的质量为
通过灼热的铜粉,测得反应后生成氧化铜的质量为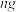 ,通过计算求出试样中
,通过计算求出试样中 的含量。
的含量。
(1) 跟水反应的离子方程式是
跟水反应的离子方程式是_______ 。
[方案二]:将样品与二氧化碳反应,通过测定反应产生氧气的体积,计算出样品中 的含量。
的含量。

(2)上图是完成该实验可能用到的实验装置,根据此实验方案,实验所使用仪器的连接次序是_______ (填写仪器编号)
(3) 跟
跟 的化学反应方程式为
的化学反应方程式为_______
(4)装置①和⑤的作用分别是_______ 和_______ 。
 的
的 样品的纯度,2个小组分别设计如下方案。首先准确称量样品
样品的纯度,2个小组分别设计如下方案。首先准确称量样品 ,然后,按照以下方案进行实验,请你完成相关内容:
,然后,按照以下方案进行实验,请你完成相关内容:[方案一]:将样品与水充分反应,使产生的
 通过灼热的铜粉,测得反应后生成氧化铜的质量为
通过灼热的铜粉,测得反应后生成氧化铜的质量为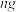 ,通过计算求出试样中
,通过计算求出试样中 的含量。
的含量。(1)
 跟水反应的离子方程式是
跟水反应的离子方程式是[方案二]:将样品与二氧化碳反应,通过测定反应产生氧气的体积,计算出样品中
 的含量。
的含量。
(2)上图是完成该实验可能用到的实验装置,根据此实验方案,实验所使用仪器的连接次序是
(3)
 跟
跟 的化学反应方程式为
的化学反应方程式为(4)装置①和⑤的作用分别是
您最近一年使用:0次



