名校
1 . 物质类别和核心元素的价态是学习元素及其化合物性质的两个重要认识视角。图为钠及其化合物的“价-类”二维图,请回答下列问题:
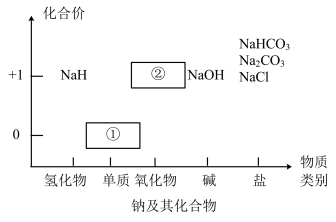
(1)淡黄色固体②用于呼吸面具,写出②和CO2的反应方程式___________ ,若有2mol的过氧化钠参与反应,转移的电子的数目为___________ 。
(2)从核心元素价态的视角看,NaH中H元素的化合价为___________ ,从H元素的价态分析,NaH常用作___________ (填“氧化剂”或“还原剂”)。
(3)纯碱和小苏打都是重要的化工原料,在生产和生活中有着广泛的应用。
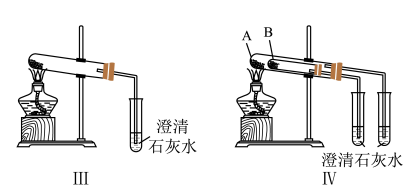
图Ⅲ、Ⅳ中___________ 能更好说明二者的稳定性(填装置序号)。Ⅳ中受热处发生反应的化学方程式:___________ 。
(4)若要除去碳酸氢钠溶液中的碳酸钠,发生反应的化学方程式为___________ 。
(5)工业上“侯氏制碱法”以NaC1、NH3、CO2及水等为原料制备纯碱,其主要反应原理为: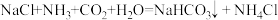 。该工艺析出的NaHCO3固体中可能含有少量氯离子杂质,检验该固体中含有氯离子杂质的操作方法是
。该工艺析出的NaHCO3固体中可能含有少量氯离子杂质,检验该固体中含有氯离子杂质的操作方法是___________ 。
(6)下列实验方案中,不能测定出Na2CO3和NaHCO3的混合物中碳酸钠质量分数的是___________。

(1)淡黄色固体②用于呼吸面具,写出②和CO2的反应方程式
(2)从核心元素价态的视角看,NaH中H元素的化合价为
(3)纯碱和小苏打都是重要的化工原料,在生产和生活中有着广泛的应用。

图Ⅲ、Ⅳ中
(4)若要除去碳酸氢钠溶液中的碳酸钠,发生反应的化学方程式为
(5)工业上“侯氏制碱法”以NaC1、NH3、CO2及水等为原料制备纯碱,其主要反应原理为:
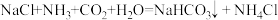 。该工艺析出的NaHCO3固体中可能含有少量氯离子杂质,检验该固体中含有氯离子杂质的操作方法是
。该工艺析出的NaHCO3固体中可能含有少量氯离子杂质,检验该固体中含有氯离子杂质的操作方法是(6)下列实验方案中,不能测定出Na2CO3和NaHCO3的混合物中碳酸钠质量分数的是___________。
| A.取ag混合物充分加热,质量减少bg。 |
| B.取ag混合物与足量稀盐酸充分反应,师热、蒸干、灼烧,得到bg固体。 |
| C.取ag混合物与足量NaOH溶液充分反应得到bg溶液 |
| D.与足量稀硫酸充分反应,逸出气体经干燥后用碱石灰吸收,质量增加bg |
您最近一年使用:0次
名校
解题方法
2 . 下图中,A是单质,B、C、D在灼烧时,火焰均为黄色。

(1)写出下列转化的化学方程式:
①A→B___________ 。
②B→D___________ 。
③A→C___________ 。
(2)请写出E的一种用途:___________ 。
(3)将少量A投入滴有酚酞溶液的水的烧杯中,并将观察到的现象与相关解释填入下表:

(1)写出下列转化的化学方程式:
①A→B
②B→D
③A→C
(2)请写出E的一种用途:
(3)将少量A投入滴有酚酞溶液的水的烧杯中,并将观察到的现象与相关解释填入下表:
| 现象 | 解释 |
| 钠熔化成小球并在液面上游动 | 因为金属钠的熔点低且与水反应放热,故熔化成小球。又因金属钠密度比水小,故在液面上。金属钠与水反应生成氢气,故会四处游动。 |
| 发出嘶嘶的响声 | 氢气与空气中的氧气在加热条件下反应发出爆鸣声,故有嘶嘶的声响。 |
您最近一年使用:0次
名校
3 . Ⅰ.现有下列七种物质:①CO2②过氧化钠③氧化铁 ④ 溶液 ⑤碳酸氢钠⑥
溶液 ⑤碳酸氢钠⑥ 溶液⑦次氯酸钠。请根据上述物质回答下列问题:
溶液⑦次氯酸钠。请根据上述物质回答下列问题:
(1)在上述物质中属于电解质的有_______ (填①~⑦序号)。
(2)含有0.4mol氧原子的②与足量①反应,产生气体在标准状况下的体积为_______ L。
(3)写出⑤物质的一种用途_______ 。
(4)某同学帮助水质检测站配制240mL④溶液以备使用。
①该同学应用托盘天平称取NaOH固体_______ g。
②配制过程所需的玻璃仪器有烧杯、玻璃棒、量筒、胶头滴管、_______ 。
③定容时仰视刻度线,则所配制的溶液的浓度会_______ (填“偏高”、“偏低”、“不变”)。
(5)⑤⑥两种溶液混合可以发生反应,离子方程式为_______ 。
(6)废水脱氮工艺有一种方法是在废水中加入过量⑦使 完全转化为N2,此方法可用离子方程式表示为:
完全转化为N2,此方法可用离子方程式表示为: 。用双线桥法在离子方程式上标出电子转移的方向和数目
。用双线桥法在离子方程式上标出电子转移的方向和数目_______ ;该反应中氧化剂与还原剂的物质的量之比为_______ 。
Ⅱ.神舟十三号载人飞船的成功发射离不开化学燃料。火箭分级推进所使用的燃料中含有的氧化剂主要有液氧、 和高氯酸铵
和高氯酸铵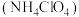 。
。
(7)写出高氯酸铵在水中的电离方程式:_______ 。
(8)载人飞船中的呼吸面具供氧剂为Na2O2,其阴、阳离子的个数比为_______ ,写出Na2O2与二氧化碳反应的化学方程式:_______ 。
 溶液 ⑤碳酸氢钠⑥
溶液 ⑤碳酸氢钠⑥ 溶液⑦次氯酸钠。请根据上述物质回答下列问题:
溶液⑦次氯酸钠。请根据上述物质回答下列问题:(1)在上述物质中属于电解质的有
(2)含有0.4mol氧原子的②与足量①反应,产生气体在标准状况下的体积为
(3)写出⑤物质的一种用途
(4)某同学帮助水质检测站配制240mL④溶液以备使用。
①该同学应用托盘天平称取NaOH固体
②配制过程所需的玻璃仪器有烧杯、玻璃棒、量筒、胶头滴管、
③定容时仰视刻度线,则所配制的溶液的浓度会
(5)⑤⑥两种溶液混合可以发生反应,离子方程式为
(6)废水脱氮工艺有一种方法是在废水中加入过量⑦使
 完全转化为N2,此方法可用离子方程式表示为:
完全转化为N2,此方法可用离子方程式表示为: 。用双线桥法在离子方程式上标出电子转移的方向和数目
。用双线桥法在离子方程式上标出电子转移的方向和数目Ⅱ.神舟十三号载人飞船的成功发射离不开化学燃料。火箭分级推进所使用的燃料中含有的氧化剂主要有液氧、
 和高氯酸铵
和高氯酸铵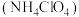 。
。(7)写出高氯酸铵在水中的电离方程式:
(8)载人飞船中的呼吸面具供氧剂为Na2O2,其阴、阳离子的个数比为
您最近一年使用:0次
名校
4 . 下列物质的性质与用途具有对应关系的是
| A.二氧化氯具有强氧化性,可用来漂白织物 | B. 能与酸反应,可用于去除油脂 能与酸反应,可用于去除油脂 |
| C.碳酸钠受热分解,可用作食品膨松剂 | D. 是淡黄色固体,在呼吸面具中用作供氧剂 是淡黄色固体,在呼吸面具中用作供氧剂 |
您最近一年使用:0次
名校
5 . 下列有关物质的性质与用途具有对应关系的是
| A.钠具有还原性,液态钠可用作核反应堆的传热介质 |
B. 具有氧化性,可用于蚀刻铜电路板 具有氧化性,可用于蚀刻铜电路板 |
| C.单晶硅熔点高,可用作半导体材料 |
D. 具有漂白性,可在呼吸面具中作为氧气的来源 具有漂白性,可在呼吸面具中作为氧气的来源 |
您最近一年使用:0次
名校
解题方法
6 . 宇航员出舱时呼吸所需氧气主要来自太空服中的呼吸面具。下列反应均能产生氧气,其中最适宜用于呼吸面具中提供氧的反应是
| A.4HNO3=4NO2↑+O2↑+2H2O | B.2H2O2=2H2O+O2↑ |
| C.2CO2+2Na2O2=2Na2CO3+O2 | D.2KClO3=2KCl+3O2↑ |
您最近一年使用:0次
名校
7 . 下列物质与其用途相符合的是
① ——制消毒剂 ②
——制消毒剂 ② ——制胶卷、感光纸 ③碘——预防甲状腺肿大
——制胶卷、感光纸 ③碘——预防甲状腺肿大
④碳酸氢钠——发酵粉 ⑤ ——呼吸面具中的供氧剂 ⑥
——呼吸面具中的供氧剂 ⑥ -漂白纺织物
-漂白纺织物
①
 ——制消毒剂 ②
——制消毒剂 ② ——制胶卷、感光纸 ③碘——预防甲状腺肿大
——制胶卷、感光纸 ③碘——预防甲状腺肿大④碳酸氢钠——发酵粉 ⑤
 ——呼吸面具中的供氧剂 ⑥
——呼吸面具中的供氧剂 ⑥ -漂白纺织物
-漂白纺织物| A.②③⑤⑥ | B.①②③⑤⑥ | C.①②③④⑤ | D.全部 |
您最近一年使用:0次
名校
解题方法
8 . 下列说法错误的是
A. 和 和 中阳离子、阴离子个数比都为2:1 中阳离子、阴离子个数比都为2:1 |
B. 和 和 都是碱性氧化物 都是碱性氧化物 |
C. 和 和 长期露置于空气中最终所得固体产物相同 长期露置于空气中最终所得固体产物相同 |
D. 分别与 分别与 和 和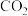 反应生成 反应生成 时,转移的电子数都为2NA 时,转移的电子数都为2NA |
您最近一年使用:0次
名校
解题方法
9 . 下列物质的应用中,利用了氧化还原反应的是
| A.用KOH溶液捕集吸收大气中的CO2 |
| B.用盐酸去除铁锈(主要成分Fe2O3·xH2O) |
C.用 作为呼吸面具或潜水艇中氧气的来源 作为呼吸面具或潜水艇中氧气的来源 |
D.用NaOH溶液除去 薄膜 薄膜 |
您最近一年使用:0次
名校
10 . 下列选项所示的物质间转化不能一步实现的是
| A.Na2O2→Na2CO3 | B.Cl2→Ca(ClO)2 | C.FeCl3→FeCl2 | D.S→SO3 |
您最近一年使用:0次



