名校
1 . 我国化学家侯德榜发明了联合制碱法,对世界制碱工业做出了巨大贡献。联合制碱法的主要流程如下(部分物质已略去):
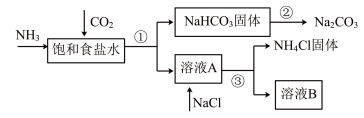
(1)①~③所涉及的操作方法中,包含过滤的是___________ (填序号)。
(2)根据上述流程图,将化学方程式补充完整:________
NH3+CO2+___________+___________=NaHCO3↓+NH4Cl
(3)煅烧NaHCO3固体的化学方程式是___________ 。
(4)下列联合制碱法流程说法正确的是___________ (填字母)。
a.CO2可以循环使用
b.副产物NH4Cl可用作肥料
c.溶液B中一定含有Na+、NH 、Cl-
、Cl-
d.①中NaHCO3析出是因为一定条件下NaHCO3的溶解度最小
(5)某纯碱样品中含杂质NaCl,取质量为ag的样品,加入足量的稀盐酸,充分反应后,加热、蒸干、灼烧,得到bg固体物质,则此样品中Na2CO3的质量分数为___________ 。(列出表达式即可)

(1)①~③所涉及的操作方法中,包含过滤的是
(2)根据上述流程图,将化学方程式补充完整:
NH3+CO2+___________+___________=NaHCO3↓+NH4Cl
(3)煅烧NaHCO3固体的化学方程式是
(4)下列联合制碱法流程说法正确的是
a.CO2可以循环使用
b.副产物NH4Cl可用作肥料
c.溶液B中一定含有Na+、NH
 、Cl-
、Cl-d.①中NaHCO3析出是因为一定条件下NaHCO3的溶解度最小
(5)某纯碱样品中含杂质NaCl,取质量为ag的样品,加入足量的稀盐酸,充分反应后,加热、蒸干、灼烧,得到bg固体物质,则此样品中Na2CO3的质量分数为
您最近一年使用:0次
名校
解题方法
2 . 我国化学家侯德榜发明了联合制碱法,对世界制碱工业做出了巨大贡献。联合制碱法的主要过程如图所示(部分物质已略去)。

(1)① ~ ③所涉及的操作方法中,包含过滤的是______ (填序号)。
(2)根据图,将化学方程式补充完整:NH3+CO2+______ +______ = NaHCO3 ↓+ NH4Cl
(3)煅烧NaHCO3固体的化学方程式是______ 。
(4)下列说法中,正确的是______ (填字母)。
a.CO2可循环使用
b.副产物NH4Cl可用作肥料
c.溶液B中一定含有Na+、NH 、Cl-
、Cl-
(5)若检验溶液B中是否含有氯离子,可进行的操作方法是_____________________ 。
(6)在下列方程式上写出缺少的物质并配平方程式,用双线桥分析反应①的电子转移
①___ Na2Cr2O7 + _____ HCl — ___ NaCl + ___ CrCl3 + ___ Cl2 +______________
② ___ ClO + _____ CrO
+ _____ CrO + _______ — ___ Cl- + ___ CrO
+ _______ — ___ Cl- + ___ CrO + ___H2O
+ ___H2O___________

(1)① ~ ③所涉及的操作方法中,包含过滤的是
(2)根据图,将化学方程式补充完整:NH3+CO2+
(3)煅烧NaHCO3固体的化学方程式是
(4)下列说法中,正确的是
a.CO2可循环使用
b.副产物NH4Cl可用作肥料
c.溶液B中一定含有Na+、NH
 、Cl-
、Cl-(5)若检验溶液B中是否含有氯离子,可进行的操作方法是
(6)在下列方程式上写出缺少的物质并配平方程式,用双线桥分析反应①的电子转移
①___ Na2Cr2O7 + _____ HCl — ___ NaCl + ___ CrCl3 + ___ Cl2 +___
② ___ ClO
 + _____ CrO
+ _____ CrO + _______ — ___ Cl- + ___ CrO
+ _______ — ___ Cl- + ___ CrO + ___H2O
+ ___H2O
您最近一年使用:0次
2022-11-10更新
|
275次组卷
|
2卷引用:北京市西城外国语学校2022-2023学年高一上学期期中考试化学试题
解题方法
3 . 碳酸氢钠属于抗酸药,用于碱化尿液及酸血症,也可用于胃酸过多,在潮湿空气中缓缓分解。某化学小组用如下方法对某品牌碳酸氢钠片中的含量进行了探究(可能含有少量Na2CO3,药品中不含干扰测定的物质)。
【鉴别】
a.取铂丝,用盐酸湿润后,蘸取药品粉末,在无色火焰中燃烧,火焰显黄色。
b.向本品水溶液中加盐酸产生泡沸现象。
【检查】配置药品质量分数为0.8%的水溶液,测pH为8.3。
【含量测定】小组采用滴定法进行含量测定:
I.用已准确称量的药品固体ag配制一定体积的溶液VmL。(此时主要溶质为NaHCO3和少量Na2CO3)
II.取V1mL上述溶液于锥形瓶中,加入酚酞指示剂2—3滴。
III.用1mol/L盐酸标准溶液滴定II中溶液至第一终点时,消耗盐酸溶液V2mL。 (此时溶质为NaCl和NaHCO3)
IV.再向锥形瓶内滴加2滴甲基橙,继续用HCl标准溶液滴定至第二终点,又消耗盐酸溶液V3mL。
已知:H2CO3的电离平衡常数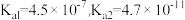 ;
;
常用的酸碱指示剂及其变色范围如下:
酚酞:pH<8.2无色、8.2<pH<10浅红色、pH>10红色
甲基橙:pH<3.1红色、3.1<pH<4.4橙色、pH>4.4黄色
(1)请写出“鉴别”中产生泡沸现象主要反应的离子反应方程式:_______ 。
(2)请结合化学用语解释“检查”中水溶液pH为8.3的主要原因(不考虑杂质影响):_______ 。
(3)“含量测定”的步骤I中配制溶液用到的玻璃仪器有烧杯、玻璃棒、胶头滴管和_______ 。
(4)滴定过程中应选择如图所示滴定管_______ (填字母)。

(5)步骤V中第二步滴定用甲基橙滴定至终点的现象是由_______ 色变为橙色。
(6)药品中碳酸氢钠的质量分数为_______ 。(碳酸氢钠摩尔质量: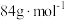 )
)
【鉴别】
a.取铂丝,用盐酸湿润后,蘸取药品粉末,在无色火焰中燃烧,火焰显黄色。
b.向本品水溶液中加盐酸产生泡沸现象。
【检查】配置药品质量分数为0.8%的水溶液,测pH为8.3。
【含量测定】小组采用滴定法进行含量测定:
I.用已准确称量的药品固体ag配制一定体积的溶液VmL。(此时主要溶质为NaHCO3和少量Na2CO3)
II.取V1mL上述溶液于锥形瓶中,加入酚酞指示剂2—3滴。
III.用1mol/L盐酸标准溶液滴定II中溶液至第一终点时,消耗盐酸溶液V2mL。 (此时溶质为NaCl和NaHCO3)
IV.再向锥形瓶内滴加2滴甲基橙,继续用HCl标准溶液滴定至第二终点,又消耗盐酸溶液V3mL。
已知:H2CO3的电离平衡常数
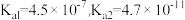 ;
;常用的酸碱指示剂及其变色范围如下:
酚酞:pH<8.2无色、8.2<pH<10浅红色、pH>10红色
甲基橙:pH<3.1红色、3.1<pH<4.4橙色、pH>4.4黄色
(1)请写出“鉴别”中产生泡沸现象主要反应的离子反应方程式:
(2)请结合化学用语解释“检查”中水溶液pH为8.3的主要原因(不考虑杂质影响):
(3)“含量测定”的步骤I中配制溶液用到的玻璃仪器有烧杯、玻璃棒、胶头滴管和
(4)滴定过程中应选择如图所示滴定管

(5)步骤V中第二步滴定用甲基橙滴定至终点的现象是由
(6)药品中碳酸氢钠的质量分数为
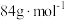 )
)
您最近一年使用:0次
4 . 乙醇俗称酒精,在生活中使用广泛。
资料1:乙醇分子有两个末端,一端是憎水(易溶于油)的—C2H5;一端是亲水(易溶于水)的—OH。
资料2:破坏蛋白质分子中形成蜷曲和螺旋的各种力,使长链舒展、松弛,可导致蛋白质变性。
资料3:水分子可以松弛蛋白质外部亲水基团之间的吸引力,而—OH不能;—C2H5可以破坏蛋白质内部憎水基团之间的吸引力。
(1)乙醇的结构及性质
①1mol乙醇分子中的极性共价键有___________ mol。
②从结构角度解释乙醇的沸点比乙烷高的原因____________________ 。
(2)乙醇的用途
①医用酒精(75%)制备过程与制酒的过程类似,不能饮用,但可接触人体医用。

结合题中资料,下列说法正确的是________________ (填字母)。
a.糖化、发酵的过程均含有化学变化
b.获得医用酒精常采用的分离提纯方法是蒸馏
c.浓度99%的酒精消毒杀菌效果一定大于75%的酒精
②乙醇是一种很好的溶剂,在油脂的皂化反应中,加入乙醇可加快反应速率,其原因是______________ 。
(3)乙醇的工业制取
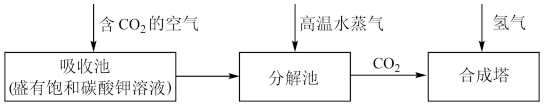
乙醇的工业制取方法很多,由碳的氧化物直接合成乙醇燃料已进入大规模生产。下图是由二氧化碳合成乙
醇的工艺流程。
该流程中能循环使用的物质是_________________________ 。
资料1:乙醇分子有两个末端,一端是憎水(易溶于油)的—C2H5;一端是亲水(易溶于水)的—OH。
资料2:破坏蛋白质分子中形成蜷曲和螺旋的各种力,使长链舒展、松弛,可导致蛋白质变性。
资料3:水分子可以松弛蛋白质外部亲水基团之间的吸引力,而—OH不能;—C2H5可以破坏蛋白质内部憎水基团之间的吸引力。
(1)乙醇的结构及性质
①1mol乙醇分子中的极性共价键有
②从结构角度解释乙醇的沸点比乙烷高的原因
(2)乙醇的用途
①医用酒精(75%)制备过程与制酒的过程类似,不能饮用,但可接触人体医用。

结合题中资料,下列说法正确的是
a.糖化、发酵的过程均含有化学变化
b.获得医用酒精常采用的分离提纯方法是蒸馏
c.浓度99%的酒精消毒杀菌效果一定大于75%的酒精
②乙醇是一种很好的溶剂,在油脂的皂化反应中,加入乙醇可加快反应速率,其原因是
(3)乙醇的工业制取
乙醇的工业制取方法很多,由碳的氧化物直接合成乙醇燃料已进入大规模生产。下图是由二氧化碳合成乙
醇的工艺流程。

该流程中能循环使用的物质是
您最近一年使用:0次



