名校
解题方法
1 . 科学家设计出烧碱溶液捕捉CO2法,原理如图所示:___________ 。
(2)上述流程中,被循环利用的物质有CaO和NaOH,请说明NaOH循环利用的途径。___________
(3)如下为产生CO2气体的体积与消耗HCl物质的量的关系图。现向流程中 和
和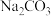 的混合液中逐滴加入稀盐酸,其中可能正确的是
的混合液中逐滴加入稀盐酸,其中可能正确的是___________ 。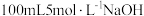 溶液,理论上最多可吸收CO2
溶液,理论上最多可吸收CO2_______ mol;此时溶液中的溶质的电离方程式为:___________ 。若喷洒完上述NaOH溶液后,测得吸收液中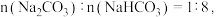 则被吸收的CO2在标准状况下的体积为
则被吸收的CO2在标准状况下的体积为___________ L。
(5)实验室中,有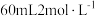 的NaOH溶液和盛有足量CO2的气体钢瓶,要制备得到纯度最大的
的NaOH溶液和盛有足量CO2的气体钢瓶,要制备得到纯度最大的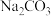 溶液,具体的实验步骤为:(实验可供选择仪器:烧杯、量筒、试管、胶头滴管、乳胶管、导管)
溶液,具体的实验步骤为:(实验可供选择仪器:烧杯、量筒、试管、胶头滴管、乳胶管、导管)___________ 。
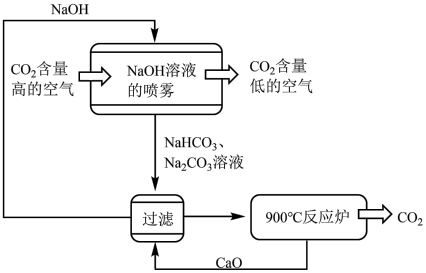
(2)上述流程中,被循环利用的物质有CaO和NaOH,请说明NaOH循环利用的途径。
(3)如下为产生CO2气体的体积与消耗HCl物质的量的关系图。现向流程中
 和
和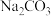 的混合液中逐滴加入稀盐酸,其中可能正确的是
的混合液中逐滴加入稀盐酸,其中可能正确的是
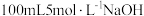 溶液,理论上最多可吸收CO2
溶液,理论上最多可吸收CO2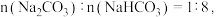 则被吸收的CO2在标准状况下的体积为
则被吸收的CO2在标准状况下的体积为(5)实验室中,有
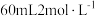 的NaOH溶液和盛有足量CO2的气体钢瓶,要制备得到纯度最大的
的NaOH溶液和盛有足量CO2的气体钢瓶,要制备得到纯度最大的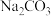 溶液,具体的实验步骤为:(实验可供选择仪器:烧杯、量筒、试管、胶头滴管、乳胶管、导管)
溶液,具体的实验步骤为:(实验可供选择仪器:烧杯、量筒、试管、胶头滴管、乳胶管、导管)
您最近一年使用:0次
名校
解题方法
2 . 取一定体积且物质量浓度相同的两种试剂进行反应.改变两种试剂的滴加顺序,反应现象明显不同的是
选项 | 试剂① | 试剂② |
A | 硫酸 | 氢氧化钡溶液 |
B |
|
|
C |
|
|
D |
|
|
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
3 . 下列有关物质性质及对应用途的描述均正确的是
A. 溶液具有碱性,可用于治疗胃酸过多 溶液具有碱性,可用于治疗胃酸过多 |
B. 结构性质稳定,可用作工业冶炼镁的保护气 结构性质稳定,可用作工业冶炼镁的保护气 |
| C.Al属于活泼金属,常温下,用铝制容器盛装浓硫酸 |
D. 是酸性氧化物,可用作于信息产业中光导纤维传输信号 是酸性氧化物,可用作于信息产业中光导纤维传输信号 |
您最近一年使用:0次
解题方法
4 . 某食品膨松剂中发挥作用的物质为 ,某兴趣小组研究加热情况下该膨松剂放出气体的量,设计实验的装置图如下。
,某兴趣小组研究加热情况下该膨松剂放出气体的量,设计实验的装置图如下。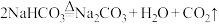
回答下列问题:
(1)A装置中NaOH溶液的作用是除去空气中的______ ,C装置内所盛试剂是______ ,E装置的作用是______ ,若没有E装置,测定的结果______ (填“偏高”、“偏低”或“无影响”)。
(2)充分加热后,测得D的质量增加6.6g,若装置B换为装置F进行实验(膨松剂质量相同)。不考虑导致误差因素,则测得D的质量增加______ 。
(3)分解产物 是重要化工原料,研究其性质:分别取少量
是重要化工原料,研究其性质:分别取少量 溶液,
溶液,
①与碱反应:滴加澄清石灰水,现象为______ 。
②与盐反应:滴加X溶液,产生白色沉淀,则X可能为______ (写其中一种的名称)。
③与酸反应:滴加盐酸,开始没有气泡,反应产生两种盐,推测两种盐的化学式______ 。
 ,某兴趣小组研究加热情况下该膨松剂放出气体的量,设计实验的装置图如下。
,某兴趣小组研究加热情况下该膨松剂放出气体的量,设计实验的装置图如下。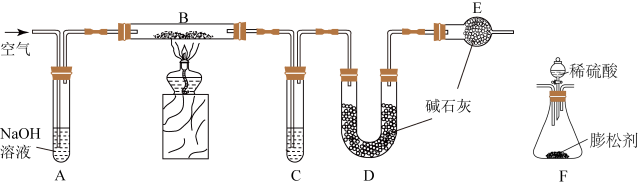
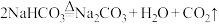
回答下列问题:
(1)A装置中NaOH溶液的作用是除去空气中的
(2)充分加热后,测得D的质量增加6.6g,若装置B换为装置F进行实验(膨松剂质量相同)。不考虑导致误差因素,则测得D的质量增加
(3)分解产物
 是重要化工原料,研究其性质:分别取少量
是重要化工原料,研究其性质:分别取少量 溶液,
溶液,①与碱反应:滴加澄清石灰水,现象为
②与盐反应:滴加X溶液,产生白色沉淀,则X可能为
③与酸反应:滴加盐酸,开始没有气泡,反应产生两种盐,推测两种盐的化学式
您最近一年使用:0次
名校
5 . 已知X、Y和Z为中学化学中的常见元素﹐根据如图所示转化关系(反应条件及部分产物已略去)。回答下列问题:

(1)若A、B、C、D均为含X的化合物。A常用作制冷剂,D是一种强酸,则
①反应I的化学方程式为___________ 。
②常温下,C的颜色为___________ 色。
③足量的铜与一定量的D的浓溶液充分反应,向所得溶液中加入100mL 4 NaOH溶液,
NaOH溶液, 恰好沉淀完全。则消耗铜的质量为
恰好沉淀完全。则消耗铜的质量为___________ g。
(2)若A、B、C、D均为含Y的化合物。A是一元强碱且焰色为黄色,E是“碳中和”的主角,则B的化学式为___________ ;C的用途有___________ (任写一种);E的空间结构为___________ 。
(3)若A、B、C、D均为含Z的化合物。A为黄铁矿的主要成分,D为强酸,则
①A在空气中煅烧生成氧化铁的化学方程式为___________ 。
②C→D的过程中选择用98.3%的浓硫酸吸收而不用 吸收的原因是
吸收的原因是___________ 。

(1)若A、B、C、D均为含X的化合物。A常用作制冷剂,D是一种强酸,则
①反应I的化学方程式为
②常温下,C的颜色为
③足量的铜与一定量的D的浓溶液充分反应,向所得溶液中加入100mL 4
 NaOH溶液,
NaOH溶液, 恰好沉淀完全。则消耗铜的质量为
恰好沉淀完全。则消耗铜的质量为(2)若A、B、C、D均为含Y的化合物。A是一元强碱且焰色为黄色,E是“碳中和”的主角,则B的化学式为
(3)若A、B、C、D均为含Z的化合物。A为黄铁矿的主要成分,D为强酸,则
①A在空气中煅烧生成氧化铁的化学方程式为
②C→D的过程中选择用98.3%的浓硫酸吸收而不用
 吸收的原因是
吸收的原因是
您最近一年使用:0次
解题方法
6 . 下列离子方程式正确的是
| A.向FeI2的溶液中通少量氯气: 2Fe2++2I- +2Cl2=2Fe3++I2+4Cl- |
B.NaHCO3溶液中加少量Ba(OH)2溶液: +Ba2++OH-=BaCO3↓+H2O +Ba2++OH-=BaCO3↓+H2O |
| C.氢氧化铝与盐酸反应:Al(OH)3+3H+= Al3++3H2O |
D.硫酸铜溶液与氢氧化钡溶液反应: +Ba2+=BaSO4↓ +Ba2+=BaSO4↓ |
您最近一年使用:0次
7 . 现有下列5种与生产生活相关的物质。
①碳酸氢钠②浓硫酸③氧化铁④次氯酸钠⑤四氧化三铁
(1)常用作油漆、涂料的红色颜料的是_______ (填序号)。
(2)用作治疗胃酸的是_______ (填序号)。
(3)84消毒液的主要成分是_______ (填序号)。
(4)具有磁性的是_______ (填序号)。
(5)能作干燥剂的是_______ (填序号)。
①碳酸氢钠②浓硫酸③氧化铁④次氯酸钠⑤四氧化三铁
(1)常用作油漆、涂料的红色颜料的是
(2)用作治疗胃酸的是
(3)84消毒液的主要成分是
(4)具有磁性的是
(5)能作干燥剂的是
您最近一年使用:0次
名校
解题方法
8 . 在给定条件下,下列选项所示的物质间转化不能一步实现的
A. |
B.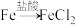 溶液 溶液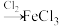 溶液 溶液 |
C.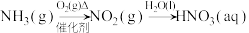 |
D.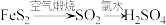 |
您最近一年使用:0次
名校
解题方法
9 . 我国化工专家侯德榜提出将氨碱法与合成氨联合生产的改进工艺,这就是联合制碱法,也称侯氏制碱法。侯氏制碱法的工业生产分为两个过程,分别为生产纯碱的制碱过程和生产氯化铵的制氨过程。工艺流程如下:
(1)“产品1”的化学式为___________ ,“过滤”后得到“产品1”的方法为___________ ,写出“产品2”的一种常见用途___________ 。
(2)写出“碳化”时发生反应的化学方程式___________
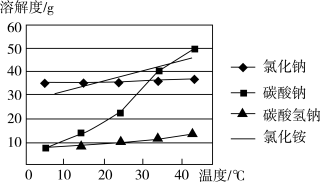
(3)采用“冷析”分离出产品2的原因是___________
(4)关于“母液1”的说法正确的是___________ (填序号)。
A.“母液1”中主要含有 、
、 、
、 、
、
B.“母液1”与“母液2”成分相同
C.“母液1”中溶质只有氯化铵
(5)研究表明,“吸氨2”不仅可以促进“产品2”的分离还可以减少某种杂质的析出,写出“吸氨2”中反应的离子方程式___________ 。

(1)“产品1”的化学式为
(2)写出“碳化”时发生反应的化学方程式
(3)采用“冷析”分离出产品2的原因是
(4)关于“母液1”的说法正确的是
A.“母液1”中主要含有
 、
、 、
、 、
、
B.“母液1”与“母液2”成分相同
C.“母液1”中溶质只有氯化铵
(5)研究表明,“吸氨2”不仅可以促进“产品2”的分离还可以减少某种杂质的析出,写出“吸氨2”中反应的离子方程式
您最近一年使用:0次
解题方法
10 . 下列混合物分离(或除杂)的方法正确的是
| A.除去Mg粉中的Al粉:加入足量NaOH溶液后,过滤、洗涤 |
| B.除去BaCO3固体中混有的BaSO4:加入过量盐酸后,过滤、洗涤 |
| C.除去NaHCO3溶液中的Na2CO3:加入适量稀盐酸 |
| D.除去Al2O3中的少量Fe2O3:加入过量氢氧化钠溶液,过滤、洗涤 |
您最近一年使用:0次

 溶液
溶液 溶液
溶液 溶液
溶液 溶液
溶液 溶液
溶液

