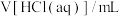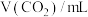名校
解题方法
1 . 现有 和
和 的固体混合物10g,加热至质量不再改变,剩余固体质量为9.38g,
的固体混合物10g,加热至质量不再改变,剩余固体质量为9.38g, 的质量分数为
的质量分数为___________ ?若参考值为0.850,则相对偏差为___________ ?请写出以上两个数据的计算过程。
 和
和 的固体混合物10g,加热至质量不再改变,剩余固体质量为9.38g,
的固体混合物10g,加热至质量不再改变,剩余固体质量为9.38g, 的质量分数为
的质量分数为
您最近一年使用:0次
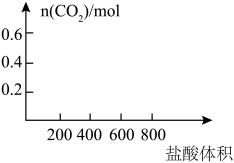
2 . 将35.8gNa2CO3和NaHCO3的固体混合物溶于足量水中,向其中逐滴加入1mol·L-1的盐酸至不再产生气体为止,测得共产生CO28.96L(标准状况)(气体溶解忽略不计)。回答下列问题:
(1)原混合物中Na2CO3为___________ g。
(2)若以滴加盐酸的体积为V(mL),产生气体的物质的量为n(mol),建立n=f(V)的函数关系,将V在不同取值范围时,n=f(V)的关系式填入下表并作图。
___________
(1)原混合物中Na2CO3为
(2)若以滴加盐酸的体积为V(mL),产生气体的物质的量为n(mol),建立n=f(V)的函数关系,将V在不同取值范围时,n=f(V)的关系式填入下表并作图。
| V的取值范围 | n=f(V) |
您最近一年使用:0次
名校
3 . 向某NaOH溶液分别通入不同量的 气体,得到A、B、C三种溶液。分别向这三种溶液中滴入
气体,得到A、B、C三种溶液。分别向这三种溶液中滴入 的盐酸,得到的气体变化如图。则:
的盐酸,得到的气体变化如图。则:_____ ;
(2)C溶液中有两种溶质,除去其中碱性强的溶质的方法为:_____ 。
(3)B溶液中原有的NaOH的物质的量为_____ 。
 气体,得到A、B、C三种溶液。分别向这三种溶液中滴入
气体,得到A、B、C三种溶液。分别向这三种溶液中滴入 的盐酸,得到的气体变化如图。则:
的盐酸,得到的气体变化如图。则: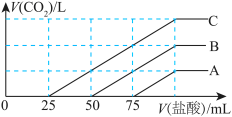
(2)C溶液中有两种溶质,除去其中碱性强的溶质的方法为:
(3)B溶液中原有的NaOH的物质的量为
您最近一年使用:0次
4 . 某干燥白色固体可能含有 、
、 、
、 中的几种,取一定质量的该固体加蒸馏水配制
中的几种,取一定质量的该固体加蒸馏水配制 溶液,并向该溶液中滴加
溶液,并向该溶液中滴加 的盐酸,得到
的盐酸,得到 体积(标准状况下)与盐酸体积的关系如图所示。回答下列问题:
体积(标准状况下)与盐酸体积的关系如图所示。回答下列问题:
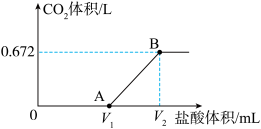
(1)产生的 的物质的量为
的物质的量为______________  ,
, 段反应的离子方程式为
段反应的离子方程式为____________________ 。
(2)若白色固体由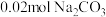 和
和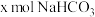 组成,则
组成,则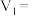
___________ ,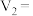
___________ 。
(3)若白色固体由 和
和 组成,
组成, ,则
,则 与
与 溶于水后发生反应的离子方程式为
溶于水后发生反应的离子方程式为_______________________________ ,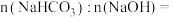
_________________ 。
(4)若白色固体只由 和
和 组成,且
组成,且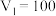 ,
, ,则
,则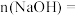
__________  ,原
,原 溶液中的
溶液中的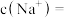
_______________  。
。
(5)另取某 和
和 组成的混合物样品,称取3份该样品溶于水后分别逐滴加入相同浓度盐酸
组成的混合物样品,称取3份该样品溶于水后分别逐滴加入相同浓度盐酸 ,充分反应,产生
,充分反应,产生 的体积如下表(标准状况下,且不考虑
的体积如下表(标准状况下,且不考虑 在水中的溶解):
在水中的溶解):
样品中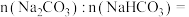
__________________ ,盐酸的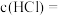
_______________  。
。
 、
、 、
、 中的几种,取一定质量的该固体加蒸馏水配制
中的几种,取一定质量的该固体加蒸馏水配制 溶液,并向该溶液中滴加
溶液,并向该溶液中滴加 的盐酸,得到
的盐酸,得到 体积(标准状况下)与盐酸体积的关系如图所示。回答下列问题:
体积(标准状况下)与盐酸体积的关系如图所示。回答下列问题:
(1)产生的
 的物质的量为
的物质的量为 ,
, 段反应的离子方程式为
段反应的离子方程式为(2)若白色固体由
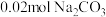 和
和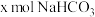 组成,则
组成,则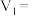
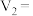
(3)若白色固体由
 和
和 组成,
组成, ,则
,则 与
与 溶于水后发生反应的离子方程式为
溶于水后发生反应的离子方程式为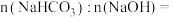
(4)若白色固体只由
 和
和 组成,且
组成,且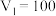 ,
, ,则
,则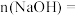
 ,原
,原 溶液中的
溶液中的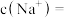
 。
。(5)另取某
 和
和 组成的混合物样品,称取3份该样品溶于水后分别逐滴加入相同浓度盐酸
组成的混合物样品,称取3份该样品溶于水后分别逐滴加入相同浓度盐酸 ,充分反应,产生
,充分反应,产生 的体积如下表(标准状况下,且不考虑
的体积如下表(标准状况下,且不考虑 在水中的溶解):
在水中的溶解):实验序号 | ① | ② | ③ |
| 100.0 | 100.0 | 100.0 |
| 3.80 | 7.60 | 11.40 |
| 896 | 1344 | 896 |
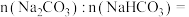
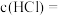
 。
。
您最近一年使用:0次
名校
5 . 将Na2CO3和NaHCO3的混合物3.27 g加热到质量不再减轻时,测得残留固体2.65 g。另取相同质量的此混合物固体,跟 100 mL某浓度的盐酸刚好完全反应生成NaCl,求;
(1)此混合物中NaHCO3与Na2CO3的物质的量之比为______________ ;
(2)所用盐酸的物质的量浓度为______________ ;
(3)生成CO2在标准状况下的体积为______________ 。
(1)此混合物中NaHCO3与Na2CO3的物质的量之比为
(2)所用盐酸的物质的量浓度为
(3)生成CO2在标准状况下的体积为
您最近一年使用:0次
2024-01-10更新
|
115次组卷
|
2卷引用:江苏省常州市溧阳中学2023-2024学年高一上学期阶段性调研测试化学试题
名校
6 . 研究钠及其化合物的性质有重要的意义。
(1)金属钠非常活泼,通常保存在___________ 中,以隔绝空气。
(2)汽车安全气囊内装有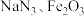 和
和 等物质。
等物质。
①当汽车发生严重碰撞时,引发 分解:
分解: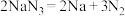 ,
, 中存在的化学键为
中存在的化学键为___________ ;若安全气囊内有 ,其完全分解所释放的
,其完全分解所释放的 在标准状况下的体积为
在标准状况下的体积为___________ L。
②产生的Na立即与 发生置换反应生成
发生置换反应生成 ,其中还原产物是
,其中还原产物是___________ 。
(3)某同学向 和
和 的混合液中逐滴加入一定浓度的盐酸,生成CO2的体积(标准状况)与加入盐酸的体积的关系如图所示。
的混合液中逐滴加入一定浓度的盐酸,生成CO2的体积(标准状况)与加入盐酸的体积的关系如图所示。
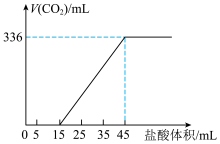
①混合液中
___________ 。
②盐酸的物质的量浓度为___________ 。
(1)金属钠非常活泼,通常保存在
(2)汽车安全气囊内装有
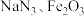 和
和 等物质。
等物质。①当汽车发生严重碰撞时,引发
 分解:
分解: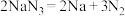 ,
, 中存在的化学键为
中存在的化学键为 ,其完全分解所释放的
,其完全分解所释放的 在标准状况下的体积为
在标准状况下的体积为②产生的Na立即与
 发生置换反应生成
发生置换反应生成 ,其中还原产物是
,其中还原产物是(3)某同学向
 和
和 的混合液中逐滴加入一定浓度的盐酸,生成CO2的体积(标准状况)与加入盐酸的体积的关系如图所示。
的混合液中逐滴加入一定浓度的盐酸,生成CO2的体积(标准状况)与加入盐酸的体积的关系如图所示。
①混合液中

②盐酸的物质的量浓度为
您最近一年使用:0次
名校
解题方法
7 . 某兴趣小组的同学模拟侯德榜制碱法制取纯碱,流程如图:

(1)向饱和NaCl溶液中通入 和氨气时,应先通入
和氨气时,应先通入___________ (填化学式)。操作①的名称为___________ 。
(2)写出反应①的化学方程式:___________ 。
(3)该流程中可循环利用的物质是___________ (填化学式)。
(4)现将 和
和 的固体均匀混合分成两等份。第一份充分加热至恒重,固体质量减少6.2g;第二份与足量稀盐酸充分反应后,加热、蒸干,得到固体23.4g。则混合物中
的固体均匀混合分成两等份。第一份充分加热至恒重,固体质量减少6.2g;第二份与足量稀盐酸充分反应后,加热、蒸干,得到固体23.4g。则混合物中 和
和 的物质的量之比为
的物质的量之比为___________ 。
(5)下列选项中哪种方法可以鉴别 溶液和
溶液和 溶液___________。
溶液___________。
(6)下列实验方案中,不能测定出 和
和 的混合物中
的混合物中 质量分数的是_______。
质量分数的是_______。
(7)钠是一种典型的碱金属元素,下列性质的递变规律正确,且能作为碱金属元素金属性递变规律判断依据的是___________(填字母)。

(1)向饱和NaCl溶液中通入
 和氨气时,应先通入
和氨气时,应先通入(2)写出反应①的化学方程式:
(3)该流程中可循环利用的物质是
(4)现将
 和
和 的固体均匀混合分成两等份。第一份充分加热至恒重,固体质量减少6.2g;第二份与足量稀盐酸充分反应后,加热、蒸干,得到固体23.4g。则混合物中
的固体均匀混合分成两等份。第一份充分加热至恒重,固体质量减少6.2g;第二份与足量稀盐酸充分反应后,加热、蒸干,得到固体23.4g。则混合物中 和
和 的物质的量之比为
的物质的量之比为(5)下列选项中哪种方法可以鉴别
 溶液和
溶液和 溶液___________。
溶液___________。| A.加入澄清石灰水 | B.加入氢氧化钠溶液 |
| C.加热 | D.逐滴加入稀盐酸 |
(6)下列实验方案中,不能测定出
 和
和 的混合物中
的混合物中 质量分数的是_______。
质量分数的是_______。| A.取ag混合物充分加热,质量减少bg |
| B.取ag混合物与足量稀盐酸充分反应,加热、蒸干、灼烧,得到bg固体 |
| C.取ag混合物与足量NaOH溶液充分反应,得到bg溶液 |
| D.取ag混合物与足量稀硫酸充分反应,逸出气体经干燥后用碱石灰吸收,质量增加bg |
(7)钠是一种典型的碱金属元素,下列性质的递变规律正确,且能作为碱金属元素金属性递变规律判断依据的是___________(填字母)。
| A.Li、Na、K的原子半径和密度都随原子序数的增加而增大 |
B.碱性: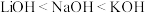 |
C.还原性: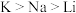 ,故K可以从NaCl溶液中置换出金属钠 ,故K可以从NaCl溶液中置换出金属钠 |
D.熔、沸点: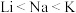 |
您最近一年使用:0次
2023-12-23更新
|
142次组卷
|
3卷引用:湖南省长沙市南雅中学2023-2024学年高一上学期第三次12月月考化学试卷
名校
解题方法
8 . 计算填空:
(1)40.5g某金属氯化物MCl2中含有Cl- 0.6mol,则M的相对原子质量为_______ 。
(2)已知16gA和20gB恰好完全反应生成0.04mol C和31.76g D,则C的摩尔质量为_______ 。
(3)现有标准状况下CO和CO2混合气体8.96L,其质量为16g,则此混合气体中,CO与CO2气体的体积比为_______ 。
(4)加热13.7g碳酸钠和碳酸氢钠的固体混合物,使碳酸氢钠完全分解,混合物质量减少3.1g,则原混合物中碳酸钠的质量为_______ g。(已知:2NaHCO3 Na2CO3+H2O+CO2)
Na2CO3+H2O+CO2)
(5)某NaOH溶液中H2O和Na+的物质的量之比为20:1,测得该溶液的密度为1.1g /mL。 溶液中c(Na+)=______ mol/L。
(1)40.5g某金属氯化物MCl2中含有Cl- 0.6mol,则M的相对原子质量为
(2)已知16gA和20gB恰好完全反应生成0.04mol C和31.76g D,则C的摩尔质量为
(3)现有标准状况下CO和CO2混合气体8.96L,其质量为16g,则此混合气体中,CO与CO2气体的体积比为
(4)加热13.7g碳酸钠和碳酸氢钠的固体混合物,使碳酸氢钠完全分解,混合物质量减少3.1g,则原混合物中碳酸钠的质量为
 Na2CO3+H2O+CO2)
Na2CO3+H2O+CO2)(5)某NaOH溶液中H2O和Na+的物质的量之比为20:1,测得该溶液的密度为1.1g /mL。 溶液中c(Na+)=
您最近一年使用:0次
名校
解题方法
9 . 向某NaOH溶液分别通入不同量的CO2气体,得到A、B、C三种溶液。分别向这三种溶液中滴入1mol·L-1的盐酸,得到的气体变化如图。则:

(1)A溶液中的溶质为___________ 。
(2)C溶液中有两种溶质,除去其中碱性强的溶质的方法为:___________ 。

(1)A溶液中的溶质为
(2)C溶液中有两种溶质,除去其中碱性强的溶质的方法为:
您最近一年使用:0次
名校
10 . 某干燥白色固体可能含有 ,
, 、
、 中的几种,取一定质量的该固体加蒸馏水配制
中的几种,取一定质量的该固体加蒸馏水配制 溶液,并向该溶液中滴加
溶液,并向该溶液中滴加 的盐酸,得到
的盐酸,得到 体积(换算成标准状况下)与盐酸体积的关系如图所示。请回答下列问题:
体积(换算成标准状况下)与盐酸体积的关系如图所示。请回答下列问题:
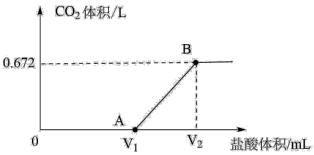
(1)产生的 的物质的量为
的物质的量为_______  ,AB段发生反应的化学方程式为
,AB段发生反应的化学方程式为_______ 。
(2)若白色固体由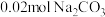 和
和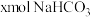 组成,则x=
组成,则x=_______ ,
_______ 。
(3)若白色固体由 和
和 组成,
组成,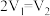 ,则
,则 与
与 溶于水后发生反应的离子方程式为
溶于水后发生反应的离子方程式为_______ ,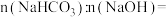
_______ 。
(4)若白色固体只由 和
和 组成,且
组成,且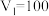 ,
,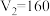 ,则
,则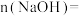
_______  。
。
 ,
, 、
、 中的几种,取一定质量的该固体加蒸馏水配制
中的几种,取一定质量的该固体加蒸馏水配制 溶液,并向该溶液中滴加
溶液,并向该溶液中滴加 的盐酸,得到
的盐酸,得到 体积(换算成标准状况下)与盐酸体积的关系如图所示。请回答下列问题:
体积(换算成标准状况下)与盐酸体积的关系如图所示。请回答下列问题:
(1)产生的
 的物质的量为
的物质的量为 ,AB段发生反应的化学方程式为
,AB段发生反应的化学方程式为(2)若白色固体由
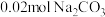 和
和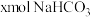 组成,则x=
组成,则x=
(3)若白色固体由
 和
和 组成,
组成,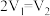 ,则
,则 与
与 溶于水后发生反应的离子方程式为
溶于水后发生反应的离子方程式为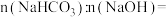
(4)若白色固体只由
 和
和 组成,且
组成,且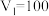 ,
,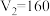 ,则
,则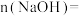
 。
。
您最近一年使用:0次
2023-02-18更新
|
441次组卷
|
3卷引用:江西省上饶市万年县第一中学2023-2024学年高一上学期第二次月考化学试题