1 . 实验题
(1)通过如图完成氢氧化铁胶体制备及性质实验。

【实验步骤】
ⅰ.向沸水中加入几滴饱和FeCl3溶液,继续煮沸至液体呈红褐色停止。ⅱ.把分别盛有CuSO4溶液和Fe(OH)3胶体的烧杯置于暗处,用红色激光
笔照射两杯中的液体,观察现象。
【回答问题】
①Fe(OH)3胶体制备的化学方程式为:___________ 。
②步骤ⅱ中能观察到的现象为___________ ,产生该现象的原因是___________ 。
③若将实验改为向氯化铁溶液中加入氢氧化钠溶液,则会产生红褐色沉淀Fe(OH)3,该反应的离子方程式为___________ 。
(2)有同学利用下面的装置鉴别碳酸钠和碳酸氢钠的稳定性。点燃酒精灯,加热盛有固体药品的部位。请结合实验现象,完成下面的填空。

2个长柄V形玻璃管左右并列固定
①[实验现象]加热开始后,很快可以看到,盛有碳酸氢钠的长柄V形玻璃管内的澄清石灰水___________ ,且固体附近的玻璃管内壁上附有大量的___________ ;盛有碳酸钠的长柄V形玻璃管内的澄清石灰水___________ 。
②[实验结论]该实验现象充分说明,碳酸氢钠受热易分解,并且分解的产物有___________ 。碳酸钠受热不分解。
(3)人体的胃液中存在一定量的胃酸,其主要成分是盐酸。当胃酸过量时,常有胃疼烧心感觉,易吐酸水,若服用适量胃舒平【其主要成分是Al(OH)3,Al(OH)3难溶于水】,能治疗胃酸过多,其反应的离子方程式是___________ 。
(1)通过如图完成氢氧化铁胶体制备及性质实验。

【实验步骤】
ⅰ.向沸水中加入几滴饱和FeCl3溶液,继续煮沸至液体呈红褐色停止。ⅱ.把分别盛有CuSO4溶液和Fe(OH)3胶体的烧杯置于暗处,用红色激光
笔照射两杯中的液体,观察现象。
【回答问题】
①Fe(OH)3胶体制备的化学方程式为:
②步骤ⅱ中能观察到的现象为
③若将实验改为向氯化铁溶液中加入氢氧化钠溶液,则会产生红褐色沉淀Fe(OH)3,该反应的离子方程式为
(2)有同学利用下面的装置鉴别碳酸钠和碳酸氢钠的稳定性。点燃酒精灯,加热盛有固体药品的部位。请结合实验现象,完成下面的填空。

2个长柄V形玻璃管左右并列固定
①[实验现象]加热开始后,很快可以看到,盛有碳酸氢钠的长柄V形玻璃管内的澄清石灰水
②[实验结论]该实验现象充分说明,碳酸氢钠受热易分解,并且分解的产物有
(3)人体的胃液中存在一定量的胃酸,其主要成分是盐酸。当胃酸过量时,常有胃疼烧心感觉,易吐酸水,若服用适量胃舒平【其主要成分是Al(OH)3,Al(OH)3难溶于水】,能治疗胃酸过多,其反应的离子方程式是
您最近一年使用:0次
2 . 碳酸氢铵可用作膨松剂,通过控制碳酸氢铵的用量,不仅使残留在食品中的氨气含量符合食品安全标准,还能使食品具有独特的味道。某同学设计实验测定膨松剂中碳酸氢铵的含量。已知:膨松剂中有少量的水分且其他成分受热不分解。下列说法不正确的是


| A.该实验通过称量装置C的质量可测定碳酸氢铵的含量 |
| B.装置D的作用是吸收空气中的水分和二氧化碳 |
| C.充分反应后停止加热,应继续从m端通入氮气一段时间 |
| D.图中装置B、C对调,不能达到实验目的 |
您最近一年使用:0次
名校
解题方法
3 . 测定放置已久的小苏打样品中纯碱的质量分数,设计如下实验方案:
(1)方案一:称取一定质量的样品,置于坩埚中加热至恒重后,冷却,再称取剩余固体质量。加热时发生的反应的化学方程式为_______ 。若样品的质量为m1g,剩余固体质量为m2g,样品中纯碱的质量分数为_______ (填“A”、“B” 、“C”或“D”)。
A.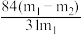 B.
B.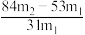 C.
C.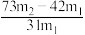 D.
D.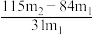
(2)方案二:按下图装置进行实验,通过测定反应所产生气体的质量来达到实验目的,分液漏斗中所装液体为稀硫酸,碱石灰是CaO和NaOH的固体混合物,请回答下列问题。
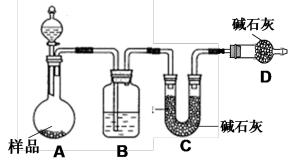
① 实验前先_______ ;
② 洗气瓶B中所装的试剂为_______ ,其作用是_______ ;
③ 实验中除称量样品质量外,还需称_______ 装置前后质量的变化。(填“A”、“B” 、“C”或“D”)。
(3)方案三:称取一定量样品20.0g,置于小烧杯中,加适量水溶解,向小烧杯中加入足量氯化钡溶液。过滤、洗涤、干燥沉淀,称量固体质量为19.7g。通过计算可得到样品中纯碱的质量分数为_______ 。
(1)方案一:称取一定质量的样品,置于坩埚中加热至恒重后,冷却,再称取剩余固体质量。加热时发生的反应的化学方程式为
A.
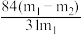 B.
B.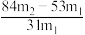 C.
C.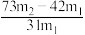 D.
D.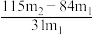
(2)方案二:按下图装置进行实验,通过测定反应所产生气体的质量来达到实验目的,分液漏斗中所装液体为稀硫酸,碱石灰是CaO和NaOH的固体混合物,请回答下列问题。

① 实验前先
② 洗气瓶B中所装的试剂为
③ 实验中除称量样品质量外,还需称
(3)方案三:称取一定量样品20.0g,置于小烧杯中,加适量水溶解,向小烧杯中加入足量氯化钡溶液。过滤、洗涤、干燥沉淀,称量固体质量为19.7g。通过计算可得到样品中纯碱的质量分数为
您最近一年使用:0次
解题方法
4 . 某探究小组设计了如图装置,进行关于 和
和 的性质实验(加热及夹持装置省略),将分别装有
的性质实验(加热及夹持装置省略),将分别装有 和
和 的试管同时放入甘油浴加热(甘油沸点为
的试管同时放入甘油浴加热(甘油沸点为 ),下列叙述不正确的是
),下列叙述不正确的是
 和
和 的性质实验(加热及夹持装置省略),将分别装有
的性质实验(加热及夹持装置省略),将分别装有 和
和 的试管同时放入甘油浴加热(甘油沸点为
的试管同时放入甘油浴加热(甘油沸点为 ),下列叙述不正确的是
),下列叙述不正确的是
A.该实验可用于比较 和 和 的稳定性 的稳定性 |
| B.a试管中的实验现象为:有气泡,但是没有沉淀产生 |
| C.b试管中的实验现象为:有气泡,但是没有沉淀产生 |
D. 可用于焙制糕点, 可用于焙制糕点, 可用于玻璃、造纸等工业 可用于玻璃、造纸等工业 |
您最近一年使用:0次
2024-01-26更新
|
87次组卷
|
2卷引用:湖南省岳阳市2023-2024学年高一上学期期末考试化学试题
5 . 某兴趣小组在实验室模拟侯氏制碱法制取纯碱,流程如图1:

(1)装置I中反应的化学方程式为_____ 。
(2)装置Ⅱ中反应的化学方程式为_____ 。
(3)向母液中加入磨细的食盐粉末,有 固体析出,为使
固体析出,为使 充分析出并分离,根据
充分析出并分离,根据 和
和 溶解度曲线(图2),需采用的操作为
溶解度曲线(图2),需采用的操作为_____ 、_____ 、过滤、洗涤、干燥。

(4)该流程中可循环利用的物质是_____ 。(填化学式)
(5)用该法制备的纯碱配制的溶液中含有 ,设计能证明该溶液中存在
,设计能证明该溶液中存在 的实验操作及现象
的实验操作及现象_____ 。

(1)装置I中反应的化学方程式为
(2)装置Ⅱ中反应的化学方程式为
(3)向母液中加入磨细的食盐粉末,有
 固体析出,为使
固体析出,为使 充分析出并分离,根据
充分析出并分离,根据 和
和 溶解度曲线(图2),需采用的操作为
溶解度曲线(图2),需采用的操作为
(4)该流程中可循环利用的物质是
(5)用该法制备的纯碱配制的溶液中含有
 ,设计能证明该溶液中存在
,设计能证明该溶液中存在 的实验操作及现象
的实验操作及现象
您最近一年使用:0次
解题方法
6 . 某小组探究Na2CO3和NaHCO3的性质。
(1)探究溶解性。在两支试管中,分别加入约1g Na2CO3和NaHCO3固体,分别加入5mL水,充分振荡后,一支试管中固体有剩余,剩余的固体是______ 。
(2)探究稳定性。按照如图所示装置进行实验(部分夹持装置已略去)。
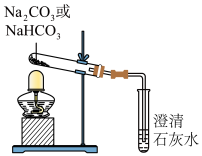
①能够证明Na2CO3的热稳定性强于NaHCO3的证据是______ 。
②NaHCO3受热分解的化学方程式是______ 。
(3)探究与酸的反应。
(4)该小组在探究Na2CO3和NaHCO3的性质时,运用的化学思想方法有______ (填序号)。
a.比较 b.定性与定量相结合
(1)探究溶解性。在两支试管中,分别加入约1g Na2CO3和NaHCO3固体,分别加入5mL水,充分振荡后,一支试管中固体有剩余,剩余的固体是
(2)探究稳定性。按照如图所示装置进行实验(部分夹持装置已略去)。

①能够证明Na2CO3的热稳定性强于NaHCO3的证据是
②NaHCO3受热分解的化学方程式是
(3)探究与酸的反应。
实验步骤 | 实现现象 | 用离子方程式解释现象 |
向盛有Na2CO3溶液的试管中滴加稀盐酸 | 开始无气泡产生,一段时间后产生气泡 | ① ② |
向盛有NaHCO3溶液的试管中滴加稀盐酸 | 立即产生气泡 |
(4)该小组在探究Na2CO3和NaHCO3的性质时,运用的化学思想方法有
a.比较 b.定性与定量相结合
您最近一年使用:0次
7 . 某小组设计实验探究钠和二氧化碳反应产物,装置如图所示(已知金属钠与二氧化碳常温下不反应)。
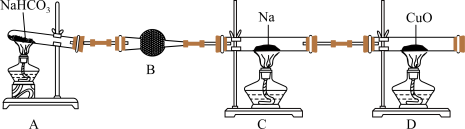
回答下列问题:
(1)B中试剂可能是_______ (填字母)。
a.碱石灰 b.氯化钙 c.五氧化二磷 d.
(2)加热装有 试管的操作是
试管的操作是_______ 。
(3)写出A中反应的化学方程式:_______ 。
(4)能证明C中产生 的实验现象是
的实验现象是_______ 。
(5)当C中钠完全反应后,停止A中反应。为了探究C中残留固体成分进行如下实验:
①实验Ⅰ中黑色粉末是_______ (填化学式)。
②仅通过实验Ⅱ_______ (填“能”或“不能”)证明固体中一定含有 ,简述理由:
,简述理由:_______ 。
③经检验 和
和 反应生成两种还原产物的物质的量之比为1∶1,且只有一种氧化产物,写出化学方程式:
反应生成两种还原产物的物质的量之比为1∶1,且只有一种氧化产物,写出化学方程式:_______ 。
(6)该装置存在的明显缺陷是_______ 。

回答下列问题:
(1)B中试剂可能是
a.碱石灰 b.氯化钙 c.五氧化二磷 d.

(2)加热装有
 试管的操作是
试管的操作是(3)写出A中反应的化学方程式:
(4)能证明C中产生
 的实验现象是
的实验现象是(5)当C中钠完全反应后,停止A中反应。为了探究C中残留固体成分进行如下实验:
| 序号 | 操作 | 现象 |
| Ⅰ | 取少量固体溶于水,静置 | 液体表面有黑色粉末 |
| Ⅱ | 过滤Ⅰ中混合物得到无色液体和黑色固体,将液体分甲、乙两份,向甲中滴加酚酞溶液 | 甲中溶液变红色 |
| Ⅲ | 向中乙溶液中滴加 溶液 溶液 | 产生白色沉淀 |
| Ⅳ | 另取C中残留固体,滴加盐酸 | 产生气体 |
②仅通过实验Ⅱ
 ,简述理由:
,简述理由:③经检验
 和
和 反应生成两种还原产物的物质的量之比为1∶1,且只有一种氧化产物,写出化学方程式:
反应生成两种还原产物的物质的量之比为1∶1,且只有一种氧化产物,写出化学方程式:(6)该装置存在的明显缺陷是
您最近一年使用:0次
名校
8 . 兴趣小组获得两包制作“跳跳糖”的添加剂,一包是柠檬酸晶体,另一包是标注为钠盐的白色粉末。将少量柠檬酸和这种白色粉末溶于水,混合后产生了使澄清石灰水变浑浊的气体。于是对白色粉末的化学成分进行了以下探究:

[提出猜想]
猜想1.碳酸钠;
猜想2.碳酸氢钠;
猜想3.碳酸钠和碳酸氢钠。
[查阅资料]碳酸钠溶液、碳酸氢钠溶液均呈碱性。
(1)[实验探究]小明、小磊分别对有关猜想设计方案并进行实验:
(2)[交流反思]大家一致认为小明和小磊的结论不准确:
①小明实验结论不准确的原因是_______ 。
②小磊的实验方案不能排除白色粉末是否含有________ 。
[结论分析]探究后他们得出添加剂的成分是柠檬酸和碳酸氢钠,分析后认为白色粉末中的碳酸钠是由碳酸氢钠分解产生的。
(3)[拓展应用]下列物质常温下放置一段时间也会分解的是________(填字母)。

[提出猜想]
猜想1.碳酸钠;
猜想2.碳酸氢钠;
猜想3.碳酸钠和碳酸氢钠。
[查阅资料]碳酸钠溶液、碳酸氢钠溶液均呈碱性。
(1)[实验探究]小明、小磊分别对有关猜想设计方案并进行实验:
| 实验操作 | 实验现象 | 实验结论 | |
| 小明 | 将白色粉末溶于水后用pH试纸测定其酸碱度 | pH | 溶液呈碱性,猜想1成立 |
| 小磊 | 用如图所示的装置进行实验 | 试管A中有水珠产生,试管B中液体变浑浊 | 猜想2成立,试管A中反应的化学方程式为 |
(2)[交流反思]大家一致认为小明和小磊的结论不准确:
①小明实验结论不准确的原因是
②小磊的实验方案不能排除白色粉末是否含有
[结论分析]探究后他们得出添加剂的成分是柠檬酸和碳酸氢钠,分析后认为白色粉末中的碳酸钠是由碳酸氢钠分解产生的。
(3)[拓展应用]下列物质常温下放置一段时间也会分解的是________(填字母)。
| A.浓硫酸 | B.氢氧化钠 | C.碳酸氢铵 | D.氯化钠 |
您最近一年使用:0次
9 . 根据实验现象书写方程式:
Ⅰ.某同学进行如下实验:
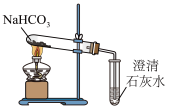
(1)加热NaHCO3的化学方程式:___________ 。
(2)一段时间后可以观察到澄清石灰水变浑浊,原因是___________ (用化学方程式表示,下同),再过一段时间后变澄清,发生的反应是___________ 。
Ⅱ.另一位同学进行如下实验:

(3)开始时,溶液的红色没有明显变化,也没有明显的气泡产生,反应的离子方程式为:___________ 。
(4)继续滴加盐酸,溶液的浅红色褪去,有大量气泡出现,反应的离子方程式为:___________ 。
Ⅲ.书写方程式:
(5)实验室检验Al3+的离子方程式:___________ 、___________ 。
(6)实验室制备Al(OH)3的离子方程式:___________ 、___________ (写出两种方法)
(7)除去Fe2O3中的Al2O3,可以选用的试剂是:___________ ,反应的离子方程式是___________ 。
(8)打磨过的铝条与NaOH反应的离子方程式:___________ 。
Ⅰ.某同学进行如下实验:

(1)加热NaHCO3的化学方程式:
(2)一段时间后可以观察到澄清石灰水变浑浊,原因是
Ⅱ.另一位同学进行如下实验:

(3)开始时,溶液的红色没有明显变化,也没有明显的气泡产生,反应的离子方程式为:
(4)继续滴加盐酸,溶液的浅红色褪去,有大量气泡出现,反应的离子方程式为:
Ⅲ.书写方程式:
(5)实验室检验Al3+的离子方程式:
(6)实验室制备Al(OH)3的离子方程式:
(7)除去Fe2O3中的Al2O3,可以选用的试剂是:
(8)打磨过的铝条与NaOH反应的离子方程式:
您最近一年使用:0次
解题方法
10 . 某研究小组用为探究碳酸钠与碳酸氢钠的性质,进行如下实验。
已知:碳酸钠固体久置空气中会吸收水,生成Na2CO3·7H2O和Na2CO3·10H2O等。
【任务一】初识碳酸钠与碳酸氢钠
(1)实验①得出结论:室温下,Na2CO3的溶解度______ NaHCO3(填“>”或“<”)。
(2)实验②无法得出相同条件下两种溶液碱性强弱的结论,理由是_____ 。
(3)实验③中碳酸钠溶液无明显现象,原因是______ (用离子方程式表示)。
【任务二】再探碳酸钠与碳酸氢钠
(4)实验④中,Na2CO3的溶解属于______ 过程(填“吸热”或“放热”)。
(5)实验⑤中,滴加NaHCO3溶液,pH下降幅度较大的理由是______ 。
【任务三】探究碳酸钠与碳酸氢钠的热稳定性

观察到的实验现象如表所示:
根据上述实验现象,回答下列问题:
(6)实验⑥,无水硫酸铜变蓝的原因是______ 。
(7)上述实验开始时均断断续续产生气泡的原因是______ 。
(8)实验结论为热稳定性:Na2CO3______ NaHCO3(填“>”“<”或“=”)。
已知:碳酸钠固体久置空气中会吸收水,生成Na2CO3·7H2O和Na2CO3·10H2O等。
【任务一】初识碳酸钠与碳酸氢钠
| 步骤 | 实验操作 | 实验现象 | |
| Na2CO3 | NaHCO3 | ||
| ① |  | 一段时间后,恢复到室温,全部溶解,得到透明溶液 | 一段时间后,恢复到室温,部分溶解,试管底部有固体残余 |
| ② | 取①的溶液,分别滴加2漓酚酞溶液 | 溶液变红色 | 溶液变浅红色 |
| ③ | 另取①的溶液,分别滴加2滴稀盐酸 | 无明显现象 | 产生少量气泡 |
(2)实验②无法得出相同条件下两种溶液碱性强弱的结论,理由是
(3)实验③中碳酸钠溶液无明显现象,原因是
【任务二】再探碳酸钠与碳酸氢钠
| 步骤 | 实验操作 | 实验数据(传感器测得) |
| ④ | 目的:探究溶解过程温度变化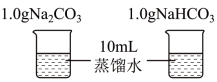 |  |
| ⑤ | 目的:测量实验过程中pH的变化 |  |
(5)实验⑤中,滴加NaHCO3溶液,pH下降幅度较大的理由是
【任务三】探究碳酸钠与碳酸氢钠的热稳定性

观察到的实验现象如表所示:
| 编号 | 药品 | 装置B | 装置C |
| ⑥ | 久置碳酸钠 | 白色变蓝色 | 开始断断续续产生气泡,一段时间后,没有气泡,溶液保持澄清 |
| ⑦ | 碳酸氢钠 | 白色变蓝色 | 开始断断续续产生气泡,一段时间后,产生连续气泡,溶液变浑浊 |
(6)实验⑥,无水硫酸铜变蓝的原因是
(7)上述实验开始时均断断续续产生气泡的原因是
(8)实验结论为热稳定性:Na2CO3
您最近一年使用:0次



