1 . 下列物质的用途与性质具有对应关系的是
| 选项 | 物质 | 用途 | 性质 |
| A | 活性炭 | 冰箱除异味、泳池水处理 | 还原性 |
| B | FeCl3 | 腐蚀印刷线路板 | 其溶液显酸性 |
| C | NaHCO3 | 作烘焙糕点的膨松剂 | 其溶液显碱性 |
| D | 浓氨水 | 检查氯气管道是否漏气 | 碱性和还原性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
2 . 利用“价类二维图”研究物质的性质是化学研究的重要手段。下图是氯元素的化合价与部分物质类别的对应关系。

回答下列问题:
(1)已知D可用于实验室制 ,焰色试验时其火焰呈现紫色。A、B、C、D四种物质中,属于电解质的是
,焰色试验时其火焰呈现紫色。A、B、C、D四种物质中,属于电解质的是_______ (填化学式)。
(2)将E滴入碳酸氢钠溶液中,有大量气泡产生,该反应的离子方程式为_______ 。
(3)取 某84消毒液(有效成分
某84消毒液(有效成分 含量为
含量为 ),加水稀释,配制成
),加水稀释,配制成 稀溶液。
稀溶液。
①配制过程中使用的玻璃仪器有烧杯、玻璃棒、胶头滴管、量筒、_______ 。
②关于配制过程的下列说法中,正确的是_______ (填字母)。
A.容量瓶用蒸馏水洗净后,应烘干后才能用于溶液配制
B.未用蒸馏水洗涤烧杯和玻璃棒可能导致结果偏低
C.定容时,俯视观察刻度线可能导致结果偏低
D.定容摇匀后,将溶液保存于容量瓶中,随用随取
③稀释后的溶液中, 的物质的量浓度为
的物质的量浓度为_______  。
。
(4)工业上“侯氏制碱法”以 、
、 、
、 及水等为原料制备纯碱,生产纯碱的工艺流程示意图如下:
及水等为原料制备纯碱,生产纯碱的工艺流程示意图如下:

①实验室分离出沉淀的操作名称是_______ ;煅烧炉里进行的化学反应方程式为:_______ 。
②检验产品 中是否含有氯离子,需要的试剂有
中是否含有氯离子,需要的试剂有_______ 。

回答下列问题:
(1)已知D可用于实验室制
 ,焰色试验时其火焰呈现紫色。A、B、C、D四种物质中,属于电解质的是
,焰色试验时其火焰呈现紫色。A、B、C、D四种物质中,属于电解质的是(2)将E滴入碳酸氢钠溶液中,有大量气泡产生,该反应的离子方程式为
(3)取
 某84消毒液(有效成分
某84消毒液(有效成分 含量为
含量为 ),加水稀释,配制成
),加水稀释,配制成 稀溶液。
稀溶液。①配制过程中使用的玻璃仪器有烧杯、玻璃棒、胶头滴管、量筒、
②关于配制过程的下列说法中,正确的是
A.容量瓶用蒸馏水洗净后,应烘干后才能用于溶液配制
B.未用蒸馏水洗涤烧杯和玻璃棒可能导致结果偏低
C.定容时,俯视观察刻度线可能导致结果偏低
D.定容摇匀后,将溶液保存于容量瓶中,随用随取
③稀释后的溶液中,
 的物质的量浓度为
的物质的量浓度为 。
。(4)工业上“侯氏制碱法”以
 、
、 、
、 及水等为原料制备纯碱,生产纯碱的工艺流程示意图如下:
及水等为原料制备纯碱,生产纯碱的工艺流程示意图如下:
①实验室分离出沉淀的操作名称是
②检验产品
 中是否含有氯离子,需要的试剂有
中是否含有氯离子,需要的试剂有
您最近一年使用:0次
2023-01-01更新
|
567次组卷
|
3卷引用:辽宁省大连市2022-2023学年高一上学期期末考试化学试题
名校
3 . 回答下列问题:
(1)关于甲、乙、丙、丁四套装置的说法正确的是_______ 。

(2)以下物质(或粒子)与其用途之间关联正确的是_______ 。
(3)实验室制取Cl2的化学方程式:_______ 。浓盐酸表现的性质是_______ 。
(4)已知:在稀硫酸中,MnO 与H2O2也能发生以下反应:2KMnO4+3H2O2+3H2SO4=K2SO4+2MnSO4+5O2↑+8H2O。由上述反应得出物质氧化性强弱的结论是_______>_______(填化学式)。
与H2O2也能发生以下反应:2KMnO4+3H2O2+3H2SO4=K2SO4+2MnSO4+5O2↑+8H2O。由上述反应得出物质氧化性强弱的结论是_______>_______(填化学式)。_______
(1)关于甲、乙、丙、丁四套装置的说法正确的是

| A.用装置甲制取氯气 | B.用丙装置可以较长时间看到白色Fe(OH)2白色沉淀 |
| C.用丁装置证明碳酸氢钠受热易分解 | D.用装置乙除去氢气中的少量氯化氢 |
| A.硬铝——制导线 | B.14C——测定文物年代 |
| C.锗——作半导体材料 | D.Ti-Fe合金——作不锈钢材料 |
(4)已知:在稀硫酸中,MnO
 与H2O2也能发生以下反应:2KMnO4+3H2O2+3H2SO4=K2SO4+2MnSO4+5O2↑+8H2O。由上述反应得出物质氧化性强弱的结论是_______>_______(填化学式)。
与H2O2也能发生以下反应:2KMnO4+3H2O2+3H2SO4=K2SO4+2MnSO4+5O2↑+8H2O。由上述反应得出物质氧化性强弱的结论是_______>_______(填化学式)。
您最近一年使用:0次
2023-09-24更新
|
324次组卷
|
4卷引用:天津市宁河区芦台第一中学2022-2023学年高一上学期期末考试化学试题
天津市宁河区芦台第一中学2022-2023学年高一上学期期末考试化学试题(已下线)专题07 铁及其化合物 金属材料-【好题汇编】备战2023-2024学年高一化学上学期期末真题分类汇编(天津专用)(已下线)专项02 氧化还原反应的概念、规律及综合应用-【好题汇编】备战2023-2024学年高一化学上学期期末真题分类汇编(天津专用)山西运城盐湖五中2023-2024学年高一上学期化学期末练兵卷(三)
4 . 下列物质的性质或用途的因果关系正确的是
| A.小苏打不稳定、受热易分解,因此面包师常用小苏打作发泡剂烘焙面包 |
| B.苯酚又名石炭酸,其水溶液具有弱酸性,因此可用于杀菌消毒 |
| C.氯化铝熔点低,因此工业常采用电解熔融氯化铝制得铝 |
| D.铵盐受热易分解,因此实验室可用加热分解NH4Cl制备NH3 |
您最近一年使用:0次
5 . 碳酸钠和碳酸氢钠是常见的钠盐,用途广泛。碳酸钠样品中混有碳酸氢钠,实验室测定碳酸钠样品中碳酸钠的质量分数,设计下列方案:
Ⅰ.方案一:气体法
实验流程如下:

实验装置如图:

(1)A装置滴入稀盐酸,开始没有气泡产生,写出开始反应的离子方程式_______ 。
(2)B装置盛放浓硫酸,作用是_______ 。如果去掉B装置,实验_______ 成功(填“能”或“不能”)。
(3)D装置的作用是_______ 。
(4)实验前后C装置的质量差是样品与盐酸反应产生的_______ 质量(填化学式)。
Ⅱ.方案二:分解法
实验步骤:用天平准确称量出干燥试管的质量为18.0g,然后称取20.0g已研碎的碳酸钠样品并放入干燥的试管中。用酒精灯加热,待充分反应并冷却后,在天平上称出试管和固体的总质量为34.9g。
(5)写出碳酸氢钠受热分解的化学方程式_______ 。
(6)该样品中碳酸钠的质量分数为_______ 。
Ⅰ.方案一:气体法
实验流程如下:

实验装置如图:

(1)A装置滴入稀盐酸,开始没有气泡产生,写出开始反应的离子方程式
(2)B装置盛放浓硫酸,作用是
(3)D装置的作用是
(4)实验前后C装置的质量差是样品与盐酸反应产生的
Ⅱ.方案二:分解法
实验步骤:用天平准确称量出干燥试管的质量为18.0g,然后称取20.0g已研碎的碳酸钠样品并放入干燥的试管中。用酒精灯加热,待充分反应并冷却后,在天平上称出试管和固体的总质量为34.9g。
(5)写出碳酸氢钠受热分解的化学方程式
(6)该样品中碳酸钠的质量分数为
您最近一年使用:0次
名校
6 . 钠元素在自然界分布很广,储量极为丰富,都以化合态存在。钠及其化合物(如 等)在生产生活中被广泛应用。
等)在生产生活中被广泛应用。
(1)金属钠用途广泛。
①可用于制备 。采用空气和
。采用空气和 为原料可直接制备
为原料可直接制备 。空气与熔融金属
。空气与熔融金属 反应前需依次通过
反应前需依次通过_______ 、_______ (填序号)。
a.浓硫酸 b.饱和食盐水 c. 溶液 d.酸性
溶液 d.酸性 溶液
溶液
②金属钠还可以用于钛、锆、铌、钽等金属的冶炼。如高温条件下, 与
与 反应制备
反应制备 ,反应的化学方程式为
,反应的化学方程式为_______ 。
(2)碳酸钠和碳酸氢钠均可作食用碱。传统蒸馒头常采用酵头发面,再用 调节面团酸度。查阅资料得知,酵头可使面团在微生物作用下产生
调节面团酸度。查阅资料得知,酵头可使面团在微生物作用下产生 气体,从而使面团疏松,但同时也会产生乳酸、醋酸等有机酸。
气体,从而使面团疏松,但同时也会产生乳酸、醋酸等有机酸。
①等质量的碳酸钠和碳酸氢钠与足量醋酸充分反应,消耗醋酸更多的是_______ 。(写名称)
②若面团发得不好,面团内的气孔少,略有酸味。可不用 而用
而用 ,继续揉面,上锅蒸后也能蒸出松软可口的馒头。解释
,继续揉面,上锅蒸后也能蒸出松软可口的馒头。解释 的作用
的作用_______ 。
(3)某实验兴趣小组想探究某食用碱( 或
或 )的成分,依次进行如下实验:
)的成分,依次进行如下实验:
实验1:取适量(约 )食用碱固体于试管中,滴加少量水,振荡,观察到固体溶解,并伴随放热现象。据此推测,该食用碱主要成分为
)食用碱固体于试管中,滴加少量水,振荡,观察到固体溶解,并伴随放热现象。据此推测,该食用碱主要成分为_______ 。(写化学式)
实验2: 长期放置在空气中会变质(部分转变为
长期放置在空气中会变质(部分转变为 ),现欲测定该食用碱中
),现欲测定该食用碱中 的质量分数,设计如下实验装置。
的质量分数,设计如下实验装置。

称取食用碱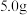 置于A试管中,C中加入一定质量并足量的
置于A试管中,C中加入一定质量并足量的 固体,充分加热,观察到D处的现象为
固体,充分加热,观察到D处的现象为_______ 。实验结束后,测得 固体增重
固体增重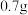 ,则该食用碱中
,则该食用碱中 的质量分数为
的质量分数为_______ 。
 等)在生产生活中被广泛应用。
等)在生产生活中被广泛应用。(1)金属钠用途广泛。
①可用于制备
 。采用空气和
。采用空气和 为原料可直接制备
为原料可直接制备 。空气与熔融金属
。空气与熔融金属 反应前需依次通过
反应前需依次通过a.浓硫酸 b.饱和食盐水 c.
 溶液 d.酸性
溶液 d.酸性 溶液
溶液②金属钠还可以用于钛、锆、铌、钽等金属的冶炼。如高温条件下,
 与
与 反应制备
反应制备 ,反应的化学方程式为
,反应的化学方程式为(2)碳酸钠和碳酸氢钠均可作食用碱。传统蒸馒头常采用酵头发面,再用
 调节面团酸度。查阅资料得知,酵头可使面团在微生物作用下产生
调节面团酸度。查阅资料得知,酵头可使面团在微生物作用下产生 气体,从而使面团疏松,但同时也会产生乳酸、醋酸等有机酸。
气体,从而使面团疏松,但同时也会产生乳酸、醋酸等有机酸。①等质量的碳酸钠和碳酸氢钠与足量醋酸充分反应,消耗醋酸更多的是
②若面团发得不好,面团内的气孔少,略有酸味。可不用
 而用
而用 ,继续揉面,上锅蒸后也能蒸出松软可口的馒头。解释
,继续揉面,上锅蒸后也能蒸出松软可口的馒头。解释 的作用
的作用(3)某实验兴趣小组想探究某食用碱(
 或
或 )的成分,依次进行如下实验:
)的成分,依次进行如下实验:实验1:取适量(约
 )食用碱固体于试管中,滴加少量水,振荡,观察到固体溶解,并伴随放热现象。据此推测,该食用碱主要成分为
)食用碱固体于试管中,滴加少量水,振荡,观察到固体溶解,并伴随放热现象。据此推测,该食用碱主要成分为实验2:
 长期放置在空气中会变质(部分转变为
长期放置在空气中会变质(部分转变为 ),现欲测定该食用碱中
),现欲测定该食用碱中 的质量分数,设计如下实验装置。
的质量分数,设计如下实验装置。
称取食用碱
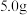 置于A试管中,C中加入一定质量并足量的
置于A试管中,C中加入一定质量并足量的 固体,充分加热,观察到D处的现象为
固体,充分加热,观察到D处的现象为 固体增重
固体增重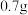 ,则该食用碱中
,则该食用碱中 的质量分数为
的质量分数为
您最近一年使用:0次
2023-11-24更新
|
123次组卷
|
2卷引用:河北省石家庄市第二中学2023-2024学年高一上学期期中考试化学试题
解题方法
7 . 碳酸钠是一种重要的化工原料,具有广泛的用途,其生产流程如图所示:

已知:“反应4”实际包含两步反应,“操作1”为过滤。
下列叙述正确的是

已知:“反应4”实际包含两步反应,“操作1”为过滤。
下列叙述正确的是
| A.在实验室完成“操作1”所需的玻璃仪器仅有漏斗和烧杯 |
| B.流程中涉及的反应只有分解反应和化合反应 |
C.“反应2”的离子反应为 |
| D.上述流程涉及的物质中只有四种属于盐类 |
您最近一年使用:0次
8 . Ⅰ.家庭厨卫用品中有许多常见的化学物质,括号内为其主要成分:
①料酒(乙醇);②食醋(乙酸);③碱面( );④小苏打(
);④小苏打( );⑤84消毒液(
);⑤84消毒液( ):⑥洁厕灵(
):⑥洁厕灵( );⑦铁锅(
);⑦铁锅( )
)
(1)乙醇的化学式为 ,属于
,属于______ (填“纯净物”或“混合物”)。
(2)用铁锅炒菜时,不宜加入过多的食醋,原因是:______ 。
(3)小苏打常用作面食的膨松剂,请用化学方程式说明原理______ 。
(4)家庭中不可将84消毒液与洁厕灵混用,否则会因产生一种有毒气体,请用离子方程式解释原因______ 。
Ⅱ.亚硝酸钠( )是一种用途广泛的工业盐,因其外观和食盐相似容易误食中毒。
)是一种用途广泛的工业盐,因其外观和食盐相似容易误食中毒。
(5)若误食亚硝酸钠会导致血红蛋白中亚铁离子转化为铁离子而中毒,服用维生素 可解除亚硝酸钠的中毒,下列关于上述中毒。解毒过程的说法中,正确的是______。
可解除亚硝酸钠的中毒,下列关于上述中毒。解毒过程的说法中,正确的是______。
(6)已知 能发生如下反应:
能发生如下反应: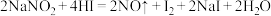 ,该反应的还原产物是
,该反应的还原产物是______ , 体现出的性质有
体现出的性质有______ 。请标出该反应的电子转移方向和数目______ 。
①料酒(乙醇);②食醋(乙酸);③碱面(
 );④小苏打(
);④小苏打( );⑤84消毒液(
);⑤84消毒液( ):⑥洁厕灵(
):⑥洁厕灵( );⑦铁锅(
);⑦铁锅( )
)(1)乙醇的化学式为
 ,属于
,属于(2)用铁锅炒菜时,不宜加入过多的食醋,原因是:
(3)小苏打常用作面食的膨松剂,请用化学方程式说明原理
(4)家庭中不可将84消毒液与洁厕灵混用,否则会因产生一种有毒气体,请用离子方程式解释原因
Ⅱ.亚硝酸钠(
 )是一种用途广泛的工业盐,因其外观和食盐相似容易误食中毒。
)是一种用途广泛的工业盐,因其外观和食盐相似容易误食中毒。(5)若误食亚硝酸钠会导致血红蛋白中亚铁离子转化为铁离子而中毒,服用维生素
 可解除亚硝酸钠的中毒,下列关于上述中毒。解毒过程的说法中,正确的是______。
可解除亚硝酸钠的中毒,下列关于上述中毒。解毒过程的说法中,正确的是______。| A.亚硝酸钠是还原剂 | B.维生素 是氧化剂 是氧化剂 |
C.维生素 能把铁离子还原成为亚铁离子 能把铁离子还原成为亚铁离子 | D.亚硝酸钠被还原 |
 能发生如下反应:
能发生如下反应: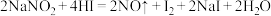 ,该反应的还原产物是
,该反应的还原产物是 体现出的性质有
体现出的性质有
您最近一年使用:0次
解题方法
9 . 我国制碱工业先驱侯德榜发明了侯氏制碱法。其模拟流程如图:
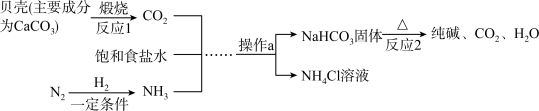
回答下列问题:
(1)饱和食盐水为氯化钠的饱和溶液,写出氯化钠在生活中的一种用途:________ 。
(2)写出N2与H2在一定条件下反应生成NH3的化学方程式:_________ 。
(3)进行操作a时所需的玻璃仪器有玻璃棒、________ 和________ 。
(4)NaHCO3固体受热分解的化学方程式为_______ 。
(5)现有ag质量分数为w的NH4Cl溶液(不考虑 与水发生的反应):
与水发生的反应):
①该溶液中所含溶质的总质量为________ (用含a、w的代数式表示,写出计算式即可)g。
②________ gNH3中所含的氮元素的总质量与该溶液中所含的氮元素的总质量相等。

回答下列问题:
(1)饱和食盐水为氯化钠的饱和溶液,写出氯化钠在生活中的一种用途:
(2)写出N2与H2在一定条件下反应生成NH3的化学方程式:
(3)进行操作a时所需的玻璃仪器有玻璃棒、
(4)NaHCO3固体受热分解的化学方程式为
(5)现有ag质量分数为w的NH4Cl溶液(不考虑
 与水发生的反应):
与水发生的反应):①该溶液中所含溶质的总质量为
②
您最近一年使用:0次
解题方法
10 . A~M为中学化学中常见的物质,其中A可用于焙制糕点。各物质间的转化关系如图所示。

回答下列问题:
(1)A的俗名是_______ 。E的化学式是_______ 。
(2)I转变成K的化学方程式是_______ 。J溶液中滴加 溶液的离子方程式是
溶液的离子方程式是_______ 。
(3)C和E的反应中,还原剂是_______ 。标准状况下,每生成 氧化产物,转移的电子数是
氧化产物,转移的电子数是_______ 。
(4)写出M的一种用途_______ 。
(5)保存H溶液时常加入少量铁粉的原因是_______ 。

回答下列问题:
(1)A的俗名是
(2)I转变成K的化学方程式是
 溶液的离子方程式是
溶液的离子方程式是(3)C和E的反应中,还原剂是
 氧化产物,转移的电子数是
氧化产物,转移的电子数是(4)写出M的一种用途
(5)保存H溶液时常加入少量铁粉的原因是
您最近一年使用:0次



