名校
1 . 下列实验操作正确且能达到实验目的的是
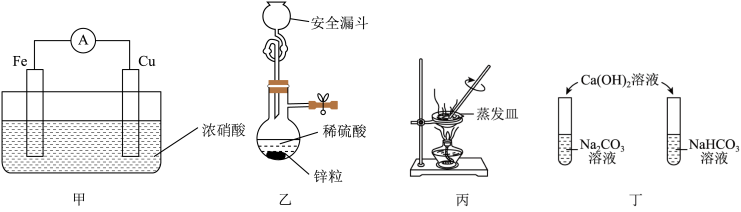
| A.用甲装置判断Fe和Cu金属的活泼性 |
B.用乙装置制取少量 |
C.用丙装置除去NaCl固体中的 |
D.用丁装置鉴别 溶液和 溶液和 溶液 溶液 |
您最近一年使用:0次
解题方法
2 . 常温下,分别向相同浓度的NaHCO3、Na2CO3溶液中逐滴加入盐酸,滴加过程中溶液的pH变化如下图所示。下列说法正确的是
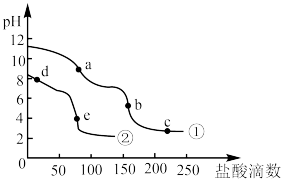
| A.曲线①表示盐酸滴入NaHCO3溶液的过程 |
| B.d、e点水的电离程度:d>e |
| C.a点的KW大于d点的KW |
D.b、c、e点均满足: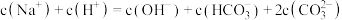 |
您最近一年使用:0次
2024-04-16更新
|
115次组卷
|
2卷引用:重庆市康德2024年普通高中学业水平选择性考试高三下学期高考模拟调研卷(三)化学试题
3 . 下列叙述正确的是
A.浓硝酸见光分解的产物有 |
B. 加入饱和 加入饱和 溶液中可生成 溶液中可生成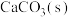 |
C.苏打不稳定,受热分解生成 |
D.铜分别与 和 和 粉在加热条件下反应生成 粉在加热条件下反应生成 和 和 |
您最近一年使用:0次
4 . 利用下列有关实验装置进行相应实验,能达到实验目的的是
 | 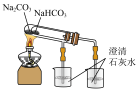 |  |  |
| A.制备Fe2S3固体 | B.比较Na2CO3、NaHCO3的热稳定性 | C.证明乙炔能使溴水褪色 | D.探究浓度对化学反应速率的影响 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
5 . 利用下列装置完成对应的实验,能达到实验目的的是
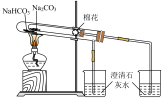 |  |  | 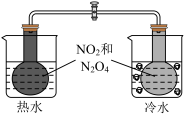 |
| A.比较碳酸钠与碳酸氢钠的热稳定性 | B.检查装置的气密性 | C.制备氢氧化铁胶体 | D.判断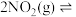  的热效应 的热效应 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
6 . 下列选用的仪器和药品能达到实验目的的是


| A.装置①:定量测定化学反应速率 | B.装置②:吸收尾气Cl2 |
| C.装置③:加热氢氧化钠固体 | D.装置④:比较NaHCO3和Na2CO3的热稳定性 |
您最近一年使用:0次
解题方法
7 . 下列说法不正确的是
| A.物质的用途:碳酸钠可用于造纸;碳酸氢钠可以制作胃药 |
| B.离子的性质:金属阳离子只有氧化性,非金属阴离子只有还原性 |
C.物质的鉴别:用稀盐酸可一次性鉴别NaOH、 ,和 ,和 三种溶液 三种溶液 |
| D.物质的性质:还原剂转移电子给氧化剂 |
您最近一年使用:0次
2021-11-26更新
|
200次组卷
|
2卷引用:重庆市缙云教育联盟2022届高三第二次诊断性检测化学试题
解题方法
8 . [化学-选修2:化学与技术]碳酸钠的用途很广,可用做冶金、纺织、漂染等工业的基本原料。请根据题意回答下列问题:
Ⅰ.世界最早工业生产碳酸钠的方法是路布兰(N.Leblanc)法。其流程如下:
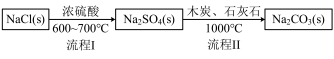
(1)流程I的另一产物是____ ,流程Ⅱ的反应分步进行:a. Na2SO4+C Na2S+CO↑
Na2S+CO↑
b.Na2S与石灰石发生复分解反应,总反应方程式可表示为__________________ 。
Ⅱ.1862年,比利时人索尔维(ErnestSolvay)用氨碱法生产碳酸钠。反应原理如下:
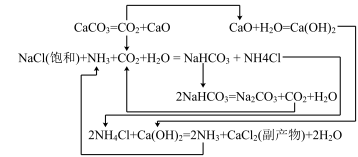
20℃时一些物质在水中的溶解度/g•(100gH2O)
(2)氨碱法生成纯碱的原料是____________ ,可循环利用的物质有____________ 。
(3)饱和NaCl溶液通NH3和CO2能生成NaHCO3的原因有:_________ 、__________ 、_________ 。
Ⅲ.我国化工专家侯德榜研究出联合制碱法,其反应原理和氨碱法类似,但将制氨和制碱联合,提高了原
料利用率。
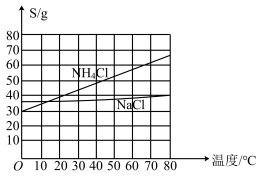
(4)生产中需向分离出NaHCO3后所得的溶液中加入NaCl固体并通入NH3,在________ (填温度范围)下析出________ (填化学式)。
Ⅰ.世界最早工业生产碳酸钠的方法是路布兰(N.Leblanc)法。其流程如下:

(1)流程I的另一产物是
 Na2S+CO↑
Na2S+CO↑ b.Na2S与石灰石发生复分解反应,总反应方程式可表示为
Ⅱ.1862年,比利时人索尔维(ErnestSolvay)用氨碱法生产碳酸钠。反应原理如下:

20℃时一些物质在水中的溶解度/g•(100gH2O)
| NaCl | NH4Cl | NaHCO3 | NH4HCO3 | Na2CO3 |
| 35.9 | 37.2 | 9.6 | 21.7 | 21.5 |
(3)饱和NaCl溶液通NH3和CO2能生成NaHCO3的原因有:
Ⅲ.我国化工专家侯德榜研究出联合制碱法,其反应原理和氨碱法类似,但将制氨和制碱联合,提高了原
料利用率。

(4)生产中需向分离出NaHCO3后所得的溶液中加入NaCl固体并通入NH3,在
您最近一年使用:0次
2016-12-09更新
|
268次组卷
|
2卷引用:2016届重庆市一中高三下学期模拟考试理综化学试卷



