名校
1 . 下列关于工业生产说法不正确 的是
| A.铝制品可用化学氧化法增加膜的厚度及对氧化膜进行着色 |
| B.工业上用电解熔融氧化物的方法制金属镁和铝 |
| C.氯碱工业中使用阳离子交换膜防止副反应的发生 |
| D.工业制备硫酸时在吸收塔中使用浓硫酸吸收三氧化硫 |
您最近一年使用:0次
2022-12-22更新
|
311次组卷
|
3卷引用:浙江省金华第一中学等四校2022-2023学年高三上学期12月联考化学试题
浙江省金华第一中学等四校2022-2023学年高三上学期12月联考化学试题浙江省(杭州二中、温州中学、金华一中、绍兴一中)四校2023届高三上学期12月联考化学试题(已下线)【2023】【高二下】【十四凤起】【期中考】【高中化学】【洪翔峰收集】
解题方法
2 . 为提高家庭应对突发事件的应急能力,2020年国家印发了“全国家庭应急物资储备建议清单”,其中小柴胡颗粒和医用口罩列于清单中。
回答下列问题。
(1)小柴胡颗粒的有效成分均从植物中提取,属于_______ (填“天然”或“合成”)药物。铝碳酸镁片中的有效成分Mg(OH)2、Al(OH)3等物质呈碱性,故具有_______ (填“抗酸”或“抗碱”)作用。
(2)熔喷布是一次性医用口罩的关键材料,由熔融态聚丙烯电喷形成的超细纤维经驻极静电处理制成。聚丙烯由_______ (写结构简式)聚合而成,熔喷布内部孔径_______ (填“大于”或“小于”)病毒气溶胶的粒径,且布料所带静电也能吸附病毒,从而有效阻止病毒通过,但允许参与人体呼吸的氧气等气体小分子自由通过,确保正常呼吸。分类回收的废弃口罩中的大部分材质难降解,且可能带有病毒,故采用_______ (填“焚烧”或“填埋”)处理更佳。
回答下列问题。
(1)小柴胡颗粒的有效成分均从植物中提取,属于
(2)熔喷布是一次性医用口罩的关键材料,由熔融态聚丙烯电喷形成的超细纤维经驻极静电处理制成。聚丙烯由
您最近一年使用:0次
解题方法
3 . 下列离子方程式中,书写正确的是
| A.将稀硫酸滴在铜片上:Cu+2H+=Cu2++H2↑ |
| B.将氧化镁与稀盐酸混合:MgO+2H+=Mg2++H2O |
| C.NaHSO4溶液与KOH溶液反应:H++OH-=H2O |
| D.将稀盐酸滴在石灰石上:CaCO3+2H+=Ca2++H2CO3 |
您最近一年使用:0次
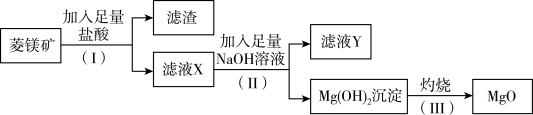
4 . 菱镁矿(主要成分为 ,还含有少量
,还含有少量 、
、 )制备
)制备 的流程如图。下列说法正确的是
的流程如图。下列说法正确的是
 ,还含有少量
,还含有少量 、
、 )制备
)制备 的流程如图。下列说法正确的是
的流程如图。下列说法正确的是
A.步骤(Ⅰ)得到的滤渣主要成分为 | B.步骤(Ⅱ)发生的反应有2个 |
| C.步骤(Ⅲ)操作可在蒸发皿中进行 | D.滤液Y中加入足量氨水可得到白色沉淀 |
您最近一年使用:0次
2022-12-10更新
|
465次组卷
|
2卷引用:安徽省皖江名校联盟2022-2023学年高三上学期12月第四次联考化学试题
名校
解题方法
5 . 下列操作不能 达到目的的是
| 实验目的 | 相关操作 | |
| A | 除去NaCl固体中少量的MgCl2 | 将固体溶解,向所得溶液中加入过量NaOH溶液,过滤,加热蒸干滤液 |
| B | 除去FeCl2溶液中混有少量FeCl3 | 向溶液中加入足量Fe粉,过滤 |
| C | 除去O2气体中的CO2 | 将混合气体缓缓通过盛有足量Na2O2的干燥管 |
| D | 除去CO2气体中混有的HCl | 将混合气体通过盛有足量饱和食盐水的洗气瓶 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
6 . 通过海水晾晒可得粗盐,粗盐中除NaCl外,还含有 、
、 、
、 以及泥沙等杂质,需要提纯后才能综合利用。某同学利用给定试剂NaOH溶液、
以及泥沙等杂质,需要提纯后才能综合利用。某同学利用给定试剂NaOH溶液、 溶液、
溶液、 溶液和盐酸,设计了如图粗盐精制的实验流程。(提示:根据实验目的,请思考试剂的用量)
溶液和盐酸,设计了如图粗盐精制的实验流程。(提示:根据实验目的,请思考试剂的用量)
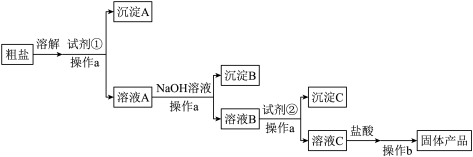
请回答:
(1)操作a名称是_______ 。
(2)试剂①是_______ 溶液(填化学式)。
(3)加入NaOH后,得到的主要沉淀B是_______ 。
(4)加入试剂②后,发生反应的离子方程式有_______ 。
(5)如果加入试剂②后直接加盐酸,产生的后果是_______ (用离子方程式表示)。
 、
、 、
、 以及泥沙等杂质,需要提纯后才能综合利用。某同学利用给定试剂NaOH溶液、
以及泥沙等杂质,需要提纯后才能综合利用。某同学利用给定试剂NaOH溶液、 溶液、
溶液、 溶液和盐酸,设计了如图粗盐精制的实验流程。(提示:根据实验目的,请思考试剂的用量)
溶液和盐酸,设计了如图粗盐精制的实验流程。(提示:根据实验目的,请思考试剂的用量)
请回答:
(1)操作a名称是
(2)试剂①是
(3)加入NaOH后,得到的主要沉淀B是
(4)加入试剂②后,发生反应的离子方程式有
(5)如果加入试剂②后直接加盐酸,产生的后果是
您最近一年使用:0次
名校
解题方法
7 . 下列有关物质的类别的说法正确的是
| A.只含有一种元素的物质不一定是单质 |
| B.2022年6月5日“神舟十四号”载人飞船成功发射。火箭采用的高强度钛合金属于化合物 |
| C.体操运动员比赛前为了防滑在手掌上涂抹的碳酸镁,根据树状分类法,属于镁盐、碳酸盐、正盐 |
| D. FeSO4∙7H2O是由FeSO4和H2O按个数比1:7所组成的混合物 |
您最近一年使用:0次
8 . 从某固体混合物中提纯KCl固体的流程图如图,试回答下列问题:
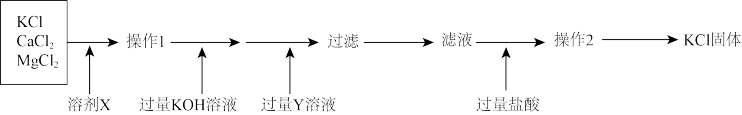
(1)溶剂X是____ ,加入过量KOH溶液发生的主要反应的离子方程式为_____ 。
(2)Y是____ ,过滤步骤得到的滤渣的主要成分为_____ (以上两空填写化学式)。
(3)过量盐酸的作用是____ ,加入盐酸后发生的反应的离子方程式为____ 。
(4)常温下,MgCO3在水中的溶解性为_____ (填“难溶”、“易溶”或“微溶”)。
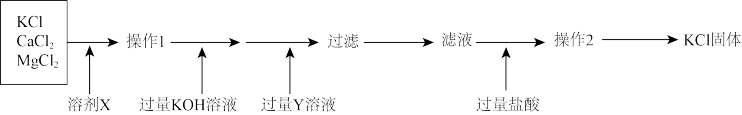
(1)溶剂X是
(2)Y是
(3)过量盐酸的作用是
(4)常温下,MgCO3在水中的溶解性为
您最近一年使用:0次
9 . 往下列烧杯中分别滴加一定量的饱和氯化镁溶液,一定会产生沉淀的是
| 化学试剂 |  |  |  |  |
| 选项 | A | B | C | D |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
10 . 利用工业废渣(主要成分为MgCO3、MgSiO3和少量Fe2O3)制备MgCO3•3H2O。
实验步骤如下:
步骤1:将废渣加入30%H2SO4溶液中,待其充分反应后进行操作1。
步骤2:向“步骤1”所得的溶液中加入有机萃取剂HX(密度小于水)萃取Fe3+,静置分层后进行操作2。
步骤3:边搅拌边向“步骤2”所得的水溶液中滴加Na2CO3溶液,至有大量沉淀生成,过滤、用蒸馏水洗涤、干燥,得到MgCO3•3H2O。
回答下列问题:
(1)步骤1发生反应时温度控制在80℃,边加入废渣边搅拌。
①适宜的加热方式为____ ,含镁化合物发生反应的离子方程式为MgSiO3+2H+=Mg2++H2SiO3、____ 。
②判断废渣充分反应的方法为____ ,所加H2SO4不宜过多的原因是____ 。
(2)“步骤2”中HX萃取Fe3+的原理为Fe3+(aq)+3HX=FeX3(org)+3H+(aq),org表示有机相。
①“操作1”和“操作2”的名称分别为____ 、____ ,萃取过程中水溶液的pH将____ (填“升高”“降低”或“不变”)。
②萃取的具体操作为将萃取剂HX加入“步骤1”所得的溶液中____ 静置;重复多次“步骤2”,其目的是____ 。
(3)“步骤3”中检验MgCO3•3H2O洗涤干净的具体操作为____ 。
实验步骤如下:
步骤1:将废渣加入30%H2SO4溶液中,待其充分反应后进行操作1。
步骤2:向“步骤1”所得的溶液中加入有机萃取剂HX(密度小于水)萃取Fe3+,静置分层后进行操作2。
步骤3:边搅拌边向“步骤2”所得的水溶液中滴加Na2CO3溶液,至有大量沉淀生成,过滤、用蒸馏水洗涤、干燥,得到MgCO3•3H2O。
回答下列问题:
(1)步骤1发生反应时温度控制在80℃,边加入废渣边搅拌。
①适宜的加热方式为
②判断废渣充分反应的方法为
(2)“步骤2”中HX萃取Fe3+的原理为Fe3+(aq)+3HX=FeX3(org)+3H+(aq),org表示有机相。
①“操作1”和“操作2”的名称分别为
②萃取的具体操作为将萃取剂HX加入“步骤1”所得的溶液中
(3)“步骤3”中检验MgCO3•3H2O洗涤干净的具体操作为
您最近一年使用:0次
2022-10-19更新
|
130次组卷
|
2卷引用:广东省河源中学2022-2023学年高三10月教学质量检测化学试题



