1 . 卤块的主要成分是MgCl2,此外还含Fe3+、Fe2+和Mn2+等离子。若以它为原料按下图所示工艺流程进行生产,可制得轻质氧化镁。
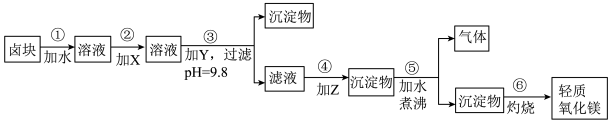
若要求产品尽量不含杂质,而且生产成本较低,请根据表1和表2提供的资料,填写空白:
表1 生成氢氧化物沉淀的pH
﹡Fe2+氢氧化物呈絮状,不易从溶液中除去,所以,常将它氧化为Fe3+,生成Fe(OH)3沉淀除去
表2 原料价格表
(1)在步骤②中加入的试剂X,最佳的选择是____________ ,其作用是_________________ ;
(2)在步骤③中加入的试剂应是_______________________ ;之所以要控制pH=9.8,其目的是___________________________________________________________ 。
(3)在步骤④中加入的试剂Z应是________________ ;
(4)在步骤⑤中发生反应的化学方程式是_____________________________________________ 。

若要求产品尽量不含杂质,而且生产成本较低,请根据表1和表2提供的资料,填写空白:
表1 生成氢氧化物沉淀的pH
| 物质 | 开始沉淀 | 沉淀完全 |
| Fe(OH)3 | 2.7 | 3.7 |
| Fe(OH)2 | 7.6 | 9.6﹡ |
| Mn(OH)2 | 8.3 | 9.8 |
| Mg(OH)2 | 9.6 | 11.1 |
表2 原料价格表
| 物质 | 价格/(元·吨-1) |
| 漂液(含25.2%NaClO) | 450 |
| 双氧水(含30%H2O2) | 2400 |
| 烧碱(含98%NaOH) | 2100 |
| 纯碱(含99.5%Na2CO3) | 600 |
(2)在步骤③中加入的试剂应是
(3)在步骤④中加入的试剂Z应是
(4)在步骤⑤中发生反应的化学方程式是
您最近一年使用:0次
名校
解题方法
2 . 下列有关物质的性质与用途具有对应关系的是
| A.MgCO3分解吸热,可用于治疗胃酸过多 |
| B.浓硫酸难挥发,可用于催化酯化反应 |
| C.FeCl3具有氧化性,可用作净水剂 |
| D.碳酸钠溶液呈碱性,可用于去除油污 |
您最近一年使用:0次
2020-12-23更新
|
194次组卷
|
2卷引用:江苏省南通市如皋中学2020-2021学年高三上学期教学质量调研(二)化学试题
名校
3 . 卤块的主要成分是MgCl2,此外还含Fe3+、Fe2+和Mn2+等离子。以卤块为原料可制得轻质氧化镁,工艺流程如图:
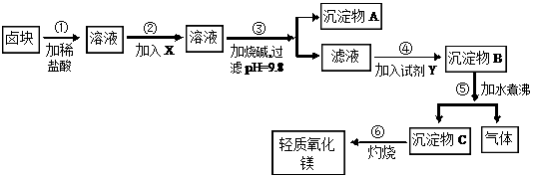
已知:Fe2+氢氧化物呈絮状,不易从溶液中除去,所以常将它氧化为Fe3+,生成Fe(OH)3沉淀除去。若要求产品尽量不含杂质,请根据表1和表2提供的资料,填写空白:
(1)在步骤②中加入的试剂X(从表2中选择)是_______ 而不是双氧水,其原因是_______________________ 。写出加入X发生反应的离子方程式_______________________ 。
(2)在步骤③中控制pH=9.8,其目的是____________________________ 。
(3)沉淀物A的成分为______________ ,试剂Y(从表2中选择)应该是_______ 。
(4)在步骤⑤中发生反应的化学方程式是________________________ 。
(5)若在实验室中完成步骤⑥,则沉淀物C必需在_______ (填仪器名称)中灼烧。

已知:Fe2+氢氧化物呈絮状,不易从溶液中除去,所以常将它氧化为Fe3+,生成Fe(OH)3沉淀除去。若要求产品尽量不含杂质,请根据表1和表2提供的资料,填写空白:
| 表1 生成氢氧化物沉淀的pH | 表2 化学试剂价格表 | ||||
| 物质 | 开始沉淀 | 沉淀完全 | 试剂 | 价格(元/吨) | |
| Fe(OH)3 | 2.7 | 3.7 | 漂液(含25.2% NaClO) | 450 | |
| Fe(OH)2 | 7.6 | 9.6 | 双氧水(含30% H2O2) | 2400 | |
| Mn(OH)2 | 8.3 | 9.8 | 烧碱(含98% NaOH) | 2100 | |
| Mg(OH)2 | 10.0 | 11.1 | 纯碱(含99.5% Na2CO3) | 600 | |
(1)在步骤②中加入的试剂X(从表2中选择)是
(2)在步骤③中控制pH=9.8,其目的是
(3)沉淀物A的成分为
(4)在步骤⑤中发生反应的化学方程式是
(5)若在实验室中完成步骤⑥,则沉淀物C必需在
您最近一年使用:0次
解题方法
4 . 卤块的主要成分是MgCl2,此外还含Fe3+、Fe2+和Mn2+等离子。若以它为原料按下图所示工艺流程进行生产,可制得轻质氧化镁(已知其中有一种中间产物是MgCO3)。
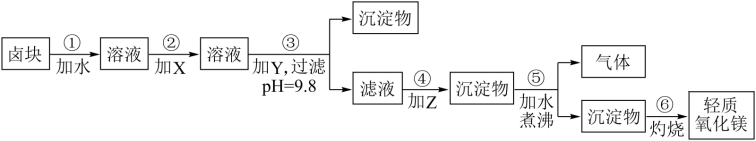
若要求产品尽量不含杂质,而且生产成本较低,根据表1和表2提供的资料,填写空白:
表1生成氢氧化物沉淀的pH
表2原料价格表
已知:Fe2+氢氧化物呈絮状,不易从溶液中除去,常将它氧化为Fe3+,生成Fe(OH)3沉淀除去。
(1)在步骤②中加入的试剂X,最佳的选择是______,其反应的离子方程式是 。
(2)在步骤③中如要控制pH=9.8,其目的是______;在步骤④中加入的试剂Z应是______;
(3)在步骤⑤中发生的化学方程式是______。

若要求产品尽量不含杂质,而且生产成本较低,根据表1和表2提供的资料,填写空白:
表1生成氢氧化物沉淀的pH
| 物质 | 开始沉淀 | 沉淀完全 |
| Fe(OH)3 | 2.7 | 3.7 |
| Fe(OH)2 | 7.6 | 9.6 |
| Mn(OH)2 | 8.3 | 9.8 |
| Mg(OH)2 | 9.6 | 11.1 |
表2原料价格表
| 物质 | 价格/元・吨-1 |
| 漂液(含25.2%NaClO) | 450 |
| 双氧水(含30%H2O2) | 2400 |
已知:Fe2+氢氧化物呈絮状,不易从溶液中除去,常将它氧化为Fe3+,生成Fe(OH)3沉淀除去。
(1)在步骤②中加入的试剂X,最佳的选择是______,其反应的离子方程式是 。
(2)在步骤③中如要控制pH=9.8,其目的是______;在步骤④中加入的试剂Z应是______;
(3)在步骤⑤中发生的化学方程式是______。
您最近一年使用:0次
解题方法
5 . 碱式氯化镁(MgOHCl)常用作塑料添加剂,我国首创利用氢氧化镁与氯化铵热分解制氨气并得到碱式氯化镁的工艺。某科研小组根据该原理设计了如图实验装置制备碱式氧化镁并探究氨的还原性,反应前,装置C中CuO的质量为14.40g。
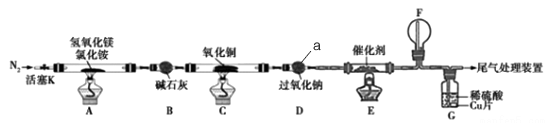
请回答下列问题:
(1)仪器a的名称是_______ .
(2)装置A中发生反应的化学方程式为____________ ,装置B的作用是_________ ,装置D的作用是________
(3)装置G中的现象为____________
(4)反应结束后装置C中的氧化铜完全反应生成红色固体,并测得其质量为12.24g。则红色固体是______ (填化学式),该反应中转移电子的物质的量为_______ mol.
(5)完成下列实验方案,证明装置C中完全反应后得到的红色固体中含有氧化亚铜(供选择的试剂:2mol/L的HNO3溶液、2mol/L的H2SO4溶液、2mol/L的NaOH溶液)。
已知:Cu2O+2H+=Cu2++Cu+H2O.

请回答下列问题:
(1)仪器a的名称是
(2)装置A中发生反应的化学方程式为
(3)装置G中的现象为
(4)反应结束后装置C中的氧化铜完全反应生成红色固体,并测得其质量为12.24g。则红色固体是
(5)完成下列实验方案,证明装置C中完全反应后得到的红色固体中含有氧化亚铜(供选择的试剂:2mol/L的HNO3溶液、2mol/L的H2SO4溶液、2mol/L的NaOH溶液)。
已知:Cu2O+2H+=Cu2++Cu+H2O.
| 实验步骤 | 预期现象和结论 |
| 步骤1取装置C中所得红色固体于大试管中 | ----- |
| 步骤2: |
您最近一年使用:0次
6 . Mg和SiO2在高温下反应生成MgO和Mg2Si。下列说法正确的是
| A.物质的熔点:Mg>MgO | B.氧元素不存在同素异形体 |
| C.Mg的还原性强于Si | D.该反应是置换反应,镁元素被氧化 |
您最近一年使用:0次
名校
解题方法
7 . 下列有关物质性质及其对应用途的说法正确的是
| A.晶体硅是半导体,故在通信工程中用于制光导纤维 |
| B.氧化镁的熔点高,故可作耐高温材料 |
| C.碳酸氢钠受热易分解,因此可用于治疗胃酸过多 |
| D.明矾具有强氧化性,因此常用于自来水的杀菌消毒 |
您最近一年使用:0次
名校
8 . 下列物质的性质与应用关系的描述不正确的是
| A.氧化镁的熔点高,是优质的耐高温材料 |
| B.金属钠着火,不可用泡沫灭火器灭火 |
| C.氯气有强氧化性,可用氯气漂白干燥的有色布条 |
| D.二氧化硫有漂白性,可用于漂白毛,丝,纸浆 |
您最近一年使用:0次
9 . 下列说法正确的是
| A.MgO的熔点高,因此被用于制造火箭、导弹和飞机的部件 |
| B.石灰石是高炉炼铁的原料之一,炉渣可用于制造水泥 |
| C.浓硫酸具有强氧化性,故不能用铁制容器贮存浓硫酸 |
| D.晶体硅熔点高、硬度大,故常用于制作芯片 |
您最近一年使用:0次
10 . 用下列实验装置进行相应实验,装置正确且能达到实验目的的是
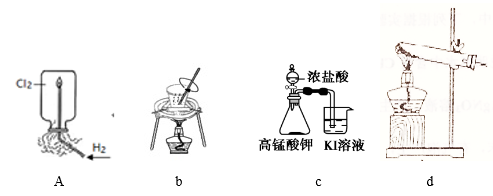

| A.用图a所示装置验证H2在Cl2中燃烧的实验现象 |
| B.用图b所示装置从饱和食盐水中提取氯化钠 |
| C.用图c所示装置探究氧化性:KMnO4>Cl2>I2 |
| D.用图d所示装置分解MgCl2·6H2O获取MgCl2 |
您最近一年使用:0次



