1 . 下列有关金属及其化合物描述正确的是
A. 常被用作焙制糕点时的膨松剂 常被用作焙制糕点时的膨松剂 |
B. 中阴、阳离子的个数比为1∶1 中阴、阳离子的个数比为1∶1 |
| C.在酒精灯上加热铝箔,铝箔熔化但不滴落,说明Al的熔点很高 |
D.用铂丝蘸取某溶液,通过焰色试验,直接观察,火焰颜色呈黄色,推断原溶液中不含 |
您最近一年使用:0次
解题方法
2 . 下列除杂试剂选用错误的一组是
| 物质(杂质) | 除杂试剂 | |
| A | 乙醇(H2O) | 生石灰 |
| B | NaHCO3溶液(Na2CO3) | 盐酸 |
| C | 氧化铁(氧化铝) |  溶液 溶液 |
| D | Cl2(HCl) | 饱和食盐水 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
3 . 铝元素是地壳中含量最多的金属元素,常以化合态的形式存在于铝土矿中,其氧化物具有两性, 与
与 类似。
类似。
Ⅰ.工业上常常从铝土矿(主要成分为 ,含
,含 、
、 杂质)中提取
杂质)中提取 ,并通过电解法制备铝单质。请根据流程图,回答相关问题。
,并通过电解法制备铝单质。请根据流程图,回答相关问题。

已知: 属于两性氢氧化物,既能溶于稀盐酸又能溶于NaOH溶液。
属于两性氢氧化物,既能溶于稀盐酸又能溶于NaOH溶液。
(1)写出“滤渣A”的化学式:_______ ;过滤时,玻璃棒的作用为_______ ;“滤液B”中的溶质为 、
、_______ (写化学式)。
(2)上述流程中“过量氨水”能否改为“过量NaOH溶液”?_______ (填“能”或“不能”),请用离子方程式解释:_______ 。
Ⅱ.已知 能与NaOH溶液反应生成亚铬酸钠(
能与NaOH溶液反应生成亚铬酸钠( ),
), 可由
可由 和硫黄(S)混合后进行反应得到,发生反应的化学方程式为
和硫黄(S)混合后进行反应得到,发生反应的化学方程式为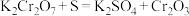 ,再经湿磨、热水洗涤、压滤、干燥、粉碎制得。回答下到问题:
,再经湿磨、热水洗涤、压滤、干燥、粉碎制得。回答下到问题:
(3)写出 与NaOH溶液反应的化学方程式:
与NaOH溶液反应的化学方程式:_______ 。
(4)由 和硫黄制取
和硫黄制取 的废水中含有一定量的
的废水中含有一定量的 ,Cr元素含量达标才能排放,可以加入
,Cr元素含量达标才能排放,可以加入 溶液去除酸性废水中的
溶液去除酸性废水中的 ,使
,使 转化为
转化为 而自身转化为三价铁,再放入沉淀池,达到指定标准后方可排放。上述过程
而自身转化为三价铁,再放入沉淀池,达到指定标准后方可排放。上述过程 溶液与
溶液与 发生的反应中氧化剂与还原剂的物质的量之比为
发生的反应中氧化剂与还原剂的物质的量之比为_______ 。
(5)某兴趣小组同学想根据上述反应原理测出该酸性废水中残留的 的物质的量浓度,采样后,经初步预算需要
的物质的量浓度,采样后,经初步预算需要 的
的 溶液240mL,配制该溶液时至少需称量
溶液240mL,配制该溶液时至少需称量_______ g 。
。
 与
与 类似。
类似。Ⅰ.工业上常常从铝土矿(主要成分为
 ,含
,含 、
、 杂质)中提取
杂质)中提取 ,并通过电解法制备铝单质。请根据流程图,回答相关问题。
,并通过电解法制备铝单质。请根据流程图,回答相关问题。
已知:
 属于两性氢氧化物,既能溶于稀盐酸又能溶于NaOH溶液。
属于两性氢氧化物,既能溶于稀盐酸又能溶于NaOH溶液。(1)写出“滤渣A”的化学式:
 、
、(2)上述流程中“过量氨水”能否改为“过量NaOH溶液”?
Ⅱ.已知
 能与NaOH溶液反应生成亚铬酸钠(
能与NaOH溶液反应生成亚铬酸钠( ),
), 可由
可由 和硫黄(S)混合后进行反应得到,发生反应的化学方程式为
和硫黄(S)混合后进行反应得到,发生反应的化学方程式为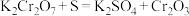 ,再经湿磨、热水洗涤、压滤、干燥、粉碎制得。回答下到问题:
,再经湿磨、热水洗涤、压滤、干燥、粉碎制得。回答下到问题:(3)写出
 与NaOH溶液反应的化学方程式:
与NaOH溶液反应的化学方程式:(4)由
 和硫黄制取
和硫黄制取 的废水中含有一定量的
的废水中含有一定量的 ,Cr元素含量达标才能排放,可以加入
,Cr元素含量达标才能排放,可以加入 溶液去除酸性废水中的
溶液去除酸性废水中的 ,使
,使 转化为
转化为 而自身转化为三价铁,再放入沉淀池,达到指定标准后方可排放。上述过程
而自身转化为三价铁,再放入沉淀池,达到指定标准后方可排放。上述过程 溶液与
溶液与 发生的反应中氧化剂与还原剂的物质的量之比为
发生的反应中氧化剂与还原剂的物质的量之比为(5)某兴趣小组同学想根据上述反应原理测出该酸性废水中残留的
 的物质的量浓度,采样后,经初步预算需要
的物质的量浓度,采样后,经初步预算需要 的
的 溶液240mL,配制该溶液时至少需称量
溶液240mL,配制该溶液时至少需称量 。
。
您最近一年使用:0次
2023-06-08更新
|
239次组卷
|
2卷引用:广东省清远市2022-2023学年高一上学期期末考试化学试题
名校
4 . 陈述I和陈述II均正确,且具有因果关系的
| 选项 | 陈述I | 陈述II |
| A | 钠金属性比钾强 | 可用Na和熔融KCl在高温下反应制备K |
| B | 过氧化钠用于制造呼吸面具 | 过氧化钠与人呼出的H2O、CO2都能发生反应生成O2 |
| C | Al2O3的熔点高 | 可用氧化铝坩埚熔化NaOH固体 |
| D | 浓硫酸具有吸水性 | 用浓硫酸干燥H2S |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
5 . 请按要求回答下列问题:
(1)钠在空气中燃烧生成淡黄色的固体,则其化学方程式为_______ ;
(2) 能溶于酸或强碱溶液生成盐和水,则是一种
能溶于酸或强碱溶液生成盐和水,则是一种_______ (填“酸性”、“碱性”或“两性”)氧化物;
(3)装氢氧化钠溶液的试剂瓶不能用玻璃塞,请用离子方程式表示原因:_______ 。
(4)某同学在做 的一次实验中,用过量的稀硝酸(其密度为1.05g/mL,
的一次实验中,用过量的稀硝酸(其密度为1.05g/mL, 的质量分数为12%)跟一定量的铁片反应,产生了标准状况下0.56L的一氧化氮,该稀硝酸的物质的量浓度为
的质量分数为12%)跟一定量的铁片反应,产生了标准状况下0.56L的一氧化氮,该稀硝酸的物质的量浓度为_______ ,被还原的 的物质的量为
的物质的量为_______ 。
(1)钠在空气中燃烧生成淡黄色的固体,则其化学方程式为
(2)
 能溶于酸或强碱溶液生成盐和水,则是一种
能溶于酸或强碱溶液生成盐和水,则是一种(3)装氢氧化钠溶液的试剂瓶不能用玻璃塞,请用离子方程式表示原因:
(4)某同学在做
 的一次实验中,用过量的稀硝酸(其密度为1.05g/mL,
的一次实验中,用过量的稀硝酸(其密度为1.05g/mL, 的质量分数为12%)跟一定量的铁片反应,产生了标准状况下0.56L的一氧化氮,该稀硝酸的物质的量浓度为
的质量分数为12%)跟一定量的铁片反应,产生了标准状况下0.56L的一氧化氮,该稀硝酸的物质的量浓度为 的物质的量为
的物质的量为
您最近一年使用:0次
6 . 铝是一种重要金属,从铝土矿(主要成分为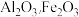 、
、 等)中冶炼Al的工业生产流程如图:
等)中冶炼Al的工业生产流程如图:
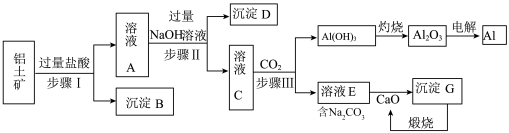
注: 是酸性氧化物,不溶于盐酸
是酸性氧化物,不溶于盐酸
(1)步骤Ⅰ、Ⅱ、Ⅲ都要用到的分离方法是___________ 。在实验室模拟该操作,要用到的玻璃仪器有:烧杯、___________ 、___________ 。
(2)溶液A含有的金属阳离子为___________ 。沉淀D的化学式为 ___________ 。
(3)步骤Ⅲ生成 沉淀的离子方程式为
沉淀的离子方程式为 ___________ 。
(4)生产过程中,可循环使用的物质有 、
、___________ 、___________ (填化学式)。
(5)经分析,a吨铝土矿可以冶炼出b吨的纯铝(假设各生产环节中无损耗),则理论上原铝土矿中 的纯度(质量分数)
的纯度(质量分数)___________ %(用含a、b的式子表示)。
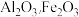 、
、 等)中冶炼Al的工业生产流程如图:
等)中冶炼Al的工业生产流程如图:
注:
 是酸性氧化物,不溶于盐酸
是酸性氧化物,不溶于盐酸(1)步骤Ⅰ、Ⅱ、Ⅲ都要用到的分离方法是
(2)溶液A含有的金属阳离子为
(3)步骤Ⅲ生成
 沉淀的离子方程式为
沉淀的离子方程式为 (4)生产过程中,可循环使用的物质有
 、
、(5)经分析,a吨铝土矿可以冶炼出b吨的纯铝(假设各生产环节中无损耗),则理论上原铝土矿中
 的纯度(质量分数)
的纯度(质量分数)
您最近一年使用:0次
7 . 下列离子方程式,正确的是
A.实验室制 胶体: 胶体: |
B.将氧化铝溶于 溶液: 溶液: |
C.用 溶液刻蚀覆铜板: 溶液刻蚀覆铜板: |
D.将稀盐酸滴在石灰石上: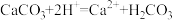 |
您最近一年使用:0次
名校
解题方法
8 . 某工厂以镍废渣(主要成分为Ni,含少量Fe、Fe3O4、Al2O3等)为原料制备翠矾(NiSO4·7H2O),其生产工艺如图。

(1)“碱浸”时发生反应的离子方程式为_______ 。
(2)实验室进行操作1需要用的玻璃仪器除了烧杯还有_______ 。
(3)通入空气氧化的目的是_______ ,也可以用一种绿色氧化剂代替空气中的氧气,写出该反应的离子方程式_______ 。
(4)滤渣B的成分是_______ (填化学式)。
(5)系列操作是将溶液经过_______ 、_______ 、过滤、洗涤、干燥得到NiSO4·7H2O晶体。
(6)NiSO4在强碱溶液中用NaClO氧化,可沉淀出能用作镍镉电池正极材料的NiOOH。写出该反应的离子方程式_______ 。

(1)“碱浸”时发生反应的离子方程式为
(2)实验室进行操作1需要用的玻璃仪器除了烧杯还有
(3)通入空气氧化的目的是
(4)滤渣B的成分是
(5)系列操作是将溶液经过
(6)NiSO4在强碱溶液中用NaClO氧化,可沉淀出能用作镍镉电池正极材料的NiOOH。写出该反应的离子方程式
您最近一年使用:0次
9 . 下列物质性质和用途正确且有对应关系的是
| 选项 | 物质性质 | 用途 |
| A |  受热易分解 受热易分解 |  可用作氮肥 可用作氮肥 |
| B | 钠单质燃烧火焰呈黄色 | 钠单质可用于制作烟花 |
| C |  溶液呈碱性 溶液呈碱性 |  可用作消毒剂 可用作消毒剂 |
| D |  是两性氧化物 是两性氧化物 | 铝制餐具不宜长时间蒸煮酸性或碱性食物 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
10 . 下列有关物质用途的说法正确的是
| A.明矾用作水处理的消毒剂 | B.过氧化钠可用作潜艇供氧剂 |
| C.Al2O3常用作耐火材料 | D.水玻璃可用作木材防火剂 |
您最近一年使用:0次



