名校
1 . 在指定溶液中下列离子能大量共存的是
A.透明澄清的溶液:K+、Fe3+、 、 、 |
B.能使紫色石蕊变红的溶液:Na+、Ba2+、[Al(OH)4]- 、 |
C.c(ClO-) = 0.3 mol/L的溶液:K+、Na+、 、S2- 、S2- |
D.加入Al能放出H2的溶液:Mg2+、 、 、 、 、 |
您最近一年使用:0次
2 . 我国铝材工业水平处于世界领先行列。下列关于金属铝及其合金的说法中,错误的是
| A.铝具有良好的导电性 |
| B.铝具有银白色金属光泽 |
| C.常温下,铝制品耐腐蚀是因为铝不活泼 |
| D.铝合金密度小、强度高,广泛应用于航空领域 |
您最近一年使用:0次
名校
3 . 下列陈述正确且有因果关系的是
| A.铝制容器表面有氧化膜保护,所以可用铝制容器盛装浓盐酸 |
B. 的密度小于空气,所以可用向下排空气法收集 的密度小于空气,所以可用向下排空气法收集 |
C. 具有还原性,所以不能用浓硫酸干燥 具有还原性,所以不能用浓硫酸干燥 |
D. 有导电性,所以 有导电性,所以 可用于制备光导纤维 可用于制备光导纤维 |
您最近一年使用:0次
解题方法
4 . 铝和铝合金是一类重要的金属材料。回答下列问题:
(1)除去镁粉中混有少量铝粉,应加入的试剂为___________ ,发生反应的离子方程式为___________ ,然后经过滤、洗涤、干燥。
(2)等质量的两份铝分别与足量的盐酸、氢氧化钠溶液反应,所得 在同温同压下的体积之比是
在同温同压下的体积之比是___________ 。
(3)某同学在实验室用铝土矿(含有 和
和 ,不考虑其他杂质)制取金属铝的流程如下:
,不考虑其他杂质)制取金属铝的流程如下: 与稀硫酸反应的离子方程式为
与稀硫酸反应的离子方程式为___________ 。
②滤液Ⅱ中溶质的用途之一是___________ 。
(1)除去镁粉中混有少量铝粉,应加入的试剂为
(2)等质量的两份铝分别与足量的盐酸、氢氧化钠溶液反应,所得
 在同温同压下的体积之比是
在同温同压下的体积之比是(3)某同学在实验室用铝土矿(含有
 和
和 ,不考虑其他杂质)制取金属铝的流程如下:
,不考虑其他杂质)制取金属铝的流程如下: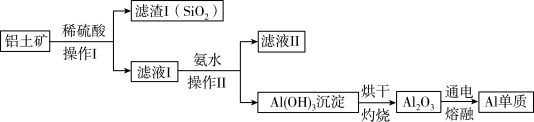
 与稀硫酸反应的离子方程式为
与稀硫酸反应的离子方程式为②滤液Ⅱ中溶质的用途之一是
您最近一年使用:0次
解题方法
5 . 已知浓度均为2.4 mol•L-1的硫酸溶液和氢氧化钠溶液各取100 mL,分别加入6.75 g的金属铝充分反应,则产生氢气的体积之比为
| A.1:1 | B.2:3 | C.3:2 | D.4:5 |
您最近一年使用:0次
6 . 可用Al与NaOH溶液反应来疏通下水管道。下列说法错误的是
| A.Al是还原剂,发生氧化反应 |
B.每生成1mol  ,转移2mol电子 ,转移2mol电子 |
| C.可用NaOH溶液除去镁粉中混有的少量Al粉 |
D.等量的铝与足量NaOH溶液反应生成的 比与足量盐酸反应生成的多 比与足量盐酸反应生成的多 |
您最近一年使用:0次
名校
解题方法
7 . 将0.1mol镁和铝的混合物溶于 稀硫酸中,然后滴加
稀硫酸中,然后滴加 的NaOH溶液。若在滴加NaOH溶液的过程中,沉淀质量随加入NaOH溶液体积的变化如图所示。
的NaOH溶液。若在滴加NaOH溶液的过程中,沉淀质量随加入NaOH溶液体积的变化如图所示。 、
、 刚好沉淀完全,则滴入NaOH溶液的体积
刚好沉淀完全,则滴入NaOH溶液的体积
_____ mL。
(2)当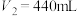 时,金属粉末中
时,金属粉末中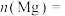
_____ ,
_____ mL。
 稀硫酸中,然后滴加
稀硫酸中,然后滴加 的NaOH溶液。若在滴加NaOH溶液的过程中,沉淀质量随加入NaOH溶液体积的变化如图所示。
的NaOH溶液。若在滴加NaOH溶液的过程中,沉淀质量随加入NaOH溶液体积的变化如图所示。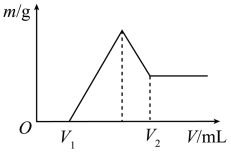
 、
、 刚好沉淀完全,则滴入NaOH溶液的体积
刚好沉淀完全,则滴入NaOH溶液的体积
(2)当
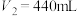 时,金属粉末中
时,金属粉末中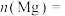

您最近一年使用:0次
解题方法
8 . 在标准状况下,实验甲、乙、丙各取30.0mL相同浓度的盐酸,然后分别慢慢加入组成相同的镁铝合金粉末,得下表中有关数据(假设反应前后溶液体积不变)。
下列说法不正确的是
| 实验序号 | 甲 | 乙 | 丙 |
| 合金质量/mg | 255 | 385 | 459 |
| 气体体积/mL | 280 | 336 | 336 |
| A.实验甲中盐酸过量 |
| B.实验乙中盐酸不足 |
| C.实验中c(HCl)=1.0mol/L |
| D.该镁铝合金粉末中Mg、Al的物质的量之比为2:1 |
您最近一年使用:0次
解题方法
9 . 已知浓度均为2.4 mol•L-1的硫酸溶液和氢氧化钠溶液各取100 mL,分别加入5.4 g的金属铝充分反应,则产生氢气的体积之比为
| A.1:1 | B.2:3 | C.3:2 | D.4:5 |
您最近一年使用:0次



