名校
解题方法
1 . 某化学实验小组同学利用如图所示装置制备氨气,并探究氨气的性质(部分仪器已略去)。___________ 。
(2)干燥氨气可选用的试剂是___________ (填序号)。
①浓H2SO4 ②碱石灰 ③P2O5
(3)收集氨气时,氨气的进气口为___________ (填“a”或“b”)。
(4)证明烧瓶中氨气集满的方法是___________ 。
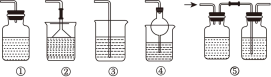
(5)为防止环境污染,下列装置中(盛放的液体均为水)可用于吸收多余氨气的是___________ (填序号)。___________ (填选项代号)。
a.装置Ⅰ中红色Fe2O3粉末变为黑色粉末,经检验是一种铁的氧化物
b.装置Ⅱ中无水CuSO4粉末变为蓝色
c.装置Ⅲ无水CaCl2的质量增加
d.生成一种无色无味气体,该气体无污染
(7)小组同学继续对(6)装置I反应后黑色粉末的组成进行探究。
(8)结合(6)(7)实验,写出(6)中NH3还原Fe2O3的化学方程式___________ 。
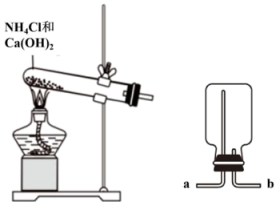
(2)干燥氨气可选用的试剂是
①浓H2SO4 ②碱石灰 ③P2O5
(3)收集氨气时,氨气的进气口为
(4)证明烧瓶中氨气集满的方法是
(5)为防止环境污染,下列装置中(盛放的液体均为水)可用于吸收多余氨气的是
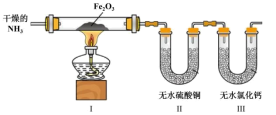
a.装置Ⅰ中红色Fe2O3粉末变为黑色粉末,经检验是一种铁的氧化物
b.装置Ⅱ中无水CuSO4粉末变为蓝色
c.装置Ⅲ无水CaCl2的质量增加
d.生成一种无色无味气体,该气体无污染
(7)小组同学继续对(6)装置I反应后黑色粉末的组成进行探究。
| 操作 | 现象 | 结论或离子方程式 |
| 步骤1:取少量黑色粉末于小烧杯中,加入过量盐酸 | 黑色粉末全部溶解,无气泡产生,溶液呈浅绿色 | 溶液中可能含有Fe2+ |
| 步骤2:取步骤1少量溶液于试管中,滴入2-3滴KSCN溶液,振荡 | 溶液颜色 | 溶液中不含有Fe3+ |
| 步骤3:向步骤2试管中滴入少量氯水 | 溶液变红色 | 涉及离子方程式有 Fe(SCN)3 Fe(SCN)3 |
您最近一年使用:0次
2024-05-27更新
|
226次组卷
|
2卷引用:北师大附属实验中学2023-2024学年度第二学期期中试卷
名校
解题方法
2 . 下列实验现象或操作不能达到相应实验目的的是
| 选项 | 实验目的 | 实验现象或操作 |
| A | 验证浓硫酸的脱水性 | 将浓硫酸滴加到蔗糖上,蔗糖变黑,体积膨胀,放出有刺激性气味的气体 |
| B | 验证Fe3+具有氧化性 | 向FeCl3溶液中加入过量铁粉,溶液由黄色变为浅绿色 |
| C | 验证浓硝酸可被炭还原为NO2 | 将炽热的木炭加入浓硝酸中,有红棕色气体产生 |
| D | 验证NH3具有还原性 | 将NH3通过灼热的CuO,黑色固体变为红色 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-02-10更新
|
1016次组卷
|
6卷引用:北京师范大学附属实验中学2022-2023学年高一下学期3月月考化学试题
名校
3 . 某小组研究溶液中 与
与 、
、 的反应。
的反应。
资料: 在溶液中呈棕色。
在溶液中呈棕色。
(1)研究现象a中的黄色溶液。
①用___________ 溶液检出溶液中含有 。
。
②甲认为是O2氧化了溶液中的 。乙认为O2不是主要原因,理由是
。乙认为O2不是主要原因,理由是___________ 。
③进行实验Ⅱ,装置如下图。左侧烧杯中的溶液只变为黄色,不变为棕色,右侧电极上产生无色气泡,经检验该气体为NO。产生NO的电极反应式是___________ 。实验Ⅱ的目的是___________ 。
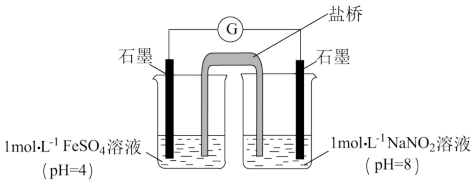
(2)研究现象a中的棕色溶液。
①综合实验I和实验Ⅱ,提出假设:现象a中溶液变为棕色可能是NO与溶液中的 或
或 发生了反应。进行实验Ⅲ,证实溶液呈棕色只是因为
发生了反应。进行实验Ⅲ,证实溶液呈棕色只是因为 与NO发生了反应。实验Ⅲ的操作和现象是
与NO发生了反应。实验Ⅲ的操作和现象是___________ 。
②加热实验I中的棕色溶液,有气体逸出,该气体在接近试管口处变为红棕色,溶液中有红褐色沉淀生成。解释产生红褐色沉淀的原因是___________ 。
(3)研究酸性条件下,溶液中 与
与 、
、 的反应。
的反应。
①i中溶液变为棕色的离子方程式是___________ 、___________ 。
②iii中出现棕色的原因是___________ 。
实验结论:本实验条件下,溶液中 、
、 的氧化性与溶液的酸碱性等有关。
的氧化性与溶液的酸碱性等有关。
 与
与 、
、 的反应。
的反应。| 实验Ⅰ | 试剂 | 现象 | |
| 滴管 | 试管 | ||
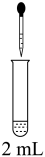 |  溶液(pH=4) 溶液(pH=4) |  溶液(pH=8) 溶液(pH=8) | a.滴入1滴FeSO4溶液,溶液变黄色,继续滴加,溶液变为棕色。2小时后,无明显变化 |
 溶液(加NaOH溶液至pH=8) 溶液(加NaOH溶液至pH=8) | b.持续滴加FeSO4溶液,无明显变化。 | ||
 在溶液中呈棕色。
在溶液中呈棕色。(1)研究现象a中的黄色溶液。
①用
 。
。②甲认为是O2氧化了溶液中的
 。乙认为O2不是主要原因,理由是
。乙认为O2不是主要原因,理由是③进行实验Ⅱ,装置如下图。左侧烧杯中的溶液只变为黄色,不变为棕色,右侧电极上产生无色气泡,经检验该气体为NO。产生NO的电极反应式是

(2)研究现象a中的棕色溶液。
①综合实验I和实验Ⅱ,提出假设:现象a中溶液变为棕色可能是NO与溶液中的
 或
或 发生了反应。进行实验Ⅲ,证实溶液呈棕色只是因为
发生了反应。进行实验Ⅲ,证实溶液呈棕色只是因为 与NO发生了反应。实验Ⅲ的操作和现象是
与NO发生了反应。实验Ⅲ的操作和现象是②加热实验I中的棕色溶液,有气体逸出,该气体在接近试管口处变为红棕色,溶液中有红褐色沉淀生成。解释产生红褐色沉淀的原因是
(3)研究酸性条件下,溶液中
 与
与 、
、 的反应。
的反应。| 序号 | 操作 | 现象 |
| i | 取 的NaNO2溶液,加醋酸至pH=3,加入 的NaNO2溶液,加醋酸至pH=3,加入 溶液 溶液 | 溶液立即变为棕色 |
| ii | 取 的NaNO3溶液,加醋酸至pH=3,加入 的NaNO3溶液,加醋酸至pH=3,加入 溶液 溶液 | 无明显变化 |
| iii | 分别取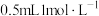 的NaNO3溶液与 的NaNO3溶液与 的FeSO4溶液,混合,小心加入0.5mL浓硫酸 的FeSO4溶液,混合,小心加入0.5mL浓硫酸 | 液体分为两层,稍后,在两层液体界面上出现棕色环 |
②iii中出现棕色的原因是
实验结论:本实验条件下,溶液中
 、
、 的氧化性与溶液的酸碱性等有关。
的氧化性与溶液的酸碱性等有关。
您最近一年使用:0次
4 . 实验小组发现新配制的 溶液放置一段时间,由浅绿色溶液变为黄色浊液A,进行如下探究。
溶液放置一段时间,由浅绿色溶液变为黄色浊液A,进行如下探究。
资料:i.胶体可以透过滤纸。 ii. 与
与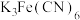 溶液反应,生成蓝色沉淀。
溶液反应,生成蓝色沉淀。
(1)探究A中的成分,进行如下实验。
①取少量A,过滤得到红褐色沉淀和黄色透明液体B。
②取少量B于试管中,加入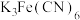 溶液,
溶液,_______ (填现象)。
③取少量B于试管中,加入_______ (填试剂),液体变为红色。
④用激光笔照射B,看到一条光亮的“通路”。
综合上述实验,说明A中铁元素的存在形态有 、
、 、
、_______ 和_______ 。
(2)进一步探究B显黄色的原因。_______ (用离子方程式表示)。
②由上述实验得出:B显黄色的主要原因不是因为含有 ,而是因为含有
,而是因为含有_______ 。理由是: _______ 。
(3)测定A的变质程度并分析对后续实验的影响。
①取25.00mL A,加入足量稀硫酸,可与24.00mL 溶液恰好完全反应。已知
溶液恰好完全反应。已知 在酸性环境下被还原为
在酸性环境下被还原为 ,A中
,A中 的浓度为
的浓度为_______  ,说明其主要成分仍然是
,说明其主要成分仍然是 。
。
②下列实验可以使用A进行的是_______ (填字母)。
a.向A中滴入NaOH溶液,制备纯净的 沉淀
沉淀
b.用A处理含有+6价Cr的酸性废水,将剧毒的+6价Cr还原至低毒的+3价
经过上述探究,实验小组对 溶液的配制与使用有了更深入的理解。
溶液的配制与使用有了更深入的理解。
 溶液放置一段时间,由浅绿色溶液变为黄色浊液A,进行如下探究。
溶液放置一段时间,由浅绿色溶液变为黄色浊液A,进行如下探究。资料:i.胶体可以透过滤纸。 ii.
 与
与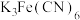 溶液反应,生成蓝色沉淀。
溶液反应,生成蓝色沉淀。(1)探究A中的成分,进行如下实验。
①取少量A,过滤得到红褐色沉淀和黄色透明液体B。
②取少量B于试管中,加入
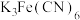 溶液,
溶液,③取少量B于试管中,加入
④用激光笔照射B,看到一条光亮的“通路”。
综合上述实验,说明A中铁元素的存在形态有
 、
、 、
、(2)进一步探究B显黄色的原因。

②由上述实验得出:B显黄色的主要原因不是因为含有
 ,而是因为含有
,而是因为含有(3)测定A的变质程度并分析对后续实验的影响。
①取25.00mL A,加入足量稀硫酸,可与24.00mL
 溶液恰好完全反应。已知
溶液恰好完全反应。已知 在酸性环境下被还原为
在酸性环境下被还原为 ,A中
,A中 的浓度为
的浓度为 ,说明其主要成分仍然是
,说明其主要成分仍然是 。
。②下列实验可以使用A进行的是
a.向A中滴入NaOH溶液,制备纯净的
 沉淀
沉淀b.用A处理含有+6价Cr的酸性废水,将剧毒的+6价Cr还原至低毒的+3价
经过上述探究,实验小组对
 溶液的配制与使用有了更深入的理解。
溶液的配制与使用有了更深入的理解。
您最近一年使用:0次
2023-01-07更新
|
365次组卷
|
3卷引用:北京市西城区2022-2023学年高一上学期期末考试化学试题
名校
解题方法
5 . 某小组在验证H2O2氧化Fe2+时发现异常现象,并对其进行深入探究。
实验I:
(1)实验I中溶液变红是因为Fe3+与SCN-发生了反应,其离子方程式是__ 。
(2)探究实验I中红色褪去的原因:取反应后溶液,___ (填实验操作和现象),证明溶液中有Fe3+,而几乎无SCN-。
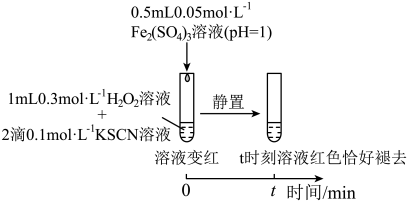
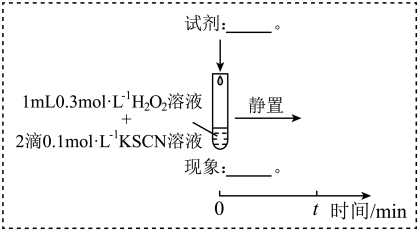
(3)研究发现,酸性溶液中H2O2能氧化SCN-,但反应很慢且无明显现象,而实验I中褪色相对较快,由此推测Fe3+能加快H2O2与SCN-的反应。通过实验II和III得到了证实。参照实验II的图例,在虚线框内补全实验III:__ 。
实验II:
实验III:
(4)查阅资料:Fe3+加快H2O2与SCN-反应的主要机理有
i.Fe3++H2O2=Fe2++HO2·+H+
ii.Fe2++H2O2=Fe3++·OH+OH-
iii.OH(羟基自由基)具有强氧化性,能直接氧化SCN-
为探究Fe2+对H2O2与SCN-反应速率的影响,设计实验如图:
实验IV:

①t′<t,对比实验IV和II可得出结论:在本实验条件下,___ 。
②结合资料和(1)~(4)的研究过程,从反应速率和化学平衡的角度解释实验I中溶液先变红后褪色的原因:____ 。
③实验I~IV中均有O2生成,小组同学推测可能是HO2·与溶液中其他微粒相互作用生成的,这些微粒有___ 。
实验I:
| 装置与操作 | 现象 |
 | 溶液立即变红,继续滴加H2O2溶液,红色变浅并逐渐褪去 |
(2)探究实验I中红色褪去的原因:取反应后溶液,
(3)研究发现,酸性溶液中H2O2能氧化SCN-,但反应很慢且无明显现象,而实验I中褪色相对较快,由此推测Fe3+能加快H2O2与SCN-的反应。通过实验II和III得到了证实。参照实验II的图例,在虚线框内补全实验III:
实验II:

实验III:

(4)查阅资料:Fe3+加快H2O2与SCN-反应的主要机理有
i.Fe3++H2O2=Fe2++HO2·+H+
ii.Fe2++H2O2=Fe3++·OH+OH-
iii.OH(羟基自由基)具有强氧化性,能直接氧化SCN-
为探究Fe2+对H2O2与SCN-反应速率的影响,设计实验如图:
实验IV:

①t′<t,对比实验IV和II可得出结论:在本实验条件下,
②结合资料和(1)~(4)的研究过程,从反应速率和化学平衡的角度解释实验I中溶液先变红后褪色的原因:
③实验I~IV中均有O2生成,小组同学推测可能是HO2·与溶液中其他微粒相互作用生成的,这些微粒有
您最近一年使用:0次
2021-08-13更新
|
638次组卷
|
7卷引用:北京市铁路第二中学2022-2023学年高二上学期期中检测化学试题
6 . 探究Fe3+具有较强的氧化性,用1 mol·L−1 FeCl3溶液与SO2进行实验。
(1)用如图所示装置进行实验(夹持装置略去)。
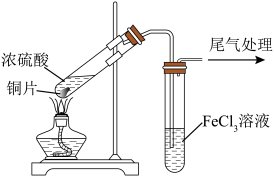
装置A中反应的化学方程式是________ 。
(2)取B中红色溶液,加入铁氰化钾,观察到________ 生成,B中有Fe2+生成。B中发生了2个反应,写出反应2的离子方程式:
反应1:Fe3+ + 6SO2 Fe(SO2)63+(红色); 反应2:
Fe(SO2)63+(红色); 反应2:________ 。
(3)B中溶液颜色由红色变为浅绿色的原因是________ 。
(1)用如图所示装置进行实验(夹持装置略去)。

| 实验操作 | 实验现象 | |
| I | 将装置A加热 | A中铜片上有气泡; B中有气泡,溶液很快变为红色 |
| II | B中继续通入足量气体,溶液仍呈红色。停止通气,静置 | 15 min后,溶液由红色变为黄色; 60 min后,变为浅绿色 |
装置A中反应的化学方程式是
(2)取B中红色溶液,加入铁氰化钾,观察到
反应1:Fe3+ + 6SO2
 Fe(SO2)63+(红色); 反应2:
Fe(SO2)63+(红色); 反应2:(3)B中溶液颜色由红色变为浅绿色的原因是
您最近一年使用:0次
2020-01-19更新
|
117次组卷
|
3卷引用:北京市西城区2019-2020学年度高二上学期期末考试化学试题
2014高三·全国·专题练习
名校
7 . 甲、乙两同学用下图所示装置进行实验,探究硝酸与铁反应的产物。
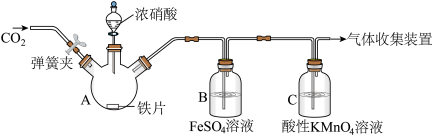
文献记载:I.在浓硝酸和活泼金属反应过程中,随着硝酸浓度的降低,其生成的产物有+4、+2、-3价等氮的化合物.
Ⅱ.FeSO4+NO Fe(NO)SO4(棕色) ΔH<0。
Fe(NO)SO4(棕色) ΔH<0。
Ⅲ.NO2和NO都能被KMnO4氧化吸收。
甲的实验操作和现象记录如下:
请回答下列问题:
(1)滴入浓硝酸加热前没有明显现象的原因是____________________________ 。
(2)检验是否生成-3价氮的化合物,应进行的实验操作是__________ 。
(3)甲取少量B中溶液,加热,实验现象是_________________________ 。请用化学平衡原理解释原因:_________________________ 。甲依据该现象得出的结论是A中有NO生成。
(4)乙认为甲得出A中有NO生成的证据不足。为获取充足的证据,乙仍采用该装置和操作进行对照实验,乙作出的改变是___________________________________ ,证明有NO生成的实验现象是___________________________________ 。
(5)证明A溶液中含有Fe3+,选择的药品是(填序号)________ 。
A.铁粉 B.溴水
C.铁氰化钾溶液 D.硫氰化钾溶液

文献记载:I.在浓硝酸和活泼金属反应过程中,随着硝酸浓度的降低,其生成的产物有+4、+2、-3价等氮的化合物.
Ⅱ.FeSO4+NO
 Fe(NO)SO4(棕色) ΔH<0。
Fe(NO)SO4(棕色) ΔH<0。Ⅲ.NO2和NO都能被KMnO4氧化吸收。
甲的实验操作和现象记录如下:
| 实验操作 | 实验现象 |
| 打开弹簧夹,通入一段时间CO2,关闭弹簧夹。 | |
| 打开分液漏斗活塞,将浓硝酸缓慢滴入烧瓶中,关闭活塞。 | 无明显现象。 |
| 加热烧瓶,反应开始后停止加热。 | ①A中有红棕色气体产生,一段时间后,气体颜色逐变浅;B中溶液变棕色;C中溶液紫色变浅。 ②反应停止后,A中无固体剩余。 |
(1)滴入浓硝酸加热前没有明显现象的原因是
(2)检验是否生成-3价氮的化合物,应进行的实验操作是
(3)甲取少量B中溶液,加热,实验现象是
(4)乙认为甲得出A中有NO生成的证据不足。为获取充足的证据,乙仍采用该装置和操作进行对照实验,乙作出的改变是
(5)证明A溶液中含有Fe3+,选择的药品是(填序号)
A.铁粉 B.溴水
C.铁氰化钾溶液 D.硫氰化钾溶液
您最近一年使用:0次
8 . 某小组在验证反应“Fe+2Ag+=Fe2++2Ag”的实验中检测到Fe3+,发现和探究过程如下。向硝酸酸化的0.05mol·L-1硝酸银溶液(pH≈2)中加入过量铁粉,搅拌后静置,烧杯底部有黑色固体,溶液呈黄色。
(1)检验产物
①取出少量黑色固体,洗涤后,_______ (填操作和现象),证明黑色固体中含有Ag。
②取上层清液,滴加K3Fe(CN)6溶液,产生蓝色沉淀,说明溶液中含有Fe2+。
(2)针对“溶液呈黄色”,甲认为溶液中有Fe3+,乙认为铁粉过量时不可能有Fe3+,乙依据的原理是___________________ (用离子方程式表示)。针对两种观点继续实验:
①取上层清液,滴加KSCN溶液,溶液变红,证实了甲的猜测,同时发现有白色沉淀生成,且溶液颜色深浅、沉淀量多少与取样时间有关,对比实验记录如下:
(资料:Ag+与SCN-生成白色沉淀AgSCN)
②对Fe3+产生的原因作出如下假设:
假设a:可能是铁粉表面有氧化层,能产生Fe3+;
假设b:空气中存在O2,由于________ (用离子方程式表示),可产生Fe3+;
假设c:酸性溶液中NO3-具有氧化性,可产生Fe3+;
假设d:根据_______ 现象,判断溶液中存在Ag+,可产生Fe3+。
③下列实验Ⅰ可证实假设a、b、c不是产生Fe3+的主要原因。实验Ⅱ可证实假设d成立。
实验Ⅰ:向硝酸酸化的________ 溶液(pH≈2)中加入过量铁粉,搅拌后静置,不同时间取上层清液滴加KSCN溶液,3min时溶液呈浅红色,30min后溶液几乎无色。
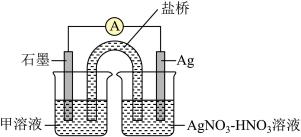
实验Ⅱ:装置如图。其中甲溶液是________ ,操作及现象是________________ 。_______________ 。
(1)检验产物
①取出少量黑色固体,洗涤后,
②取上层清液,滴加K3Fe(CN)6溶液,产生蓝色沉淀,说明溶液中含有Fe2+。
(2)针对“溶液呈黄色”,甲认为溶液中有Fe3+,乙认为铁粉过量时不可能有Fe3+,乙依据的原理是
①取上层清液,滴加KSCN溶液,溶液变红,证实了甲的猜测,同时发现有白色沉淀生成,且溶液颜色深浅、沉淀量多少与取样时间有关,对比实验记录如下:
| 序号 | 取样时间/min | 现象 |
| ⅰ | 3 | 产生大量白色沉淀;溶液呈红色 |
| ⅱ | 30 | 产生白色沉淀;较3min时量少;溶液红色较3min时加深 |
| ⅲ | 120 | 产生白色沉淀;较30min时量少;溶液红色较30min时变浅 |
②对Fe3+产生的原因作出如下假设:
假设a:可能是铁粉表面有氧化层,能产生Fe3+;
假设b:空气中存在O2,由于
假设c:酸性溶液中NO3-具有氧化性,可产生Fe3+;
假设d:根据
③下列实验Ⅰ可证实假设a、b、c不是产生Fe3+的主要原因。实验Ⅱ可证实假设d成立。
实验Ⅰ:向硝酸酸化的
实验Ⅱ:装置如图。其中甲溶液是
您最近一年使用:0次
2017-08-08更新
|
5148次组卷
|
23卷引用:北京市第四十三中学2021-2022学年高三上学期期中考试化学试题
北京市第四十三中学2021-2022学年高三上学期期中考试化学试题2017年全国普通高等学校招生统一考试理综化学(北京卷精编版)贵州省遵义航天高级中学2018届高三第一次模拟考试(9月月考)理科综合化学试题辽宁省实验中学分校2018届高三12月月考理科综合化学试题(已下线)《考前20天终极攻略》-5月27日 综合实验设计、探究和评价(已下线)解密18 物质的制备、实验方案的设计与评价——备战2018年高考化学之高频考点解密(已下线)考点07 元素化合物综合——《备战2020年高考精选考点专项突破题集》湖南长沙长郡中学2020届高三2月份网络教学质量监测卷理综化学试题四川省成都市第七中学2020年高中毕业班教学质量监测卷理科综合化学试题河北省衡水中学2020年高中毕业班教学质量监测卷理科综合化学试题湖南省株洲市2020年高中毕业班教学质量监测卷理科综合化学试题(已下线)专题3.3 铁及其重要化合物(练)——2020年高考化学一轮复习讲练测(已下线)专题16 化学实验综合应用-备战2021届高考化学二轮复习题型专练(已下线)考点32 化学实验方案设计与评价-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点33 物质的定性与定量分析-备战2022年高考化学一轮复习考点帮(浙江专用)陕西省西安市高新第一中学2020届高三教学质量监测理综化学试题天津市西青区杨柳青第一中学2021--2022 学年高三上学期第一次阶段检测化学试题(已下线)考点53 化学实验方案设计与评价-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)题型48 实验原理探究型综合实验北京市中国人民大学附属中学2023-2024学年高三上学期期末考前化学练习 广东省广州市普通高中2024届高三下学期毕业班冲刺训练题(二)化学试题北京市第二十二中学2023-2024学年高一下学期期中考试化学试题北京市丰台区第二中学2024届高三下学期三模化学试题



