名校
解题方法
1 . 下列关于 、
、 性质实验的说法错误的是
性质实验的说法错误的是
 、
、 性质实验的说法错误的是
性质实验的说法错误的是
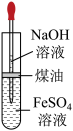
A.用如图装置可以制备 |
B.向某溶液中滴加KSCN溶液,溶液不变色,滴加氯水后溶液显红色,此现象不能确定溶液中含有 |
C.除去 溶液中的 溶液中的 杂质,可以向溶液中加入过量铁粉,然后过滤 杂质,可以向溶液中加入过量铁粉,然后过滤 |
D.向 溶液中加入少量铁粉是为了防止 溶液中加入少量铁粉是为了防止 被氧化 被氧化 |
您最近一年使用:0次
名校
2 . 下列实验操作、现象及实验目的均相符合的是
| 选项 | 实验目的 | 实验操作及现象 |
| A | 验证某溶液中含有Fe3+,不含Fe2+ | 取少量该溶液于试管中,滴加KSCN溶液,混合溶液变血红色 |
| B | 验证某溶液中含有Ba2+ | 用洁净的铂丝蘸取少量该溶液进行焰色反应,观察到火焰成红色 |
| C | 清洗铜与浓硫酸反应后装有剩余溶液的试管 |  |
| D | 验证酸性条件下氧化性:Fe3+< | 将稀硫酸加入盛有Fe(NO3)2溶液的试管中,溶液变为棕黄色,且试管口有红棕色气体生成 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
3 . 下列关于Fe3+、Fe2+性质实验的说法错误的是( )


| A.用如图装置可以制备Fe(OH)2沉淀 |
| B.配制FeCl3溶液时,先将氯化铁晶体溶于较浓的盐酸中,再加水稀释到所需要的浓度 |
| C.向某溶液中滴加KSCN溶液,溶液不变色,滴加氯水后溶液显红色,此现象不能确定溶液中含有Fe2+ |
| D.向FeCl2溶液中加入少量铁粉是为了防止Fe2+被氧化 |
您最近一年使用:0次
2016-12-09更新
|
476次组卷
|
16卷引用:宁夏平罗中学2022-2023学年高三上学期第一次月考化学试题
宁夏平罗中学2022-2023学年高三上学期第一次月考化学试题2015-2016学年河北保定一中高二下期末化学试卷【全国百强校】甘肃省静宁县第一中学2019届高三上学期第一次模拟考试化学试题黑龙江省齐齐哈尔市第八中学2019届高三9月月考化学试题河北省邯郸市大名县第一中学2019-2020学年高二下学期第一次半月考化学试题安徽省滁州市定远县民族中学2020-2021学年高一11月月考化学试题安徽省滁州市定远育才学校2021-2022学年高二上学期开学摸底考试化学试题江西省安福中学2021-2022学年高二上学期开学考试化学(理)试题安徽省滁州市定远县育才学校2021-2022学年高一上学期月考化学试题上海财经大学附属中学2022-2023学年高二上学期期中考试化学试题上海市卢湾高级中学2022-2023学年高三上学期期中考试化学试题上海市卢湾高级中学2022-2023学年高三上学期期中考试化学试题天津市实验中学滨海学校黄南民族班2021-2022学年高三上学期期中质量监测化学试题辽宁省大石桥市第三高级中学2021-2022学年高一12月月考化学试题(已下线)第3讲 铁盐及其亚铁盐陕西省西安市铁一中学2023-2024学年高三上学期9月月考化学试题
4 . 回答下列问题。
(1)实验室常用如图所示装置来制取和观察 在空气中被氧化时颜色的变化。
在空气中被氧化时颜色的变化。
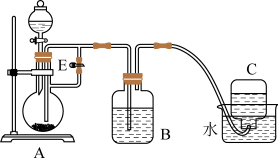
实验时在A中加入铁屑和稀硫酸,B中加入一定量的NaOH溶液,则A中发生的反应的离子方程式是:_________________ 。实验开始时先将活塞E___________ (填“打开”或“关闭”),C中收集到气体的主要成分是__________ 。实验结束后拔去装置B中的橡皮塞,使空气进入,装置B中发生的现象为_________________________ 。
(2)从制造印刷电路板的腐蚀废液(主要含 、
、 、
、 )中回收铜,并重新获得
)中回收铜,并重新获得 溶液,处理流程如图所示:
溶液,处理流程如图所示:
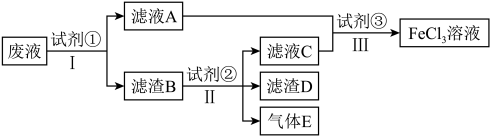
已知试剂①为铁,试剂②为稀盐酸,则滤渣B的成分为___________ ,若试剂③为氯水,则步骤Ⅱ的离子反应方程式为___________ ,检验废液中 存在的最佳试剂是
存在的最佳试剂是___________ (填标号),检验时实验现象为___________ 。
A.氢氧化钠溶液 B.酸性 溶液 C.氯水 D.KSCN溶液
溶液 C.氯水 D.KSCN溶液
(1)实验室常用如图所示装置来制取和观察
 在空气中被氧化时颜色的变化。
在空气中被氧化时颜色的变化。
实验时在A中加入铁屑和稀硫酸,B中加入一定量的NaOH溶液,则A中发生的反应的离子方程式是:
(2)从制造印刷电路板的腐蚀废液(主要含
 、
、 、
、 )中回收铜,并重新获得
)中回收铜,并重新获得 溶液,处理流程如图所示:
溶液,处理流程如图所示:
已知试剂①为铁,试剂②为稀盐酸,则滤渣B的成分为
 存在的最佳试剂是
存在的最佳试剂是A.氢氧化钠溶液 B.酸性
 溶液 C.氯水 D.KSCN溶液
溶液 C.氯水 D.KSCN溶液
您最近一年使用:0次
名校
解题方法
5 . 某化学小组探究酸性条件下NO 、SO
、SO 、Fe3+三种微粒的氧化性强弱,设计如图实验(夹持仪器已略去,装置的气密性已检验)。(忽略氧气对反应的影响)
、Fe3+三种微粒的氧化性强弱,设计如图实验(夹持仪器已略去,装置的气密性已检验)。(忽略氧气对反应的影响)
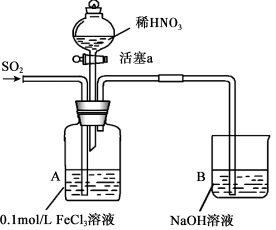
实验记录如表:
请回答下列问题:
(1)指出仪器a的名称_______ 。
(2)写出A装置中通入二氧化硫气体发生反应的离子方程式_______ 。
(3)实验Ⅱ中发生反应的离子方程式是_______ 。
(4)实验Ⅲ中,浅绿色溶液变为黄色的原因是_______ 。(用语言叙述)。
(5)若将实验Ⅳ改为:往A中通入空气,液面上方的现象是_______ 。
(6)综合上述实验得出的结论是:在酸性条件下,氧化性强弱顺序为_______ 。
 、SO
、SO 、Fe3+三种微粒的氧化性强弱,设计如图实验(夹持仪器已略去,装置的气密性已检验)。(忽略氧气对反应的影响)
、Fe3+三种微粒的氧化性强弱,设计如图实验(夹持仪器已略去,装置的气密性已检验)。(忽略氧气对反应的影响)
实验记录如表:
| 选项 | 实验操作 | 实验现象 |
| Ⅰ | 向A装置中通入一段时间SO2气体 | A中溶液最终变为浅绿色 |
| Ⅱ | 取出少量A装置中的溶液,先加入KSCN溶液,再加入BaCl2溶液 | 加入KSCN溶液后溶液不变色,再加入BaCl2溶液产生白色沉淀 |
| Ш | 打开活塞a,将过量HNO3加入装置A中,关闭活塞a | A中浅绿色溶液最终变为黄色 |
| Ⅳ | 取出Ш中少量A装置中的溶液,加入KSCN溶液 | 溶液变为红色 |
(1)指出仪器a的名称
(2)写出A装置中通入二氧化硫气体发生反应的离子方程式
(3)实验Ⅱ中发生反应的离子方程式是
(4)实验Ⅲ中,浅绿色溶液变为黄色的原因是
(5)若将实验Ⅳ改为:往A中通入空气,液面上方的现象是
(6)综合上述实验得出的结论是:在酸性条件下,氧化性强弱顺序为
您最近一年使用:0次
名校
6 . 下列常见实验的现象或表述正确的是
A.向某溶液中加入 滴 滴 溶液,溶液不显红色,再向溶液中加入几滴新制的氯水,溶液变为红色,该溶液中一定含有 溶液,溶液不显红色,再向溶液中加入几滴新制的氯水,溶液变为红色,该溶液中一定含有 |
B.为检验红砖中铁的价态,向红砖粉末中加入盐酸,充分反应后取上层清液于试管中,滴加 溶液 溶液 滴,溶液变为红色,说明红砖中只有三氧化二铁 滴,溶液变为红色,说明红砖中只有三氧化二铁 |
| C.制备氢氧化亚铁时,向硫酸亚铁溶液中滴加氢氧化钠溶液,边加边搅拌,即可制得白色的氢氧化亚铁 |
D. 与过量 与过量 溶液反应生成 溶液反应生成 ,则与过量 ,则与过量 反应也生成 反应也生成 |
您最近一年使用:0次
7 . 完成下列实验的现象和方程式
(1)FeCl2溶液中加入KSCN溶液现象为___________ ,再加入氯水后,现象为___________ ,加入氯水后的离子方程式为___________ 。酸性KMnO4溶液中加入FeSO4溶液现象为___________ ,发生反应的离子方程式为___________ 。
(2)利用如图装置验证苏打和小苏打的热稳定性,小试管中发生反应的化学方程式为___________ 。烧杯中试剂名称为___________ ,A烧杯中的现象为___________ 。
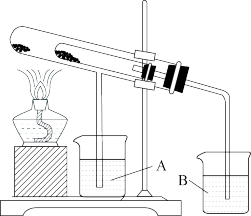
(3)将充满NO2的试管倒置在水中,水进入试管,液面逐渐上升,气体颜色由___________ 色变为 ___________ 色,试管内液面上升至试管容积的___________ 处,该反应的化学方程式为___________ 。
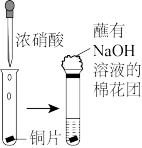
(4)如图向盛有铜片的试管中滴加浓硝酸,产生___________ (填颜色)气体,溶液颜色变为___________ 色,化学方程式为___________ ,该反应中氧化剂和还原剂的物质的量之比为___________ 。已知氢氧化钠溶液吸收二氧化氮的方程式为2NO2+2NaOH=NaNO3+NaNO2+H2O,该反应中氧化产物为___________ ,氧化剂和还原剂的质量比为 ___________ 。
(1)FeCl2溶液中加入KSCN溶液现象为
(2)利用如图装置验证苏打和小苏打的热稳定性,小试管中发生反应的化学方程式为

(3)将充满NO2的试管倒置在水中,水进入试管,液面逐渐上升,气体颜色由
(4)如图向盛有铜片的试管中滴加浓硝酸,产生

您最近一年使用:0次
名校
解题方法
8 . 浓硫酸是一种强氧化性酸,在一定条件下能将多种金属、非金属单质氧化。请回答下列问题:
(1)写出浓硫酸与木炭粉在加热条件下反应的化学方程式___________ 。
(2)试用下表中所列各装置设计一个实验,验证上述反应所产生的各种产物,这种装置的连接顺序是(填编号)___________ →___________ →___________ →___________ 。
注: ④中的加热装置已省略
(3)实验时可观察到装置①中A瓶的溶液褪色,C瓶的溶液不褪色,B瓶中反应的离子方程式是___________ ;C瓶溶液的作用是___________ 。
(4) 装置②中所加固体药品是___________ 。
(5) 装置③中所盛溶液是___________ 。
(6)铁在冷的浓硫酸中能发生钝化。某兴趣小组的同学发现将铁与一定量的浓硫酸加热时,观察到铁完全溶解得到溶液A,并产生大量气体B.(提出猜想)
①所得溶液中的金属离子可能含有Fe2+和Fe3+中的一种或两种。
②所得气体B点可能组成是___________ 。
(实验探究)实验室提供下列试剂和如图2的装置:
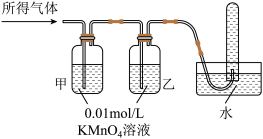
0.01mol/L酸性KMnO4溶液、0.1mol/LKSCN溶液、3%H2O2溶液、淀粉溶液、蒸馏水。在配置0.01mol/L酸性KMnO4溶液过程中,需要用到的仪器是烧杯、玻璃棒、100mL容量瓶和___________ (填仪器名称)。请你完成以下探究实验。
(1)写出浓硫酸与木炭粉在加热条件下反应的化学方程式
(2)试用下表中所列各装置设计一个实验,验证上述反应所产生的各种产物,这种装置的连接顺序是(填编号)
| 编号 | ① | ② | ③ | ④ |
| 装置 | 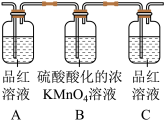 | 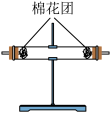 | 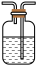 | 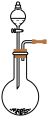 |
(3)实验时可观察到装置①中A瓶的溶液褪色,C瓶的溶液不褪色,B瓶中反应的离子方程式是
(4) 装置②中所加固体药品是
(5) 装置③中所盛溶液是
(6)铁在冷的浓硫酸中能发生钝化。某兴趣小组的同学发现将铁与一定量的浓硫酸加热时,观察到铁完全溶解得到溶液A,并产生大量气体B.(提出猜想)
①所得溶液中的金属离子可能含有Fe2+和Fe3+中的一种或两种。
②所得气体B点可能组成是
(实验探究)实验室提供下列试剂和如图2的装置:

0.01mol/L酸性KMnO4溶液、0.1mol/LKSCN溶液、3%H2O2溶液、淀粉溶液、蒸馏水。在配置0.01mol/L酸性KMnO4溶液过程中,需要用到的仪器是烧杯、玻璃棒、100mL容量瓶和
| 实验操作 | 预期现象 | 结论 | |
| 验证猜想① | 含有Fe2+和Fe3+ | ||
| 验证猜想② | 将所得气体通入如图2所示装置 | 含有两种气体 |
您最近一年使用:0次
名校
解题方法
9 . 对氧化铁与铝粉发生的“铝热反应”(装置如图)的现象有这样的描述:“反应放出大量的热,并发出耀眼的光芒”、“纸漏斗的下部被烧穿,有熔融物落入沙中”。查阅资料得知:Al、A12O3、Fe、Fe2O3熔点数据如表,下列叙述正确的是
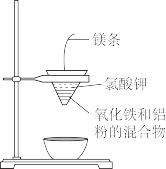

| 物质 | Al | Al2O3 | Fe | Fe2O3 |
| 熔点 /℃ | 660 | 2054 | 1535 | 1462 |
| A.铝热剂特指铝和氧化铁的混合物 |
| B.镁条和KClO3是铝热反应的催化剂 |
| C.该反应所得熔融物熔点低于660℃ |
| D.将少量该反应所得的熔融物溶于足量稀H2SO4,充分反应后,滴加KSCN溶液无明显现象,说明熔融物中无Fe2O3 |
您最近一年使用:0次
2020-08-03更新
|
407次组卷
|
7卷引用:宁夏固原市隆德县中学2021届高三上学期第二次月考化学试题
宁夏固原市隆德县中学2021届高三上学期第二次月考化学试题湖北省2019-2020学年高一下学期期末统一联合测试化学试题黑龙江省牡丹江市第一高级中学2020-2021学年高二上学期8月开学考试化学试题(已下线)3.2.1 金属材料-2020-2021学年高一化学同步课堂帮帮帮(人教版2019必修第一册)河北省张家口市第一中学2020-2021学年高二上学期10月月考(衔接班)化学 试题上海市崇明区民本中学2020-2021学年高二上学期期中考试化学试题(已下线)【教材实验热点】12 铝热反应
10 . 铁及其化合物有丰富多彩的化学性质。回答下列问题:
(1)铁元素在周期表中的位置为第______ 周期_____ 族。
(2)FeCl3溶液可用于吸收尾气中的SO2,写出该反应的离子方程式:_________ 。
(3)某化学兴趣小组同学用如图装置,充分加热硫酸亚铁晶体(FeSO4·xH2O)至完全分解。
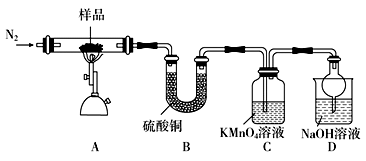
① 装置A中需持续通入N2,其目的是______________________________ 。
② 充分反应一段时间后,小组同学观察到实验现象为:装置A中残留有红棕色固体,装置B中固体变蓝,C中溶液褪色,请写出FeSO4分解的化学方程式:______________ 。
③ 装置D中干燥管的作用为______________ 。
(1)铁元素在周期表中的位置为第
(2)FeCl3溶液可用于吸收尾气中的SO2,写出该反应的离子方程式:
(3)某化学兴趣小组同学用如图装置,充分加热硫酸亚铁晶体(FeSO4·xH2O)至完全分解。

① 装置A中需持续通入N2,其目的是
② 充分反应一段时间后,小组同学观察到实验现象为:装置A中残留有红棕色固体,装置B中固体变蓝,C中溶液褪色,请写出FeSO4分解的化学方程式:
③ 装置D中干燥管的作用为
您最近一年使用:0次



