名校
1 . 下列关于物质的性质与用途的对应关系不正确的是
| A.Na2SO3具有还原性,可用于废水脱氯(Cl2) |
| B.FeCl3有强氧化性,可用于制作印刷线路板 |
| C.K-Na合金导热性好,可用作快中子反应堆热交换剂 |
| D.BaCO3难溶于水,可用于检查肠胃的内服药剂 |
您最近一年使用:0次
解题方法
2 . 化合价和物质类别是整理元素及化合物知识的两个要素,可表示为“价类”二维图。下图是铁元素的“价类”二维图,下列说法正确的是

| A.常温下Fe与水反应生成Fe3O4 |
| B.工业上用CO还原Fe2O3炼铁,该反应属于置换反应 |
| C.维生素C能将Fe3+转化为Fe2+,过程中维生素C做还原剂 |
| D.Fe(OH)2浊液露置于空气中,白色迅速转变为红褐色 |
您最近一年使用:0次
2024-01-10更新
|
110次组卷
|
2卷引用:江苏省启东市东南中学2023-2024学年高一上学期第二次质量检测化学试卷
3 . 下列实验设计及其对应的离子方程式均正确的是
A. 溶液中加入碘化钾淀粉溶液,验证 溶液中加入碘化钾淀粉溶液,验证 氧化性: 氧化性: |
B.把铁片插入 溶液中,验证古代湿法冶铜: 溶液中,验证古代湿法冶铜: |
C.某溶液中滴入 溶液显红色,说明含 溶液显红色,说明含 : :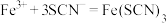 |
D.用 溶液分别与 溶液分别与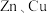 反应,比较 反应,比较 金属活动性顺序: 金属活动性顺序: |
您最近一年使用:0次
名校
4 . 下列离子方程式正确的是
A. 溶于水: 溶于水: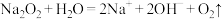 |
B.铜片放入稀硝酸中: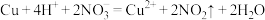 |
C. 溶液可用于刻制印刷铜电路板: 溶液可用于刻制印刷铜电路板: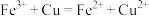 |
D.用二氧化锰制氯气: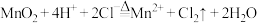 |
您最近一年使用:0次
名校
解题方法
5 . 根据下列实验操作和现象所得到的结论不正确 的是
| 选项 | 实验操作和现象 | 结论 |
| A | 向沸水中滴加少量饱和FeCl3溶液,得到红褐色液体,用激光笔照射可观察到光亮 “通路” “通路” | 所得红褐色液体是胶体 |
| B | 向FeSO4溶液中通入氯气,再滴加几滴KSCN溶液,溶液显红色 | Fe2+被完全氧化为Fe3+ |
| C | 将铂丝用盐酸洗净后,在外焰上灼烧至与原来的火焰颜色相同时,再用铂丝蘸取少量待测溶液进行焰色试验,火焰呈黄色 | 该溶液中含有Na+ |
| D | 向溶液中FeCl3滴加KI溶液,再滴加淀粉溶液,溶液显蓝色 | 氧化性:Fe3+>I2 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
6 . 下列有关物质的性质与用途不具有 对应关系的是
| A.Na的熔点低,可用于高温下与TiCl4反应制备Ti |
| B.NaHCO3能与酸反应,可用作抗胃酸药 |
| C.铁粉具还原性,可用于食品抗氧化 |
| D.FeCl3具有氧化性,可用于蚀刻电路板 |
您最近一年使用:0次
7 . 将H2S和空气的混合气体通入FeCl3、FeCl2、CuCl2的混合溶液中反应回收S,如图所示,下列说法正确的是

| A.在图示的转化中,化合价不变的元素只有铜 |
| B.由图示的转化可得出的氧化性的强弱顺序是:Fe3+>O2>S |
| C.回收S的总反应为2H2S+O2=2S+2H2O |
| D.①②③三步均为氧化还原反应 |
您最近一年使用:0次
2023-12-26更新
|
311次组卷
|
8卷引用:江苏省南宁市第三十三中学2023-2024学年高一下学期3月月考化学试题
江苏省南宁市第三十三中学2023-2024学年高一下学期3月月考化学试题上海市上海中学2023-2024学年高一上学期期中考试化学试题河北省石家庄市第二十三中学2023-2024学年高一下学期第一次月考(3月)化学试题(已下线)期中测试卷一【测试范围:第五、六章】-2023-2024学年高一化学下学期期中考点大串讲(人教版2019必修第二册)河南省新乡市原阳县实验高级中学2023-2024学年高一下学期3月月考化学试题黑龙江省大庆市大庆中学2023-2024学年高一下学期4月月考化学试题重庆市璧山来凤中学校2023-2024学年高一下学期3月月考化学试题名校期中好题汇编-非金属元素(选择题)
解题方法
8 . 下列图示基本实验操作正确的是
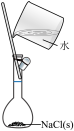 | 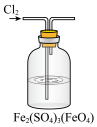 |  |  |
A.配制一定物质的量浓度的 溶液 溶液 | B.提纯 | C.验证Na与水反应是否为放热反应 | D.蒸干 溶液获得 溶液获得 晶体 晶体 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
9 . 下列操作中,不会影响溶液中 、
、 、
、 、
、 、
、 等离子大量共存的是
等离子大量共存的是
 、
、 、
、 、
、 、
、 等离子大量共存的是
等离子大量共存的是A.通入 气体 气体 | B.加入硝酸银溶液 | C.加入硫氰化钾溶液 | D.加入硫酸溶液 |
您最近一年使用:0次
名校
解题方法
10 . 小组同学用FeSO4∙7H2O晶体和蒸馏水配制100 mL0.5mol∙L-1 FeSO4溶液(pH为3.3),再进行性质探究实验。
Ⅰ.配制溶液
(1)用到的仪器有:天平、药匙、量筒、烧杯、玻璃棒、___________ 。
(2)计算需要FeSO4∙7H2O晶体的质量是___________ g。
(3)下列情况中,会使所配溶液浓度偏低的是___________ (填字母)。
a.转移时,容量瓶没有干燥 b.转移时,未洗涤烧杯和玻璃棒
c.定容时,眼睛俯视刻度线 d.定容时,发现液面高于刻度线,将多余溶液吸出
Ⅱ.性质探究
立即取出一定量配制好的溶液放入2个试管中,分别进行如下实验:
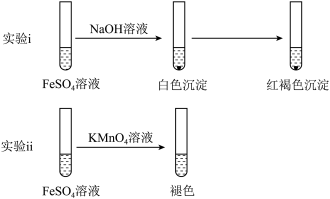
(4)写出实验ⅰ中白色沉淀转化为红褐色沉淀的化学方程式并标明电子转移的方向和数目___________ 。
(5)实验ⅱ中高锰酸钾溶液褪色,说明FeSO4溶液具有___________ 性。
Ⅲ.异常探究
配制好的溶液放置1 h后溶液变黄。24 h后产生黄褐色沉淀,测得上层清液pH为1.4。
(6)取少量黄色溶液,___________ (填操作和现象),证明黄色溶液中含有Fe3+。分析推理,溶液变黄的原因是___________ 。
(7)实验证实黄褐色沉淀为Fe(OH)SO4。
①某学生为验证黄褐色沉淀中的 ,设计了以下实验方案:取过滤后的沉淀少许于试管,加入稍过量的稀盐酸将其溶解,再加入BaCl2溶液,观察是否有沉淀生成。请判断上述实验方案是否合理,若不合理请说明理由:
,设计了以下实验方案:取过滤后的沉淀少许于试管,加入稍过量的稀盐酸将其溶解,再加入BaCl2溶液,观察是否有沉淀生成。请判断上述实验方案是否合理,若不合理请说明理由:___________ 。
②写出Fe3+转化为Fe(OH)SO4反应的离子方程式为___________ 。
Ⅰ.配制溶液
(1)用到的仪器有:天平、药匙、量筒、烧杯、玻璃棒、
(2)计算需要FeSO4∙7H2O晶体的质量是
(3)下列情况中,会使所配溶液浓度偏低的是
a.转移时,容量瓶没有干燥 b.转移时,未洗涤烧杯和玻璃棒
c.定容时,眼睛俯视刻度线 d.定容时,发现液面高于刻度线,将多余溶液吸出
Ⅱ.性质探究
立即取出一定量配制好的溶液放入2个试管中,分别进行如下实验:

(4)写出实验ⅰ中白色沉淀转化为红褐色沉淀的化学方程式并标明电子转移的方向和数目
(5)实验ⅱ中高锰酸钾溶液褪色,说明FeSO4溶液具有
Ⅲ.异常探究
配制好的溶液放置1 h后溶液变黄。24 h后产生黄褐色沉淀,测得上层清液pH为1.4。
(6)取少量黄色溶液,
(7)实验证实黄褐色沉淀为Fe(OH)SO4。
①某学生为验证黄褐色沉淀中的
 ,设计了以下实验方案:取过滤后的沉淀少许于试管,加入稍过量的稀盐酸将其溶解,再加入BaCl2溶液,观察是否有沉淀生成。请判断上述实验方案是否合理,若不合理请说明理由:
,设计了以下实验方案:取过滤后的沉淀少许于试管,加入稍过量的稀盐酸将其溶解,再加入BaCl2溶液,观察是否有沉淀生成。请判断上述实验方案是否合理,若不合理请说明理由:②写出Fe3+转化为Fe(OH)SO4反应的离子方程式为
您最近一年使用:0次



