1 . 铁酸锌(ZnFe2O4)是可见光的敏感半导体材料,也可以用作脱硫剂,难溶于水和稀硫酸,以锌灰(含ZnO及少量PbO、CuO、Fe2O3、SiO2)和Fe2(SO4)3为原料制备的ZnFe2O4的过程可以表示为下图:

已知:锌和铝都是活泼金属,它们的单质及化合物的性质具有一定的相似性
(1)请写出ZnO与氢氧化钠溶液反应的化学反应方程式:___________ 。
(2)下列说法正确的是___________。
(3)浸取过程中为了提高锌灰的浸取效果,还可以采取哪些方法(写出两种)___________ 。
(4)700℃时ZnFe2O4会分解,设计实验验证ZnFe2O4中含有Fe元素:___________ 。
(5)400℃时,装有脱硫剂的硫化反应器中,ZnFe2O4与H2、H2S反应生硫化物,其化学方程式为___________ 。

已知:锌和铝都是活泼金属,它们的单质及化合物的性质具有一定的相似性
(1)请写出ZnO与氢氧化钠溶液反应的化学反应方程式:
(2)下列说法正确的是___________。
| A.杂质中的SiO2属于酸性氧化物,能与Fe2O3反应 |
| B.除杂过程包括加足量锌粉、双氧水氧化等步骤,除Pb2+和Cu2+外,与锌粉反应的离子还有Fe3+和H+ |
| C.碳酸氢钠是为了调节溶液的pH,也可以用弱碱NH3·H2O代替 |
| D.ZnFe2O4难溶于稀硫酸,但在SO2-H2SO4体系中溶解度会明显增大 |
(3)浸取过程中为了提高锌灰的浸取效果,还可以采取哪些方法(写出两种)
(4)700℃时ZnFe2O4会分解,设计实验验证ZnFe2O4中含有Fe元素:
(5)400℃时,装有脱硫剂的硫化反应器中,ZnFe2O4与H2、H2S反应生硫化物,其化学方程式为
您最近一年使用:0次
2 . 绿色化学在推动社会可持续发展中发挥着重要作用。某科研团队设计了一种熔盐液相氧化法制备高价铬盐的新工艺,该工艺不消耗除铬铁矿、氢氧化钠和空气以外的其他原料,不产生废弃物,实现了 的深度利用和
的深度利用和 内循环。工艺流程如图:
内循环。工艺流程如图:
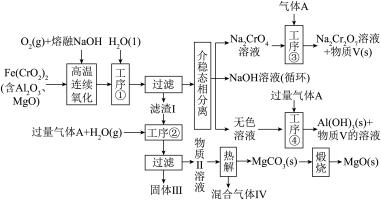
回答下列问题:
(1) 中Cr元素的化合价为+3价,写出高温连续氧化工序中该物质发生反应的化学方程式:
中Cr元素的化合价为+3价,写出高温连续氧化工序中该物质发生反应的化学方程式:_________ 。
(2)滤渣Ⅰ的主要成分是_________ (填化学式)。工序③中发生反应的离子方程式为_________ 。
(3)热解工序产生的混合气体Ⅳ最适宜返回工序_________ (填“①”或“②”或“③”或“④”)参与内循环。
(4) 难溶于水,常温时
难溶于水,常温时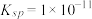 ;
; 难溶于水,能溶于强酸、强碱。
难溶于水,能溶于强酸、强碱。
①欲使 的
的 溶液中的
溶液中的 沉淀完全(离子浓度小于
沉淀完全(离子浓度小于 ),需加入等体积浓度至少为
),需加入等体积浓度至少为_________  的
的 溶液。
溶液。
②20℃时,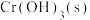 在不同浓度的NaOH溶液中的最大溶解量(
在不同浓度的NaOH溶液中的最大溶解量( )如图1所示。下列叙述正确
)如图1所示。下列叙述正确_________ 的是(填字母)。
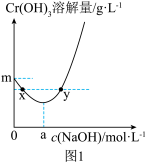
A.NaOH浓度越小,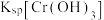 越小
越小
B.x、y两点对应的溶液中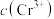 不相等
不相等
C.当NaOH浓度小于 时,随着NaOH浓度的增大,
时,随着NaOH浓度的增大, 溶解量减小是因为
溶解量减小是因为 浓度增大使
浓度增大使 溶解平衡逆向移动
溶解平衡逆向移动
D.当NaOH浓度为 时,溶液中
时,溶液中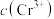 一定最小
一定最小
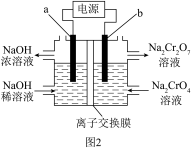
(5)工序③也可以利用电解法制 ,工作原理如下图2所示(a、b电极均为石墨)。该装置中的离子交换膜为
,工作原理如下图2所示(a、b电极均为石墨)。该装置中的离子交换膜为_________ (填离子符号)交换膜。制备 时,若电路中有4mol电子转移时,理论上右侧溶液总质量减少
时,若电路中有4mol电子转移时,理论上右侧溶液总质量减少_________ g。
 的深度利用和
的深度利用和 内循环。工艺流程如图:
内循环。工艺流程如图:
回答下列问题:
(1)
 中Cr元素的化合价为+3价,写出高温连续氧化工序中该物质发生反应的化学方程式:
中Cr元素的化合价为+3价,写出高温连续氧化工序中该物质发生反应的化学方程式:(2)滤渣Ⅰ的主要成分是
(3)热解工序产生的混合气体Ⅳ最适宜返回工序
(4)
 难溶于水,常温时
难溶于水,常温时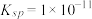 ;
; 难溶于水,能溶于强酸、强碱。
难溶于水,能溶于强酸、强碱。①欲使
 的
的 溶液中的
溶液中的 沉淀完全(离子浓度小于
沉淀完全(离子浓度小于 ),需加入等体积浓度至少为
),需加入等体积浓度至少为 的
的 溶液。
溶液。②20℃时,
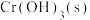 在不同浓度的NaOH溶液中的最大溶解量(
在不同浓度的NaOH溶液中的最大溶解量( )如图1所示。下列叙述正确
)如图1所示。下列叙述正确
A.NaOH浓度越小,
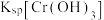 越小
越小B.x、y两点对应的溶液中
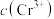 不相等
不相等C.当NaOH浓度小于
 时,随着NaOH浓度的增大,
时,随着NaOH浓度的增大, 溶解量减小是因为
溶解量减小是因为 浓度增大使
浓度增大使 溶解平衡逆向移动
溶解平衡逆向移动D.当NaOH浓度为
 时,溶液中
时,溶液中 一定最小
一定最小(5)工序③也可以利用电解法制
 ,工作原理如下图2所示(a、b电极均为石墨)。该装置中的离子交换膜为
,工作原理如下图2所示(a、b电极均为石墨)。该装置中的离子交换膜为 时,若电路中有4mol电子转移时,理论上右侧溶液总质量减少
时,若电路中有4mol电子转移时,理论上右侧溶液总质量减少
您最近一年使用:0次
2022-11-30更新
|
987次组卷
|
5卷引用:辽宁省部分省级示范性高中2022-2023学年高二下学期3月测试化学试题
辽宁省部分省级示范性高中2022-2023学年高二下学期3月测试化学试题江西省临川第一中学2022-2023学年高三上学期11月教学质量检测化学试题 (已下线)河南省湘豫名校联考2022-2023学年高三上学期12月期末摸底考试变式汇编(17-21)江西省宁冈中学2022-2023学年高三上学期12月月考化学试题江西省吉安市第三中学2022-2023学年高三上学期12月月考化学试题
名校
解题方法
3 . 已知FeCl3溶液与KI溶液的反应为可逆反应,某小组同学对该反应进行实验探究。
(1)甲同学首先进行了实验1
①写出FeCl3溶液与KI溶液反应的离子方程式_____ 。
②加入KSCN溶液的目的是_____ 。
③甲同学认为溶液不显红色的原因是反应体系中c(Fe3+)太低,故改进实验方案,进行了实验2。
本实验改用0.1 mol•L-1 KI溶液的目的是______ 。
用化学平衡原理解释实验2中加入CCl4后上层溶液红色消失的原因:______ 。
(2)甲同学认为“用CCl4萃取后上层溶液仍为棕黄色”的原因是I2未被充分萃取,但乙同学查阅资料得到信息:I2、I 在水中均呈棕黄色,两者有如下关系:I2+I-⇌I
在水中均呈棕黄色,两者有如下关系:I2+I-⇌I 。于是提出假设:萃取后的溶液呈棕黄色的主要原因是存在I
。于是提出假设:萃取后的溶液呈棕黄色的主要原因是存在I 。
。
①为验证假设,乙同学设计并完成了实验3。
实验3的结论是_____ 。
②甲同学依据乙同学的实验设计思路,选用实验2中的试剂,运用控制变量的方法设计了更加严谨的实验,证明了平衡I2+I-⇌I 的存在。请你补充完整他设计的实验步骤:将实验2中下层紫红色溶液平均分成两份,分装于两支试管中,向试管1中加入1 mL水,振荡、静置;向试管2中
的存在。请你补充完整他设计的实验步骤:将实验2中下层紫红色溶液平均分成两份,分装于两支试管中,向试管1中加入1 mL水,振荡、静置;向试管2中____ ,振荡、静置,对比观察现象。
(1)甲同学首先进行了实验1
| 实验1 | 实验步骤 | 实验现象 |
| ⅰ.取2 mL 1 mol•L-1 KI溶液,滴加0.1 mol•L-1 FeCl3溶液3滴(1滴约为0.05 mL,下同) | ⅰ.溶液呈棕黄色. | |
| ⅱ.向其中滴加2滴0.1 mol•L-1 KSCN溶液. | ⅱ.溶液不显红色. |
②加入KSCN溶液的目的是
③甲同学认为溶液不显红色的原因是反应体系中c(Fe3+)太低,故改进实验方案,进行了实验2。
| 实验2 | 实验步骤 | 实验现象 |
| ⅰ.取2 mL 0.1 mol•L-1 KI溶液,滴加0.1 mol•L-1 FeCl3溶液3滴。 | ⅰ.溶液呈棕黄色。 | |
| ⅱ.向其中滴加2滴0.1 mol•L-1 KSCN溶液。 | ⅱ.溶液显红色。 | |
| ⅲ.继续加入2 mL CCl4,充分振荡、静置。 | ⅲ.液体分层,上层红色消失,变为棕黄色,下层呈紫红色。 |
用化学平衡原理解释实验2中加入CCl4后上层溶液红色消失的原因:
(2)甲同学认为“用CCl4萃取后上层溶液仍为棕黄色”的原因是I2未被充分萃取,但乙同学查阅资料得到信息:I2、I
 在水中均呈棕黄色,两者有如下关系:I2+I-⇌I
在水中均呈棕黄色,两者有如下关系:I2+I-⇌I 。于是提出假设:萃取后的溶液呈棕黄色的主要原因是存在I
。于是提出假设:萃取后的溶液呈棕黄色的主要原因是存在I 。
。①为验证假设,乙同学设计并完成了实验3。
| 实验3 | 实验步骤 | 实验现象 |
| ⅰ.取1 mL实验2中棕黄色的上层清液,再加入2 mL CCl4,振荡、静置。 | ⅰ.液体分层,上层呈黄色,下层呈紫红色。 | |
| ⅱ.取1 mL饱和碘水,加入2 mL CCl4,振荡静置。 | ⅱ.液体分层,上层为无色,下层呈紫红色。 |
②甲同学依据乙同学的实验设计思路,选用实验2中的试剂,运用控制变量的方法设计了更加严谨的实验,证明了平衡I2+I-⇌I
 的存在。请你补充完整他设计的实验步骤:将实验2中下层紫红色溶液平均分成两份,分装于两支试管中,向试管1中加入1 mL水,振荡、静置;向试管2中
的存在。请你补充完整他设计的实验步骤:将实验2中下层紫红色溶液平均分成两份,分装于两支试管中,向试管1中加入1 mL水,振荡、静置;向试管2中
您最近一年使用:0次
2020-12-23更新
|
1075次组卷
|
2卷引用:广东实验中学2020-2021学年高二上学期期中考试化学试题
4 . 某班同学用如下实验探究Fe2+、Fe3+的性质。回答下列问题:
(1)分别取一定量氯化铁、氯化亚铁固体,均配制成0.1mol/L的溶液.在FeCl2液中需加入少量铁屑,其目的是________ 。
(2)甲组同学取2mlFeCl2溶液.加入几滴氯水,再加入1滴KSCN溶液,溶液变红,说明Cl2可将Fe2+氧化。FeCl2溶液与氯水反应的离子方程式为_______ 。
(3)乙组同学认为甲组的实验不够严谨,该组同学在2mLFeCl2溶液中先加入0.5ml煤油,再于液面下依次加入几滴氯水和l滴KSCN溶液,溶液变红,煤油的作用是______ 。
(4)丙组同学取10 mL0.1mol/LKI溶液,加入6mL0.1mol/LFeCl3溶液混合。分别取2mL此溶液于3 支试管中进行如下实验:
① 第一支试管中加入1mLCCl4充分振荡、静置,CCl4层呈紫色;
② 第二支试管中加入1滴K3[Fe(CN)6] 溶液,生成蓝色沉淀:
③ 第三支试管中加入1滴KSCN溶液,溶液变红。
实验②检验的离子是_____ (填离子符号);实验①和③说明:在I-过量的情况下,溶液中仍含有______ (填离子符号),由此可以证明该氧化还原反应为______ 。
(5)丁组同学向盛有H2O2溶液的试管中加入几滴酸化的FeCl2溶液,溶液·变成棕黄色,发生反应的离子方程式为________ ;一段时间后.溶液中有气泡出现,并放热.随后有红褐色沉淀生成。产生气泡的原因是______ ;生成沉淀的原因是______ (用平衡移动原理解释)。
(1)分别取一定量氯化铁、氯化亚铁固体,均配制成0.1mol/L的溶液.在FeCl2液中需加入少量铁屑,其目的是
(2)甲组同学取2mlFeCl2溶液.加入几滴氯水,再加入1滴KSCN溶液,溶液变红,说明Cl2可将Fe2+氧化。FeCl2溶液与氯水反应的离子方程式为
(3)乙组同学认为甲组的实验不够严谨,该组同学在2mLFeCl2溶液中先加入0.5ml煤油,再于液面下依次加入几滴氯水和l滴KSCN溶液,溶液变红,煤油的作用是
(4)丙组同学取10 mL0.1mol/LKI溶液,加入6mL0.1mol/LFeCl3溶液混合。分别取2mL此溶液于3 支试管中进行如下实验:
① 第一支试管中加入1mLCCl4充分振荡、静置,CCl4层呈紫色;
② 第二支试管中加入1滴K3[Fe(CN)6] 溶液,生成蓝色沉淀:
③ 第三支试管中加入1滴KSCN溶液,溶液变红。
实验②检验的离子是
(5)丁组同学向盛有H2O2溶液的试管中加入几滴酸化的FeCl2溶液,溶液·变成棕黄色,发生反应的离子方程式为
您最近一年使用:0次
2019-01-30更新
|
5604次组卷
|
40卷引用:2016-2017学年广东省清远三中高二上第二次月考化学卷
2016-2017学年广东省清远三中高二上第二次月考化学卷【校级联考】福建省龙岩市非一级达标校2018-2019学年高二上学期期末教学质量检查化学试题广东省韶关市2019-2020学年高二下学期期末考试化学试题2016年全国普通高等学校招生统一考试化学(新课标2卷精编版)2017届湖北省应城一中高三上学期调研测试化学试卷2017届四川省双流中学高三上学期10月月考化学试卷2017届广西桂林十八中高三上10月月考化学试卷2017届海南省海南中学高三上学期月考三化学试卷2017届四川省泸州市泸化中学高三上10月月考化学卷2016-2017学年北京五十六中九高三上学期期中考试化学试卷天津市南开区2017届高三高考二模化学试卷黑龙江省大庆实验中学2018届高三上学期第一次月考理科综合化学试题内蒙古巴彦淖尔市第一中学2018届高三上学期期中考试理科综合化学试题甘肃省会宁县第一中学2018届高三上学期第三次月考理科综合化学试题青海省西宁二十一中2018届高三上学期12月月考化学试卷黑龙江省哈尔滨市第九中学2017-2018学年高一上学期期末考试化学试题(已下线)解密05 金属及其化合物(教师版)——备战2018年高考化学之高频考点解密【校级联考】安徽省江南片2019届高三上学期入学摸底考试化学试题陕西安康市紫阳县紫阳中学2019届高三上学期入学调研考试化学试题福建省泉州第五中学2019届高三入学调研考试化学试题2016年全国普通高等学校招生统一考试化学(全国2卷参考版)内蒙古包头稀土高新区二中2020届高三10月月考理综化学试题吉林省长春市东北师大附中2020届高中毕业班三月份网络教学质量监测卷理科综合化学部分(已下线)专题3.3 铁及其重要化合物(讲)——2020年高考化学一轮复习讲练测(已下线)第11讲 铁及其重要化合物(精讲)——2021年高考化学一轮复习讲练测黑龙江省牡丹江市第一高级中学2021届高三上学期开学考试化学试题(已下线)专题讲座(三)“铁三角”综合实验题解题策略(精练)——2021年高考化学一轮复习讲练测(已下线)专题讲座(九) 热点实验综合探究 (精练)-2021年高考化学一轮复习讲练测(已下线)解密06 金属及其化合物(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(浙江专版)(已下线)解密06 金属及其化合物(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(已下线)考点15 铁及其化合物-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点15 铁及其化合物-备战2022年高考化学一轮复习考点帮(浙江专用)四川省邻水实验学校2022届高三上学期入学考试理综化学试题(已下线)解密06 金属及其化合物(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)(已下线)解密06 金属及其化合物(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(浙江专用)(已下线)【教材实验热点】04 Fe(OH)2与Fe(OH)3胶体的制备(已下线)考点14 铁及其化合物-备战2023年高考化学一轮复习考点帮(全国通用)第三章 金属及其化合物 第13讲 铁及其重要化合物(已下线)题型31 Fe2+、Fe3+的检验与性质探究(已下线)第一部分 化学综合实验 热点6 物质性质探究实验
名校
解题方法
5 . 为研究铁盐与亚硫酸盐之间的反应,某研究小组利用孔穴板进行了实验探究:
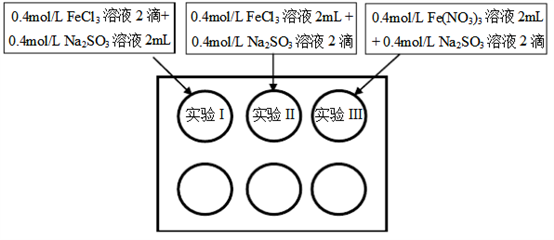
小组记录的实验现象如下表所示:
(1)测得实验所用0.4mol/L FeCl3溶液及Fe(NO3)3溶液pH均约为1.0。两溶液均呈酸性的原因是__________ (用离子方程式表示)。
(2)开始混合时,实验I中红褐色比II、III中略浅的原因是___________ 。
(3)为了探究5min后实验II、III中溶液红褐色变浅的原因,小组同学设计了实验IV:分别取少量5min后实验I、II、III中溶液,加入2滴铁氰化钾溶液,发现实验II、III中出现蓝色沉淀,实验I中无明显变化。根据实验IV的现象,结合化学用语解释红褐色变浅的原因是___________ 。
(4)针对5min后实验III中溶液颜色比实验II中深,小组同学认为可能存在三种因素:
①Cl- 可以加快Fe3+与SO32-的氧化还原反应;
②___________ ;
③NO3- 在酸性环境下代替Fe3+氧化了SO32-,同时消耗H+,使Fe3+水解出的Fe(OH)3较多。
通过实验V和实验VI进行因素探究:
实验结论:因素①和因素②均成立,因素③不明显。请将上述方案填写完整。
(5)通过上述实验,以下结果或推论合理的是___________ (填字母)。
a.Fe3+与SO32-同时发生水解反应和氧化还原反应,且水解反应的速率快,等待足够长时间后,将以氧化还原反应为主
b.浓度为1.2 mol/L的稀硝酸在5min内不能将Fe2+氧化
c.向pH大于1的稀硝酸中加入少量Ba(NO3)2,使其完全溶解,可用来检验实验I的上层清液中是否存在SO42-

小组记录的实验现象如下表所示:
| 开始时 | 5min后 | 3天后 | |
| 实验I | 溶液立即变为红褐色,比II、III中略浅 | 与开始混合时一致 | 溶液呈黄色,底部出现红褐色沉淀 |
| 实验II | 溶液立即变为红褐色 | 红褐色明显变浅 | 溶液呈黄绿色 |
| 实验III | 溶液立即变为红褐色 | 红褐色变浅,比II中深 | 溶液呈黄色 |
(1)测得实验所用0.4mol/L FeCl3溶液及Fe(NO3)3溶液pH均约为1.0。两溶液均呈酸性的原因是
(2)开始混合时,实验I中红褐色比II、III中略浅的原因是
(3)为了探究5min后实验II、III中溶液红褐色变浅的原因,小组同学设计了实验IV:分别取少量5min后实验I、II、III中溶液,加入2滴铁氰化钾溶液,发现实验II、III中出现蓝色沉淀,实验I中无明显变化。根据实验IV的现象,结合化学用语解释红褐色变浅的原因是
(4)针对5min后实验III中溶液颜色比实验II中深,小组同学认为可能存在三种因素:
①Cl- 可以加快Fe3+与SO32-的氧化还原反应;
②
③NO3- 在酸性环境下代替Fe3+氧化了SO32-,同时消耗H+,使Fe3+水解出的Fe(OH)3较多。
通过实验V和实验VI进行因素探究:
| 实验操作(已知Na+对实验无影响) | 5min后的现象 | |
| 实验V | 在2mL pH=1.0的0.4mol/L Fe(NO3)3溶液中溶解约 | 溶液的红褐色介于II、III之间 |
| 实验VI | 在2mL pH=1.0的稀硝酸中溶解约0.19g NaNO3固体,再加入2滴0.4mol/L Na2SO3溶液。向其中滴入少量BaCl2溶液 |
实验结论:因素①和因素②均成立,因素③不明显。请将上述方案填写完整。
(5)通过上述实验,以下结果或推论合理的是
a.Fe3+与SO32-同时发生水解反应和氧化还原反应,且水解反应的速率快,等待足够长时间后,将以氧化还原反应为主
b.浓度为1.2 mol/L的稀硝酸在5min内不能将Fe2+氧化
c.向pH大于1的稀硝酸中加入少量Ba(NO3)2,使其完全溶解,可用来检验实验I的上层清液中是否存在SO42-
您最近一年使用:0次
2018-05-16更新
|
1098次组卷
|
3卷引用:首都师范大学附属中学2022-2023高二上学期期中练习化学试题
名校
6 . 某品牌糖衣片补血剂,除去糖衣后显淡蓝绿色,主要成分是硫酸亚铁,不含其它铁的化合物。某研究性学习小组为测定该补血剂中硫酸亚铁的含量进行了以下探究:
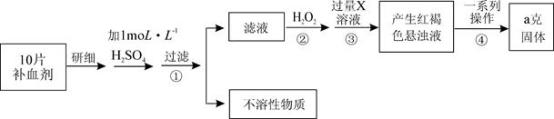
请回答下列问题:
Ⅰ.(1)实验时用10mol·L-1的浓硫酸配制100 mL 1 mol·L-1 H2SO4溶液,所需浓硫酸的体积为_____ mL。
(2)容量瓶所具备的功能是___________________ (填序号)。
A.配制一定体积准确浓度的溶液
B.长期贮存溶液
C.常用来代替量筒量取一定体积的液体
D.用来溶解固体溶质
(3)在下列配制过程示意图中,错误的有(填序号)__________________ 。
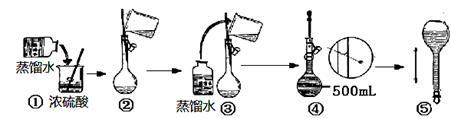
(4)下列说法正确的是_________________ 。
A.洗涤烧杯2~3次,并将洗涤液移入容量瓶以减少误差
B.某同学将浓硫酸稀释后未冷却至室温便将溶液转移至容量瓶,所配溶液浓度会偏低
C.定容时仰视观察, 所配溶液浓度会偏低
Ⅱ.(1)步骤③中产生的红褐色物质是(填化学式)_____________ 。
(2)从红褐色的悬浊液到最后的称量,其过程中所需的基本操作为:
a.________ , b.洗涤, c.灼烧, d.冷却
(3)若称得固体的质量为ag,则每片补血剂中含硫酸亚铁的质量为_______ g。

请回答下列问题:
Ⅰ.(1)实验时用10mol·L-1的浓硫酸配制100 mL 1 mol·L-1 H2SO4溶液,所需浓硫酸的体积为
(2)容量瓶所具备的功能是
A.配制一定体积准确浓度的溶液
B.长期贮存溶液
C.常用来代替量筒量取一定体积的液体
D.用来溶解固体溶质
(3)在下列配制过程示意图中,错误的有(填序号)

(4)下列说法正确的是
A.洗涤烧杯2~3次,并将洗涤液移入容量瓶以减少误差
B.某同学将浓硫酸稀释后未冷却至室温便将溶液转移至容量瓶,所配溶液浓度会偏低
C.定容时仰视观察, 所配溶液浓度会偏低
Ⅱ.(1)步骤③中产生的红褐色物质是(填化学式)
(2)从红褐色的悬浊液到最后的称量,其过程中所需的基本操作为:
a.
(3)若称得固体的质量为ag,则每片补血剂中含硫酸亚铁的质量为
您最近一年使用:0次
2019-01-30更新
|
744次组卷
|
2卷引用:黑龙江省牡丹江市海林林业局第一中学2019-2020学年高二下学期第一次月考化学试题
名校
7 . 三氯化铁是合成草酸铁的重要原料。
(1)利用工业FeCl3制取纯净的草酸铁晶体[Fe2(C2O4)3·5H2O]的实验流程如下图所示:
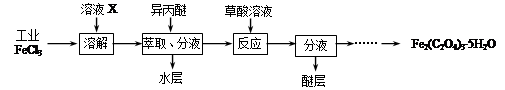
①为抑制FeCl3水解,溶液X为____________ 。
②上述流程中FeCl3能被异丙醚萃取,其原因是_________ ;检验萃取、分液后所得水层中是否含有Fe3+的方法是______________ 。
③所得Fe2(C2O4)3·5H2O需用冰水洗涤,其目的是__________________ 。
④为测定所得草酸铁晶体的纯度,实验室称取a g样品,加硫酸酸化,用KMnO4标准溶液滴定生成的H2C2O4,KMnO4标准溶液应置于如图所示仪器________________ (填“甲”或“乙”)中。下列情况会造成实验测得Fe2(C2O4)3·5H2O含量偏低的是________________ 。

a.盛放KMnO4的滴定管水洗后未用标准液润洗
b.滴定管滴定前尖嘴部分有气泡,滴定后消失
c.滴定前仰视读数,滴定后俯视读数
(2)某研究性学习小组欲从蚀刻镀铜电路板所得废液(溶质为FeCl2、CuCl2、FeCl3)出发,制备单质铜和无水FeCl3,再由FeCl3合成Fe2(C2O4)3·5H2O。请补充完整由蚀刻废液制备单质铜和无水FeCl3的实验步骤(可选用的试剂:铁粉、盐酸、NaOH溶液和H2O2溶液):向废液中加入足量铁粉,充分反应后过滤;__________ ;___________ ;调节溶液pH,将溶液蒸发浓缩、冷却结晶、过滤、洗涤干燥得FeCl3·6H2O;________________ ,得到无水FeCl3。
(1)利用工业FeCl3制取纯净的草酸铁晶体[Fe2(C2O4)3·5H2O]的实验流程如下图所示:

①为抑制FeCl3水解,溶液X为
②上述流程中FeCl3能被异丙醚萃取,其原因是
③所得Fe2(C2O4)3·5H2O需用冰水洗涤,其目的是
④为测定所得草酸铁晶体的纯度,实验室称取a g样品,加硫酸酸化,用KMnO4标准溶液滴定生成的H2C2O4,KMnO4标准溶液应置于如图所示仪器

a.盛放KMnO4的滴定管水洗后未用标准液润洗
b.滴定管滴定前尖嘴部分有气泡,滴定后消失
c.滴定前仰视读数,滴定后俯视读数
(2)某研究性学习小组欲从蚀刻镀铜电路板所得废液(溶质为FeCl2、CuCl2、FeCl3)出发,制备单质铜和无水FeCl3,再由FeCl3合成Fe2(C2O4)3·5H2O。请补充完整由蚀刻废液制备单质铜和无水FeCl3的实验步骤(可选用的试剂:铁粉、盐酸、NaOH溶液和H2O2溶液):向废液中加入足量铁粉,充分反应后过滤;
您最近一年使用:0次
2016-12-09更新
|
712次组卷
|
4卷引用:福建省福州一中2019-2020学年高二下学期第一次月考化学试题
福建省福州一中2019-2020学年高二下学期第一次月考化学试题(已下线)2014届江苏省南通市高三第二次调研化学试卷2016届江苏省泰州中学高三上学期第二次质检化学试卷2017届江苏省南通市高三高考全真模拟(二)化学试卷



