名校
解题方法
1 . 铁是人类较早使用的金属之一。运用铁及其化合物的知识,完成下列问题。
(1)向沸水中逐滴滴加lmol/LFeCl3溶液﹐至液体呈透明的红褐色,该分散系中粒子直径的范围是_______ nm。
(2)在实验室中,FeCl3可以用铁粉与_______ 反应制备,保存FeCl2溶液会加入少量铁屑,其原理是_______ (用化学方程式表示)。
(3)电子工业需要用30%的FeCl3溶液腐蚀敷在绝缘板上的铜,制造印刷电路板,请写出FeCl3溶液与铜反应的离子方程式:_______ 。某校同学为测定FeCl3腐蚀铜后所得溶液的组成,进行了如下实验:
①甲同学取少量待测溶液﹐滴入_______ (写出试剂名称),溶液呈红色,证明溶液中含有Fe3+。
②乙同学取少量待测溶液﹐滴加酸性高锰酸钾溶液,振荡后紫红色褪去,因此他得出结论,溶液中存在Fe2+。丙同学认为乙同学的实验方法不严谨,理由是_______ 。(用离子方程式和必要的文字进行解释)已知:氧化性KMnO4>Cl2
③通过查阅资料,同学们得知,Fe2+能与K3[Fe(CN)6)]溶液反应生成Fe3[Fe(CN)6)]2蓝色沉淀。乙同学另取少量待测溶液﹐滴加K3[Fe(CN)6)]溶液,有蓝色沉淀生成,证明溶液中存在Fe2+。该反应的离子方程式为_______ 。
(4)欲从FeCl3腐蚀铜后所得溶液中回收铜,并重新获得FeCl3溶液,设计实验方案如下:
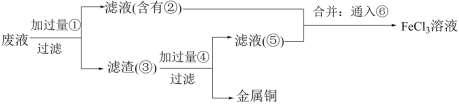
已知⑥为黄绿色的气体单质,请写出通入⑥的离子方程式:_______ 。用H2O2代替⑥也能实现实验目的。请写出加入H2O2的离子方程式:_______ 。
(1)向沸水中逐滴滴加lmol/LFeCl3溶液﹐至液体呈透明的红褐色,该分散系中粒子直径的范围是
(2)在实验室中,FeCl3可以用铁粉与
(3)电子工业需要用30%的FeCl3溶液腐蚀敷在绝缘板上的铜,制造印刷电路板,请写出FeCl3溶液与铜反应的离子方程式:
①甲同学取少量待测溶液﹐滴入
②乙同学取少量待测溶液﹐滴加酸性高锰酸钾溶液,振荡后紫红色褪去,因此他得出结论,溶液中存在Fe2+。丙同学认为乙同学的实验方法不严谨,理由是
③通过查阅资料,同学们得知,Fe2+能与K3[Fe(CN)6)]溶液反应生成Fe3[Fe(CN)6)]2蓝色沉淀。乙同学另取少量待测溶液﹐滴加K3[Fe(CN)6)]溶液,有蓝色沉淀生成,证明溶液中存在Fe2+。该反应的离子方程式为
(4)欲从FeCl3腐蚀铜后所得溶液中回收铜,并重新获得FeCl3溶液,设计实验方案如下:
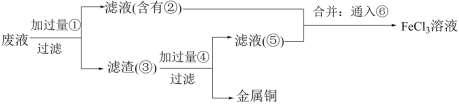
已知⑥为黄绿色的气体单质,请写出通入⑥的离子方程式:
您最近一年使用:0次
2022-04-05更新
|
408次组卷
|
2卷引用:四川省成都市龙泉驿区教育科学研究院2021-2022学年高二下学期期中考试化学试卷
2 . 某兴趣小组研究亚硝酸钠,查阅下列资料,试根据信息回答下列问题。
(1)已知NaNO2能发生如下反应: 2NaNO2+4HI=2NO↑+I2+2NaI+2H2O。请用双线桥表示电子转移的方向和数目。________________ ;该反应中氧化剂是_____ ;若有0.75mol电子转移,则被还原的氧化剂粒子数为_______ 。(用NA表示)
(2)误食NaNO2会导致血红蛋白中的Fe2+转化为Fe3+而中毒,可服用维生素C解毒。下列分析错误的是______ (填序号)。
A.NaNO2被还原 B.维生素C具有还原性
C.还原性: 维生素C > Fe2+ D.NaNO2是还原剂
(3)下列方法中,可用来区分NaNO2和NaCl的是______ (填序号)。
A. 焰色反应 B.分别滴加酸化FeSO4溶液和KSCN溶液
C.在酸性条件下加入KI 淀粉溶液 D.分别滴加AgNO3溶液
(4)某同学把新制的氯水加到NaNO2溶液中,观察到氯水褪色,同时生成NaNO3和HCl,请写出反应的离子方程式:_______________ 。
| 药品 | NaNO2 (亚硝酸钠) |
| 性质 | 1.在酸性溶液中有较强氧化性,能将Fe2+ 氧化成Fe3+ ; 2.AgNO2是一种难溶于水、易溶于酸的盐。 |
(1)已知NaNO2能发生如下反应: 2NaNO2+4HI=2NO↑+I2+2NaI+2H2O。请用双线桥表示电子转移的方向和数目。
(2)误食NaNO2会导致血红蛋白中的Fe2+转化为Fe3+而中毒,可服用维生素C解毒。下列分析错误的是
A.NaNO2被还原 B.维生素C具有还原性
C.还原性: 维生素C > Fe2+ D.NaNO2是还原剂
(3)下列方法中,可用来区分NaNO2和NaCl的是
A. 焰色反应 B.分别滴加酸化FeSO4溶液和KSCN溶液
C.在酸性条件下加入KI 淀粉溶液 D.分别滴加AgNO3溶液
(4)某同学把新制的氯水加到NaNO2溶液中,观察到氯水褪色,同时生成NaNO3和HCl,请写出反应的离子方程式:
您最近一年使用:0次
2018-01-31更新
|
534次组卷
|
6卷引用:【全国校级联考】辽宁省六校协作体2018-2019学年高二上学期期初考试化学试题
3 . 某班同学用如下实验探究Fe2+、Fe3+和FeO42-的性质。
资料:K2FeO4为紫色固体,微溶于KOH溶液;具有强氧化性,在酸性或中性溶液中快速产生O2,在碱性溶液中较稳定。回答下列问题:
(1)分别取一定量氯化铁、氯化亚铁固体,均配制成0.1mol/L的溶液。在FeCl2溶液中需加入少量铁屑,其目的是________ ;将FeCl3晶体溶于浓盐酸,再稀释到需要的浓度,盐酸的作用是________ 。
(2)制备K2FeO4(夹持装置略)后,取C中紫色溶液,加入稀硫酸,产生黄绿色气体,得溶液a,经检验气体中含有Cl2。为证明是否K2FeO4氧化了Cl-而产生Cl2,设计以下方案:
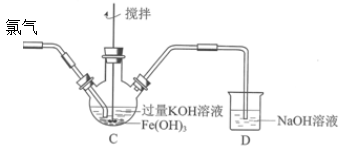
Ⅰ.由方案Ⅰ中溶液变红可知a中含有______ 离子,但该离子的产生不能判断一定是K2FeO4将Cl-氧化,还可能由________________ 产生(用方程式表示)。
Ⅱ.方案Ⅱ可证明K2FeO4氧化了Cl-。用KOH溶液洗涤的目的是________________ 。根据K2FeO4的制备原理3Cl2+2Fe(OH)3+10KOH=2K2FeO4+6KCl+8H2O得出:氧化性Cl2______ FeO42-(填“>”或“<”),而方案Ⅱ实验表明,Cl2和FeO42-的氧化性强弱关系相反,原因是________________ 。
资料:K2FeO4为紫色固体,微溶于KOH溶液;具有强氧化性,在酸性或中性溶液中快速产生O2,在碱性溶液中较稳定。回答下列问题:
(1)分别取一定量氯化铁、氯化亚铁固体,均配制成0.1mol/L的溶液。在FeCl2溶液中需加入少量铁屑,其目的是
(2)制备K2FeO4(夹持装置略)后,取C中紫色溶液,加入稀硫酸,产生黄绿色气体,得溶液a,经检验气体中含有Cl2。为证明是否K2FeO4氧化了Cl-而产生Cl2,设计以下方案:
| 方案Ⅰ | 取少量a,滴加KSCN溶液至过量,溶液呈红色。 |
| 方案Ⅱ | 用KOH溶液充分洗涤C中所得固体,再用KOH溶液将K2FeO4溶出,得到紫色溶液b。取少量b,滴加盐酸,有Cl2产生。 |

Ⅰ.由方案Ⅰ中溶液变红可知a中含有
Ⅱ.方案Ⅱ可证明K2FeO4氧化了Cl-。用KOH溶液洗涤的目的是
您最近一年使用:0次
名校
解题方法
4 . 某小组在验证H2O2氧化Fe2+时发现异常现象,并对其进行深入探究。
实验I:
(1)实验I中溶液变红是因为Fe3+与SCN-发生了反应,其离子方程式是__ 。
(2)探究实验I中红色褪去的原因:取反应后溶液,___ (填实验操作和现象),证明溶液中有Fe3+,而几乎无SCN-。
(3)研究发现,酸性溶液中H2O2能氧化SCN-,但反应很慢且无明显现象,而实验I中褪色相对较快,由此推测Fe3+能加快H2O2与SCN-的反应。通过实验II和III得到了证实。参照实验II的图例,在虚线框内补全实验III:__ 。
实验II:
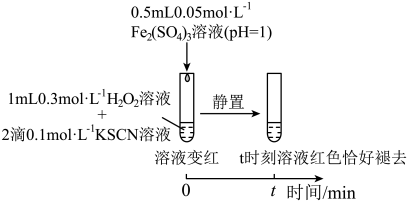
实验III:
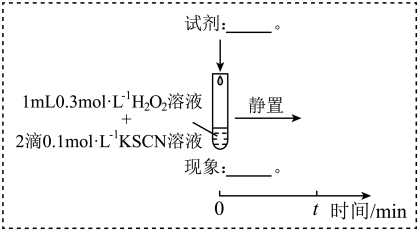
(4)查阅资料:Fe3+加快H2O2与SCN-反应的主要机理有
i.Fe3++H2O2=Fe2++HO2·+H+
ii.Fe2++H2O2=Fe3++·OH+OH-
iii.OH(羟基自由基)具有强氧化性,能直接氧化SCN-
为探究Fe2+对H2O2与SCN-反应速率的影响,设计实验如图:
实验IV:

①t′<t,对比实验IV和II可得出结论:在本实验条件下,___ 。
②结合资料和(1)~(4)的研究过程,从反应速率和化学平衡的角度解释实验I中溶液先变红后褪色的原因:____ 。
③实验I~IV中均有O2生成,小组同学推测可能是HO2·与溶液中其他微粒相互作用生成的,这些微粒有___ 。
实验I:
| 装置与操作 | 现象 |
 | 溶液立即变红,继续滴加H2O2溶液,红色变浅并逐渐褪去 |
(2)探究实验I中红色褪去的原因:取反应后溶液,
(3)研究发现,酸性溶液中H2O2能氧化SCN-,但反应很慢且无明显现象,而实验I中褪色相对较快,由此推测Fe3+能加快H2O2与SCN-的反应。通过实验II和III得到了证实。参照实验II的图例,在虚线框内补全实验III:
实验II:

实验III:

(4)查阅资料:Fe3+加快H2O2与SCN-反应的主要机理有
i.Fe3++H2O2=Fe2++HO2·+H+
ii.Fe2++H2O2=Fe3++·OH+OH-
iii.OH(羟基自由基)具有强氧化性,能直接氧化SCN-
为探究Fe2+对H2O2与SCN-反应速率的影响,设计实验如图:
实验IV:

①t′<t,对比实验IV和II可得出结论:在本实验条件下,
②结合资料和(1)~(4)的研究过程,从反应速率和化学平衡的角度解释实验I中溶液先变红后褪色的原因:
③实验I~IV中均有O2生成,小组同学推测可能是HO2·与溶液中其他微粒相互作用生成的,这些微粒有
您最近一年使用:0次
2021-08-13更新
|
638次组卷
|
7卷引用:北京市铁路第二中学2022-2023学年高二上学期期中检测化学试题
解题方法
5 . 菠菜是常见食品,可以补充入体所必需的微量元素铁。某兴趣小组设计实验,探究菠菜中铁元素的价态和含量,实验流程如下:
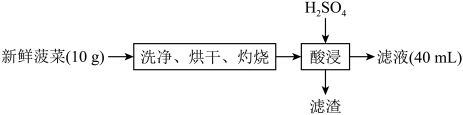
回答下列问题:
(1)灼烧过程中必须用到下列仪器中的___________(填标号)。
(2)灼烧的灰烬中含有铁的氧化物,硫酸酸浸的目的是___________ 。
(3)取少许滤液于试管中,滴入几滴KSCN溶液,显红色,说明滤液中含有_______ ;另取滤液检验,滤液能使 溶液紫色褪去,说明滤液中存在具有
溶液紫色褪去,说明滤液中存在具有_____ (填“氧化性”或“还原性”)的粒子。
(4)为进一步探究 和
和 的氧化性和还原性,该兴趣小组设计并进行如下实验,记录现象,完成实验报告。
的氧化性和还原性,该兴趣小组设计并进行如下实验,记录现象,完成实验报告。
(5)分光光度法测量铁元素含量的流程示意如下:

①用离子方程式解释加入且 的目的是
的目的是___________ 。
②溶液颜色越深,光的透过能力越差,即透光率越小。若不加 ,测出菠菜中铁元素的含量
,测出菠菜中铁元素的含量___________ (填“偏大”或“偏小”)。
③测得10mL滤液中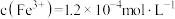 ,该菠菜中铁元素的含量为
,该菠菜中铁元素的含量为________ mg/100g。

回答下列问题:
(1)灼烧过程中必须用到下列仪器中的___________(填标号)。
A. | B. | C. | D. |
(3)取少许滤液于试管中,滴入几滴KSCN溶液,显红色,说明滤液中含有
 溶液紫色褪去,说明滤液中存在具有
溶液紫色褪去,说明滤液中存在具有(4)为进一步探究
 和
和 的氧化性和还原性,该兴趣小组设计并进行如下实验,记录现象,完成实验报告。
的氧化性和还原性,该兴趣小组设计并进行如下实验,记录现象,完成实验报告。| 实验操作 | 实验现象 | 离子方程式 | 实验结论 |
向 溶液中添加新制氯水 溶液中添加新制氯水 | 溶液由浅绿色变为棕黄色 |  | ① |
向 溶液加入足量的铁粉 溶液加入足量的铁粉 | 铁粉逐渐溶解,溶液由棕黄色变为浅绿色 | ② |  具有氧化性 具有氧化性 |

①用离子方程式解释加入且
 的目的是
的目的是②溶液颜色越深,光的透过能力越差,即透光率越小。若不加
 ,测出菠菜中铁元素的含量
,测出菠菜中铁元素的含量③测得10mL滤液中
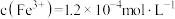 ,该菠菜中铁元素的含量为
,该菠菜中铁元素的含量为
您最近一年使用:0次
名校
6 . 某小组同学对FeCl3与KI的反应进行探究。
【初步探究】室温下进行下表所列实验。
(1)证明实验Ⅰ中有I2生成,加入的试剂为_______ 。
(2)实验Ⅱ可以证明Fe3+与I-发生可逆反应,其操作为_______ 。
(3)写出实验Ⅰ反应的离子方程式:_______ 。
(4)实验Ⅰ中溶液的颜色不变后再进行后续实验,其目的是_______ 。
【深入探究】20min后继续观察实验现象:实验Ⅰ溶液棕黄色变深;实验Ⅱ溶液红色变浅。
(5)已知在酸性较强的条件下,I-可被空气氧化为I2,故甲同学提出假设:该反应条件下空气将I-氧化为I2,使实验Ⅰ中溶液棕黄色变深。甲同学设计实验:_______ ,20 min内溶液不变蓝,证明该假设不成立,导致溶液不变蓝的因素 可能是_______ (写出1条即可)。
(6)乙同学查阅资料可知:FeCl3与KI的反应体系中还存在I-+I2 I
I ,I
,I 呈棕褐色。依据资料从平衡移动原理解释实验Ⅱ中20 min后溶液红色变浅的原因:
呈棕褐色。依据资料从平衡移动原理解释实验Ⅱ中20 min后溶液红色变浅的原因:_______ 。
【初步探究】室温下进行下表所列实验。
| 序号 | 操作 | 现象 |
| 实验Ⅰ | 取5 mL0.1 mol·L-1KI溶液,滴加0.1 mol·L-1FeCl3溶液5~6滴(混合溶液pH=5) | 溶液变为棕黄色 |
| 实验Ⅱ | _______ | 溶液变红 |
(2)实验Ⅱ可以证明Fe3+与I-发生可逆反应,其操作为
(3)写出实验Ⅰ反应的离子方程式:
(4)实验Ⅰ中溶液的颜色不变后再进行后续实验,其目的是
【深入探究】20min后继续观察实验现象:实验Ⅰ溶液棕黄色变深;实验Ⅱ溶液红色变浅。
(5)已知在酸性较强的条件下,I-可被空气氧化为I2,故甲同学提出假设:该反应条件下空气将I-氧化为I2,使实验Ⅰ中溶液棕黄色变深。甲同学设计实验:
(6)乙同学查阅资料可知:FeCl3与KI的反应体系中还存在I-+I2
 I
I ,I
,I 呈棕褐色。依据资料从平衡移动原理解释实验Ⅱ中20 min后溶液红色变浅的原因:
呈棕褐色。依据资料从平衡移动原理解释实验Ⅱ中20 min后溶液红色变浅的原因:
您最近一年使用:0次
2022-10-22更新
|
212次组卷
|
3卷引用:北京市顺义牛栏山第一中学2022-2023学年高二上学期10月月考化学试题
7 . 黑木耳是常见食品,可以补充人体所必需的微量元素铁。某兴趣小组设计实验,检验黑木耳中的铁元素,实验流程如图:
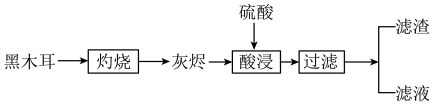
(1)灼烧黑木耳必须用到下列仪器中的___ (填字母)。
A. B.
B. C.
C. D.
D.
(2)灰烬中含有铁的氧化物以及钾、钙、硅等元素的化合物,酸浸的目的是___ 。
(3)取少许滤液于试管中,滴入几滴KSCN溶液,显红色,说明滤液中含有___ ;另取滤液检验,滤液能使KMnO4溶液紫色褪去,说明滤液中存在具有___ (填“氧化性”或“还原性”)的粒子。
(4)为进一步探究Fe3+和Fe2+的氧化性和还原性,该兴趣小组设计并进行如下实验,记录现象,完成实验报告。
(5)实验结束,离开实验室之前,下列做法正确的是___ (填字母)。
A.废弃药品直接倒入水池冲走 B.药品仪器归放
C.清洁实验仪器,打扫实验室卫生 D.关闭水电、门窗

(1)灼烧黑木耳必须用到下列仪器中的
A.
 B.
B. C.
C. D.
D.
(2)灰烬中含有铁的氧化物以及钾、钙、硅等元素的化合物,酸浸的目的是
(3)取少许滤液于试管中,滴入几滴KSCN溶液,显红色,说明滤液中含有
(4)为进一步探究Fe3+和Fe2+的氧化性和还原性,该兴趣小组设计并进行如下实验,记录现象,完成实验报告。
| 实验操作 | 实验现象 | 离子方程式 | 实验结论 |
| 向FeCl2溶液中添加新制氯水 | 溶液由浅绿色变为棕黄色 | 2Fe2++Cl2=2Fe3++2Cl- | ① |
| 向FeCl3溶液加入足量的铁粉 | 铁粉逐渐溶解,溶液由棕黄色变为浅绿色 | ② | Fe3+具有氧化性 |
A.废弃药品直接倒入水池冲走 B.药品仪器归放
C.清洁实验仪器,打扫实验室卫生 D.关闭水电、门窗
您最近一年使用:0次
2021-05-23更新
|
767次组卷
|
5卷引用:2021年1月广东省普通高中学业水平合格性考试化学试题
2021年1月广东省普通高中学业水平合格性考试化学试题(已下线)第12讲 铁、亚铁盐和铁盐-【暑假自学课】2022年新高一化学暑假精品课(鲁科版2019必修第一册)(已下线)考点14 铁及其化合物-备战2023年高考化学一轮复习考点帮(全国通用)广东省深圳市南头中学2021~2022学年下学期期中考试化学试题 (学考科目)(已下线)考点14 铁及其化合物(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)
8 . 下列实验与结论相匹配的是
| 选项 | 实验 | 结论 |
| A | 向某溶液中滴加盐酸酸化的氯化钡溶液,产生白色沉淀 | 该溶液中一定有 |
| B | 取少量菠菜叶剪碎研磨后加水搅拌,取上层清液于试管中,加入稀硝酸后再加入 溶液 溶液 | 若溶液变红,说明菠菜中含有铁元素 |
| C | 用玻璃棒蘸取浓硫酸滴到蓝色石蕊试纸上,试纸先变红后变黑 | 浓硫酸具有氧化性 |
| D | 将电石与饱和食盐水反应产生的气体直接通入酸性 溶液中,溶液褪色 溶液中,溶液褪色 | 乙炔具有还原性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
9 . 下列实验对应的现象和结论都正确的是
| 选项 | 实验 | 现象 | 结论 |
| A | 向食品脱氧剂样品(含还原铁粉)中加入硫酸后滴加酸性 溶液 溶液 | 紫红色褪去 | 食品脱氧剂样品中含 |
| B | 向 溶液中滴入 溶液中滴入 溶液,再滴加 溶液,再滴加 溶液 溶液 | 加入 后溶液变成血红色 后溶液变成血红色 |  既有氧化性又有还原性 既有氧化性又有还原性 |
| C | 向 溶液加入铜片 溶液加入铜片 | 溶液变蓝、有黑色固体出现 | 金属铁比铜活泼 |
| D | 向 溶液中加入 溶液中加入 溶液后滴加几滴淀粉溶液 溶液后滴加几滴淀粉溶液 | 溶液变为蓝色 | 氧化性: |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-03-16更新
|
2273次组卷
|
5卷引用:河北省石家庄市第二中学2022-2023学年高二下学期期末考试化学试题
河北省石家庄市第二中学2022-2023学年高二下学期期末考试化学试题广东省广州市2023届高三一模考试化学试题(已下线)专题14 化学实验方案的设计与评价(已下线)广东省广州市天河区2023届高三二模化学试题变式题(选择题11-16)广东省广州市2022-2023学年高三普通高中毕业班综合测试(一)化学试题
解题方法
10 . 下列实验目的、实验操作及现象、结论均正确的是
| 选项 | 实验目的 | 实验操作及现象 | 结论 |
| A | 判断强酸和弱酸 |  溶液显碱性, 溶液显碱性, 溶液显酸性 溶液显酸性 | 可以确定 是弱酸,无法判断 是弱酸,无法判断 是否为弱酸 是否为弱酸 |
| B | 判断反应物的浓度对平衡的影响 | 向 溶液中加入 溶液中加入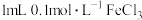 溶液,达到平衡,再加入 溶液,达到平衡,再加入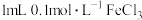 溶液,溶液红色加深 溶液,溶液红色加深 | 说明增大反应物浓度,化学平衡正向移动 |
| C | 验证 的氧化性 的氧化性 | 向黄绿色的氯水中加入 溶液,溶液黄绿色褪去 溶液,溶液黄绿色褪去 |  有强氧化性 有强氧化性 |
| D | 验证菠菜中含有铁元素 | 将新鲜菠菜剪碎、研磨、溶解、过滤,向滤液中加入几滴KSCN溶液,溶液不变红 | 说明菠菜中不含铁元素 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次



