1 . 可用KSCN溶液检验的离子为
| A.Na+ | B.Ag+ | C.Fe2+ | D.Fe3+ |
您最近一年使用:0次
2020-12-19更新
|
372次组卷
|
5卷引用:上海市浦东新区2019-2020学年高二上学期期末考试化学试题
名校
解题方法
2 . 电子工业中常用FeCl3溶液腐蚀镀铜板来制作印刷电路板,利用腐蚀后所得废液回收Cu并循环利用FeCl3溶液的流程图如下:
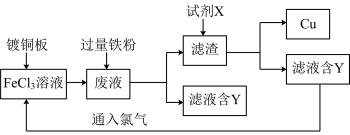
请回答:
(1)FeCl3溶液与镀铜板反应的化学方程式是___________ 。
(2)流程图中滤渣的化学成分是___________ (填化学式)。要检验废液中是否含有Fe3+所需的试剂是_______ 溶液(填化学式),废液中是否含有Fe3+现象为:________ 。
(3)试剂X是___________ 。
(4)滤液中含有的物质Y与氯气反应的离子方程式是___________ 。

请回答:
(1)FeCl3溶液与镀铜板反应的化学方程式是
(2)流程图中滤渣的化学成分是
(3)试剂X是
(4)滤液中含有的物质Y与氯气反应的离子方程式是
您最近一年使用:0次
3 . 只用下列试剂中的一种,就能将FeCl3、AlCl3和NaCl三种溶液区别开的是
| A.KSCN溶液 | B.BaCl2溶液 | C.NaOH溶液 | D.AgNO3溶液 |
您最近一年使用:0次
名校
解题方法
4 . 某工厂排放的工业废水中含Fe3+、Al3+、Cu2+,工厂为了减少环境污染,利用废铁屑和其他化学试剂进行如图操作,得到了铁红、Al2O3和金属Cu,回答下列问题:

(1)固体A的成分是_____ 。(用化学式表示)
(2)写出B→D的离子方程式_____ 。要检验溶液D中是否含有Fe3+所需的试剂是______ (用化学式表示)溶液,若含有Fe3+则观察到的现是________ 。
(3)溶液E焰色反应呈黄色,试剂H是_______ (用化学式表示);D→E反应的离子方程式是________ 。
(4)写出铁红在工业上的一种主要用途:_______ 。

(1)固体A的成分是
(2)写出B→D的离子方程式
(3)溶液E焰色反应呈黄色,试剂H是
(4)写出铁红在工业上的一种主要用途:
您最近一年使用:0次
2020-12-10更新
|
291次组卷
|
4卷引用:广东省肇庆市端州区肇庆市第一中学2020-2021学年高一上学期诊断性测试(三)化学试题
5 . 下列实验报告中,完全正确的是
| 序号 | 实验操作 | 现象 | 结论 |
| A | 向溶液中滴加用盐酸酸化的BaCl2溶液 | 有白色沉淀 | 原溶液中含 |
| B | 向溶液中滴加氯水后,再滴入KSCN溶液 | 溶液变红色 | 原溶液中含Fe3+ |
| C | 向装有Na2O2的试管中加入水后,立即滴加酚酞试液 | 溶液先变红后褪色 | Na2O2有漂白性 |
| D | 用洁净的玻璃棒蘸取溶液进行焰色反应 | 观察到有紫色火焰 | 原溶液中有K+ |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
6 . 下列化学反应的离子方程式正确的是
| A.氢氧化铝中滴加盐酸:H++OH-=H2O |
B.碳酸氢钙溶液中加入氢氧化钠溶液: +OH-= +OH-= +H2O +H2O |
C.金属铝溶于氢氧化钠溶液:2Al +6OH-=2 +3H2↑ +3H2↑ |
| D.用FeCl3溶液腐蚀铜电路板:2Fe3++Cu=2Fe2++Cu2+ |
您最近一年使用:0次
2020-12-10更新
|
291次组卷
|
3卷引用:广东省肇庆市端州区肇庆市第一中学2020-2021学年高一上学期诊断性测试(三)化学试题
名校
解题方法
7 . 一种磁性材料的磨削废料(含镍质量分数约21%)主要成分是铁镍合金,还含有铜、钙、镁、硅的氧化物。由该废料制备纯度较高的氢氧化镍,工艺流程如下:
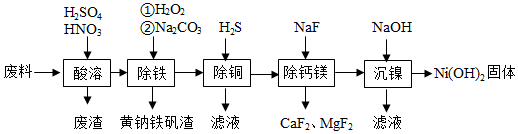
回答下列问题:
(1)合金中的镍难溶于稀硫酸,“酸溶”时除了加入稀硫酸,还要边搅拌边缓慢加入稀硝酸,反应有 生成。写出金属镍溶解的离子方程式
生成。写出金属镍溶解的离子方程式_____ ,“酸溶”时产生的废渣主要成分为_________ 。
(2)“除铁”时H2O2的作用是______ ,为了证明添加的H2O2已足量,应选择的试剂是________ (填“铁氰化钾”或“硫氰化钾”的化学式)溶液。黄钠铁矾 有沉淀颗粒大、沉淀速率快、容易过滤等特点,已知x=1、y=3、m=2,则n=
有沉淀颗粒大、沉淀速率快、容易过滤等特点,已知x=1、y=3、m=2,则n=____ ,写出“除铁”中加入Na2CO3时反应的离子方程式_____ 。
(3)“除铜”时,反应的离子方程式为______ ,若用Na2S代替H2S除铜,优点是_____ 。
(4)已知“除钙镁”过程在陶瓷容器中进行,NaF的实际用量为理论用量的1.1倍,用量不宜过大的原因是______ 。
(5)100kg废料经上述工艺制得Ni(OH)2固体的质量为31 kg,则镍回收率的计算式为______ 。

回答下列问题:
(1)合金中的镍难溶于稀硫酸,“酸溶”时除了加入稀硫酸,还要边搅拌边缓慢加入稀硝酸,反应有
 生成。写出金属镍溶解的离子方程式
生成。写出金属镍溶解的离子方程式(2)“除铁”时H2O2的作用是
 有沉淀颗粒大、沉淀速率快、容易过滤等特点,已知x=1、y=3、m=2,则n=
有沉淀颗粒大、沉淀速率快、容易过滤等特点,已知x=1、y=3、m=2,则n=(3)“除铜”时,反应的离子方程式为
(4)已知“除钙镁”过程在陶瓷容器中进行,NaF的实际用量为理论用量的1.1倍,用量不宜过大的原因是
(5)100kg废料经上述工艺制得Ni(OH)2固体的质量为31 kg,则镍回收率的计算式为
您最近一年使用:0次
名校
8 . 下列实验中,对应的现象以及结论都正确且两者具有因果关系的是
| 选项 | 实验 | 现象 | 结论 |
| A | 将稀硝酸加入过量铁粉中,充分反应后滴加KSCN溶液 | 有气体生成,溶液呈血红色 | 稀硝酸将Fe氧化为Fe3+ |
| B | 将铜粉加1.0 mol·L-1Fe2(SO4)3溶液中 | 溶液变蓝、有黑色固体出现 | 金属铁比铜活泼 |
| C | SO2通入到酸性高锰酸钾溶液中 | 紫红色褪去 | 二氧化硫具有漂白性 |
| D | 将浓硫酸滴到蔗糖表面 | 固体变黑膨胀 | 浓硫酸有脱水性和强氧化性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2020-12-08更新
|
974次组卷
|
3卷引用:华南师范大学附属中学2021届高三综合测试二化学试题
名校
解题方法
9 . 下列实验方案可行的是
| A.用浓硫酸干燥NH3 | B.用碱石灰干燥SO2气体 |
| C.用NaOH溶液除去Cl2中的HCl | D.加入Fe粉除去Fe2+溶液中的杂质Fe3+ |
您最近一年使用:0次
2020-12-02更新
|
256次组卷
|
3卷引用:广东省河源市东源县2020-2021学年高二上学期第一次段考化学试题(合格考)
名校
解题方法
10 . 已知A、B、C均为含铁化合物,请根据以下四种物质的转化过程回答相关问题:
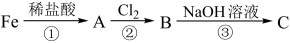
(1)反应①、②、③中属于氧化还原反应的是_______ (填序号);
(2)向B的溶液中滴入几滴KSCN溶液后,可观察到的现象是__________________ ;
(3)C的化学式为____________ ;
(4)氯气是一种有强烈刺激性气味的________ 色气体,写出反应②的离子方程式__________ ;
(5)加入铁粉可以实现B转化为A,请写出实现该转化的化学方程式___________________ 。
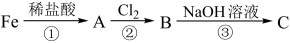
(1)反应①、②、③中属于氧化还原反应的是
(2)向B的溶液中滴入几滴KSCN溶液后,可观察到的现象是
(3)C的化学式为
(4)氯气是一种有强烈刺激性气味的
(5)加入铁粉可以实现B转化为A,请写出实现该转化的化学方程式
您最近一年使用:0次



