解题方法
1 . 下列反应的离子方程式错误的是
A. 与KI溶液反应: 与KI溶液反应: |
B.盐酸与KOH溶液反应: |
C.Fe与 溶液反应: 溶液反应: |
D. 溶液与氨水反应: 溶液与氨水反应: |
您最近一年使用:0次
名校
解题方法
2 . 以硫酸厂矿渣(含Fe2O3,α-Al2O3,SiO2等)为原料制备铁黄(FeOOH)的工艺流程如图:
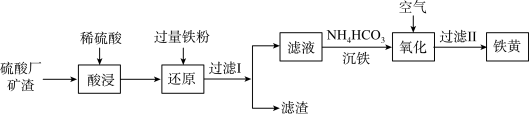
资料:i. α-Al2O3化学性质极不活泼,不溶于水也不溶于酸或碱。
ii.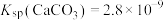 ;
;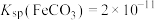 。回答下列问题:
。回答下列问题:
(1)为了提高“酸浸”的效率可以采用的措施有_________________________ (写出两种即可)。
(2)“还原”过程中的离子方程式为_____________________________________ 。
(3)“滤渣”中主要成分为(填化学式)_______________ 。
(4)①沉铁是将二价铁转化为难溶性碳酸盐,这个过程中有 气体产生,反应的离子方程式为
气体产生,反应的离子方程式为_______ 。
②“沉铁”过程中往往有副产物Fe(OH)2生成,分析原因是______________ 。
③若用 “沉铁”,则无副产物Fe(OH)2产生,当反应完成时,溶液中
“沉铁”,则无副产物Fe(OH)2产生,当反应完成时,溶液中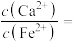
__________ 。
(5)工业上为了充分利用铁资源,硫酸厂矿渣也可以用来炼铁,在1225℃、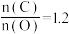 时,焙烧时间与金属产率的关系如图:
时,焙烧时间与金属产率的关系如图:

请分析焙烧时间超过15min时,金属产率下降的原因可能是_____________ 。

资料:i. α-Al2O3化学性质极不活泼,不溶于水也不溶于酸或碱。
ii.
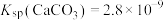 ;
;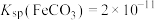 。回答下列问题:
。回答下列问题:(1)为了提高“酸浸”的效率可以采用的措施有
(2)“还原”过程中的离子方程式为
(3)“滤渣”中主要成分为(填化学式)
(4)①沉铁是将二价铁转化为难溶性碳酸盐,这个过程中有
 气体产生,反应的离子方程式为
气体产生,反应的离子方程式为②“沉铁”过程中往往有副产物Fe(OH)2生成,分析原因是
③若用
 “沉铁”,则无副产物Fe(OH)2产生,当反应完成时,溶液中
“沉铁”,则无副产物Fe(OH)2产生,当反应完成时,溶液中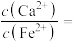
(5)工业上为了充分利用铁资源,硫酸厂矿渣也可以用来炼铁,在1225℃、
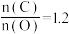 时,焙烧时间与金属产率的关系如图:
时,焙烧时间与金属产率的关系如图:
请分析焙烧时间超过15min时,金属产率下降的原因可能是
您最近一年使用:0次
3 . 下列离子方程式中,正确的是
A.铜片加入稀硝酸中: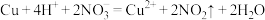 |
B.氧化铜加入稀硫酸中: |
C.铁粉加入氯化铁溶液中: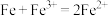 |
D.氯化钠溶液加入硝酸银溶液中: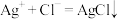 |
您最近一年使用:0次
名校
解题方法
4 . 下列指定反应的离子方程式正确的是
| A.金属钠放入水中:Na+2H2O=Na++2OH−+H2↑ |
| B.将铁粉放入FeCl3溶液中:Fe3++Fe=2Fe2+ |
C.将铜丝插入稀硝酸中:Cu+4H++2NO =Cu2++2NO2↑+H2O =Cu2++2NO2↑+H2O |
D.NaOH溶液中通入过量的二氧化碳:CO2+OH−=HCO |
您最近一年使用:0次
2022-07-10更新
|
111次组卷
|
2卷引用:四川省甘孜州2021-2022学年高二下学期学业质量统一监测期末统考化学试题
名校
5 . 下表是Fe2+、Fe3+、Cu2+被完全沉淀时溶液的pH。某硫酸铜酸性溶液中含有少量Fe2+、Fe3+杂质,为制得纯净的CuSO4,加入试剂最佳组合是
| 金属离子 | Fe2+ | Fe3+ | Cu2+ |
| 完全沉淀时的pH | 7.7 | 4.5 | 6.7 |
| A.H2O2、CuO | B.氨水 |
| C.KMnO4、CuCO3 | D.NaOH溶液 |
您最近一年使用:0次
名校
6 . 设NA表示阿伏加德罗常数的值,下列说法正确的是
| A.等体积的CO2和CO,分子数目均为NA |
| B.标准状况下,22.4 L的H2和22.4 L的F2混合后,气体分子数为2NA |
| C.有铁粉参加的反应若生成3 mol Fe2+,则转移电子数为6NA |
| D.10.1 g N(C2H5)3中所含的极性共价键数目为1.8NA |
您最近一年使用:0次
解题方法
7 . 一定量的盐酸跟过量的铁粉反应时,为了减缓反应速度,且不影响生成氢气的总量,可向盐酸中加入适量的
| A.NaOH(s) | B.CH3COONa(s) | C.FeCl3(s) | D.NaNO3溶液 |
您最近一年使用:0次
名校
8 . 下列实验中,对应的现象以及结论都正确且两者具有因果关系的是( )
| 选项 | 实验 | 现象 | 结论 |
| A | 将稀硝酸加入过量铁粉中,充分反应后滴加 溶液 溶液 | 有气体生成,溶液呈血红色 | 稀硝酸将 氧化为 氧化为 |
| B | 将铜粉加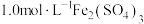 溶液中 溶液中 | 溶液变蓝、有黑色固体出现 | 金属铁比铜活泼 |
| C |  晶体溶于稀硫酸,滴加 晶体溶于稀硫酸,滴加 溶液 溶液 | 溶液变红 |  晶体已变 晶体已变质 |
| D | 取少量绿矾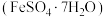 溶于稀硫酸中,滴加 溶于稀硫酸中,滴加 溶液。 溶液。 | 溶液未变红色 | 绿矾未因氧化而变质 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
9 . 用铁泥(主要成分为Fe2O3、FeO和少量Fe)制备纳米Fe3O4,的流程示意图如下:
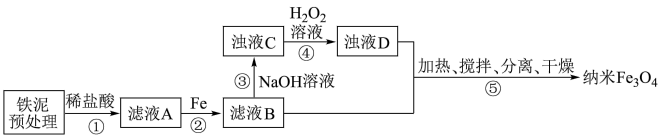
下列叙述错误的是

下列叙述错误的是
| A.为提高步骤①的反应速率,可采取搅拌、升温等措施 |
| B.步骤②中,主要反应的离子方程式是2Fe3++Fe=3Fe2+ |
| C.步骤④中,反应完成后剩余的H2O2无需除去 |
| D.步骤⑤中,“分离”包含的操作有过滤、洗涤 |
您最近一年使用:0次
2019-02-26更新
|
784次组卷
|
7卷引用:四川省内江市威远中学2023-2024学年高二上学期第一次月考化学试题



