1 . 铁及其化合物在日常生产生活中有着广泛应用。
I.在常温下,Fe与水并不起反应,但在高温下,Fe与水蒸气可发生反应。现设计如下装置完成高温下“Fe与水蒸气反应”的实验,并检验其产物(已知:Fe3O4中Fe的化合价为+2价、+3价)。
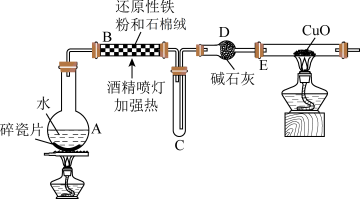
(1)装置B中发生反应的化学方程式为___________ 。
(2)装置C中导管“短进长出”的原因___________ 。
(3)取反应后得到的黑色粉末放入一试管中,加入稀硫酸将固体溶解,再滴加几滴KSCN溶液,振荡,溶液没有出现红色,原因是___________ (用离子方程式表示)。
II.某学生设计了如图装置制备白色Fe(OH)2固体。
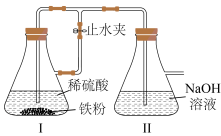
(4)开始实验时,先打开止水夹,待装置中空气已排尽,再关闭止水夹。
①关闭止水夹前,如何证明装置中空气已排尽:___________ 。
②装置II中发生反应的主要化学方程式为___________ 。
③若未排净装置中的空气,则装置II中观察到的实验现象为___________ 。
I.在常温下,Fe与水并不起反应,但在高温下,Fe与水蒸气可发生反应。现设计如下装置完成高温下“Fe与水蒸气反应”的实验,并检验其产物(已知:Fe3O4中Fe的化合价为+2价、+3价)。

(1)装置B中发生反应的化学方程式为
(2)装置C中导管“短进长出”的原因
(3)取反应后得到的黑色粉末放入一试管中,加入稀硫酸将固体溶解,再滴加几滴KSCN溶液,振荡,溶液没有出现红色,原因是
II.某学生设计了如图装置制备白色Fe(OH)2固体。

(4)开始实验时,先打开止水夹,待装置中空气已排尽,再关闭止水夹。
①关闭止水夹前,如何证明装置中空气已排尽:
②装置II中发生反应的主要化学方程式为
③若未排净装置中的空气,则装置II中观察到的实验现象为
您最近一年使用:0次
2 . Ⅰ.钠、铝、铁是三种重要的金属,它们的单质及其化合物在生活生产中有重要的作用。请回答下列问题:
(1)钠着火不能用二氧化碳来灭火,已知钠在足量二氧化碳中燃烧生成炭黑和一种白色固体。根据实验现象写出方程式:_______ ,该反应中氧化剂和还原剂的物质的量之比为______ 。
Ⅱ.一些活泼金属也可作还原剂,将相对不活泼的金属从其化合物中置换出来。例如“铝热反应”的原理是: 。其反应装置如下图所示,已知镁条与氯酸钾反应产生高温可引发“铝热反应”。某同学对“铝热反应”的现象有这样的描述:“反应放出大量的热,并发出耀眼的光芒”;“纸漏斗的下部被烧穿,有熔融物落入装有沙子的蒸发皿中”。由化学手册查阅得有关物质的熔、沸点数据如下表。
。其反应装置如下图所示,已知镁条与氯酸钾反应产生高温可引发“铝热反应”。某同学对“铝热反应”的现象有这样的描述:“反应放出大量的热,并发出耀眼的光芒”;“纸漏斗的下部被烧穿,有熔融物落入装有沙子的蒸发皿中”。由化学手册查阅得有关物质的熔、沸点数据如下表。
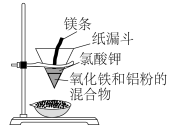
(2)该同学推测,铝热反应所得到的熔融物可能是铁铝合金。理由是该反应放出的热量使铁熔化,而铝的熔点比铁的低,此时液态的铁和铝熔合成铁铝合金,设计一个简单的实验方案,证明上述所得的块状熔融物中含有金属铝。该实验所用试剂是_____ (填化学式),该试剂与金属铝反应的离子方程式为_______ 。
(3)另一同学推测铝热反应得到的熔融物中还含有 ,他设计了如下方案来验证熔融物是否有
,他设计了如下方案来验证熔融物是否有 剩余:取一块该熔融物冷却后投入到稍过量稀硫酸中,向反应后的混合液中滴加物质甲的溶液,观察到溶液颜色未变红,证明该熔融物中不含有
剩余:取一块该熔融物冷却后投入到稍过量稀硫酸中,向反应后的混合液中滴加物质甲的溶液,观察到溶液颜色未变红,证明该熔融物中不含有 。则物质甲是
。则物质甲是_______ (填化学式)。该同学的实验方案是否合理?______ (填“合理”或“不合理”)。理由:_______ (用离子方程式说明)。
(1)钠着火不能用二氧化碳来灭火,已知钠在足量二氧化碳中燃烧生成炭黑和一种白色固体。根据实验现象写出方程式:
Ⅱ.一些活泼金属也可作还原剂,将相对不活泼的金属从其化合物中置换出来。例如“铝热反应”的原理是:
 。其反应装置如下图所示,已知镁条与氯酸钾反应产生高温可引发“铝热反应”。某同学对“铝热反应”的现象有这样的描述:“反应放出大量的热,并发出耀眼的光芒”;“纸漏斗的下部被烧穿,有熔融物落入装有沙子的蒸发皿中”。由化学手册查阅得有关物质的熔、沸点数据如下表。
。其反应装置如下图所示,已知镁条与氯酸钾反应产生高温可引发“铝热反应”。某同学对“铝热反应”的现象有这样的描述:“反应放出大量的热,并发出耀眼的光芒”;“纸漏斗的下部被烧穿,有熔融物落入装有沙子的蒸发皿中”。由化学手册查阅得有关物质的熔、沸点数据如下表。
| 物质 | Al |  | Fe |  |
| 熔点/℃ | 660 | 2054 | 1535 | 1460 |
| 沸点/℃ | 2467 | 2980 | 2750 |
(2)该同学推测,铝热反应所得到的熔融物可能是铁铝合金。理由是该反应放出的热量使铁熔化,而铝的熔点比铁的低,此时液态的铁和铝熔合成铁铝合金,设计一个简单的实验方案,证明上述所得的块状熔融物中含有金属铝。该实验所用试剂是
(3)另一同学推测铝热反应得到的熔融物中还含有
 ,他设计了如下方案来验证熔融物是否有
,他设计了如下方案来验证熔融物是否有 剩余:取一块该熔融物冷却后投入到稍过量稀硫酸中,向反应后的混合液中滴加物质甲的溶液,观察到溶液颜色未变红,证明该熔融物中不含有
剩余:取一块该熔融物冷却后投入到稍过量稀硫酸中,向反应后的混合液中滴加物质甲的溶液,观察到溶液颜色未变红,证明该熔融物中不含有 。则物质甲是
。则物质甲是
您最近一年使用:0次
2024-01-14更新
|
173次组卷
|
2卷引用:辽宁省部分高中2023-2024学年高一上学期期末考试高化学试题
3 . (1)利用原电池装置可以验证Fe3+与Cu2+氧化性相对强弱,如图所示。写出该氧化还原反应的离子方程式:___________ 。该装置中的负极材料是___________ (填化学式),正极反应式是___________ 。

(2)某研究性学习小组为证明 为可逆反应,设计如下两种方案(已知:酸性溶液中Fe2+易被空气氧化为Fe3+)。
为可逆反应,设计如下两种方案(已知:酸性溶液中Fe2+易被空气氧化为Fe3+)。
方案一:取5mL0.1mol/LKI溶液,滴加2mL0.1mol/L的FeCl3溶液,滴入5滴稀盐酸,再继续加入2mLCCl4,充分振荡、静置、分层,取上层清液,滴加KSCN溶液,现象是___________ ,即可证明该反应为可逆反应。你认为此方案___________ (“不严密”或“严密”),理由是___________ (用离子方程式表示)。
方案二:设计如图原电池装置,接通灵敏电流计,指针向右偏转,随着反应时间进行;电流计读数逐渐变小,最后读数变为零。当指针读数变零后,在右边的池了中加入1mol/L FeCl2溶液,灵敏电流计指针向左偏转,即可证明该反应为可逆反应。你认为灵敏电流计“读数变为零”的原因是___________ 。


(2)某研究性学习小组为证明
 为可逆反应,设计如下两种方案(已知:酸性溶液中Fe2+易被空气氧化为Fe3+)。
为可逆反应,设计如下两种方案(已知:酸性溶液中Fe2+易被空气氧化为Fe3+)。方案一:取5mL0.1mol/LKI溶液,滴加2mL0.1mol/L的FeCl3溶液,滴入5滴稀盐酸,再继续加入2mLCCl4,充分振荡、静置、分层,取上层清液,滴加KSCN溶液,现象是
方案二:设计如图原电池装置,接通灵敏电流计,指针向右偏转,随着反应时间进行;电流计读数逐渐变小,最后读数变为零。当指针读数变零后,在右边的池了中加入1mol/L FeCl2溶液,灵敏电流计指针向左偏转,即可证明该反应为可逆反应。你认为灵敏电流计“读数变为零”的原因是

您最近一年使用:0次
4 . 四氧化三铁俗称为磁性氧化铁,通常用作颜料、抛光剂和电讯器材等。某化学兴趣小组取磁性氧化铁进行铝热反应实验并对产物进行探究。

(1)取磁性氧化铁按图装置进行铝热反应,引发铝热反应的实验操作是__________ 。
(2)取少许反应生成的“铁块”溶于盐酸,滴加硫氰化钾溶液后溶液不变红,则______ (填“能”或“不能”)说明“铁块”一定不含四氧化三铁,理由是_________ 。
(3)设计一个简单的实验方案,证明上述所得的“铁块”中含有金属铝,该实验所用的试剂是__________ ,反应的离子方程式为___________ 。
(4)请写出此铝热反应的化学方程式:_____________ 。

(1)取磁性氧化铁按图装置进行铝热反应,引发铝热反应的实验操作是
(2)取少许反应生成的“铁块”溶于盐酸,滴加硫氰化钾溶液后溶液不变红,则
(3)设计一个简单的实验方案,证明上述所得的“铁块”中含有金属铝,该实验所用的试剂是
(4)请写出此铝热反应的化学方程式:
您最近一年使用:0次
2020-01-28更新
|
278次组卷
|
3卷引用:人教版高中化学必修1第三章《金属及其化合物》测试卷1
名校
5 . 向100mLFe2(SO4)3和CuSO4的混合溶液中逐渐加入铁粉,充分反应后溶液中剩余固体的质量与加入铁粉的质量关系如图所示。忽略溶液体积的变化,下列说法错误的是
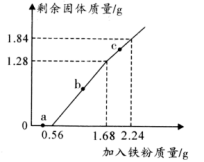
| A.a点时溶液中的阳离子为Cu2+、Fe2+和Fe3+ |
B.c点时溶液中发生的反应为: |
| C.c点时溶液中溶质的物质的量浓度为0.5mol/L |
D.原溶液中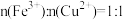 |
您最近一年使用:0次
2021-12-29更新
|
268次组卷
|
4卷引用:河南省南阳市六校2021-2022学年高一上学期第二次联考化学试题
6 . 如图是铁及其化合物的“价一类”二维图。下列说法错误的是


| A.乙是碱性氧化物,但乙不能与水反应生成丁 |
| B.K2FeO4具有强氧化性,可用于杀菌清毒 |
| C.甲高温时与水蒸气反应转化为丙 |
| D.若戊、己都是盐酸盐,则这两种物质均可通过化合反应获得 |
您最近一年使用:0次
2023-02-10更新
|
334次组卷
|
2卷引用:山东省济南市2022-2023学年高一上学期期末考试化学试题
7 . 对印刷电路板制作过程中( )产生废液
)产生废液 进行回收处理,流程如图所示。下列说法不正确的是
进行回收处理,流程如图所示。下列说法不正确的是

 )产生废液
)产生废液 进行回收处理,流程如图所示。下列说法不正确的是
进行回收处理,流程如图所示。下列说法不正确的是
A. 与 与 完全反应,转移电子数约为 完全反应,转移电子数约为 |
| B.实验室中进行操作①②时,需用到的玻璃仪器有烧杯、漏斗和玻璃棒 |
| C.若向溶液A中、溶液B中分别加入少量铁粉,铁粉均有减少 |
D.若废液 中滴加 中滴加 溶液变红,则 溶液变红,则 中 中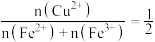 |
您最近一年使用:0次
名校
8 . 同一还原剂与多种氧化剂在一起时,先与氧化性强的粒子反应,待强的反应完后,再与氧化性弱的反应,称为反应先后规律。已知 ,且氧化性:
,且氧化性: ,在溶有
,在溶有 和
和 的溶液中加入铁粉,下列说法中正确的是
的溶液中加入铁粉,下列说法中正确的是
 ,且氧化性:
,且氧化性: ,在溶有
,在溶有 和
和 的溶液中加入铁粉,下列说法中正确的是
的溶液中加入铁粉,下列说法中正确的是A.若铁粉无剩余,且溶液中有 ,则溶液中一定无 ,则溶液中一定无 |
B.若铁粉无剩余,且溶液中无 ,则溶液中一定有 ,则溶液中一定有 ,也可能有 ,也可能有 |
| C.若铁粉有剩余,则不溶物中一定有铜 |
D.若铁粉有剩余,则溶液中的金属阳离子有 和 和 |
您最近一年使用:0次
2022-01-16更新
|
1670次组卷
|
6卷引用:河南省南阳市2021-2022学年高一上学期期末考试化学试题
2012·江苏·二模
名校
解题方法
9 . 向50mL稀H2SO4与稀HNO3的混合溶液中逐渐加入铁粉,假设加入铁粉的质量与产生气体的体积(标准状况)之间的关系如图所示,且每一段只对应一个反应。下列说法正确的
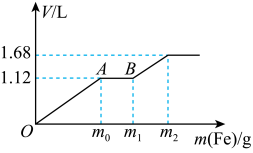

| A.开始时产生的气体为H2 |
| B.AB段产生的反应为置换反应 |
| C.所用混合溶液中c(HNO3)=0.5mol·L-1 |
| D.参加反应铁粉的总质量m2=5.6g |
您最近一年使用:0次
2020-08-20更新
|
461次组卷
|
37卷引用:2012届江苏省苏中三市高三5月第二次调研测试化学试卷
(已下线)2012届江苏省苏中三市高三5月第二次调研测试化学试卷(已下线)2014年高考化学 题型十一 图像分析型专题练习卷(已下线) 2012届江苏省苏中三市高三5月第二次调研测试化学试卷 2016届福建省仙游一中高三上学期10月月考化学试卷2017届河北省邯郸市大名一中高三上学期第一次月考化学试卷2017届湖北省沙市中学高三上学期第二次考试化学试卷安徽省六安市第一中学2017-2018学年高二上学期开学考试化学试题河北省深州中学2016-2017学年高一下学期期末考试化学试题河北省故城县高级中学2018届高三9月月考化学试题上海市交通大学附属中学2017-2018学年高二上学期第一次月考化学试题1山西省怀仁县第一中学2018届高三上学期第二次月考化学试题湖北省襄阳市第四中学2018届高三9月月考化学试题上海市交通大学附属中学2017-2018学年高二上学期第一次月考化学试题2上海交通大学附属中学2017-2018学年高二上学期第一次月考化学试题黑龙江省大庆实验中学2017-2018学年高一下学期开学考试化学试题云南省曲靖市麒麟高中2017-2018学年高一下学期期末考试化学试题上海市交通大学附属中学2017-2018学年高二上学期第一次月考化学试题3吉林省扶余市第一中学2018-2019学年高一下学期第一次月考化学试题云南省文山州马关县二中2019-2020学年高二上学期9月份考试化学试题云南省开远市实验中学2019-2020学年高二上学期开学考试化学试题云南省金平县第一中学2019-2020学年高一上学期期末考试化学试题云南省开远市第二中学校2019-2020学年高一上学期期末考试化学试题(已下线)上海市上海交通大学附属中学2017-2018学年高二10月月考化学试题云南省曲靖市陆良县联办高级中学2019-2020学年高一上学期期末考试化学试题(已下线)【南昌新东方】2019 新建二中 高一下 第一次月考安徽省安庆市怀宁县第二中学2019届高三上学期第四次月考化学试题重庆市外国语大学附属外国语学校2019-2020学年高一下学期期中考试化学试题黑龙江省哈尔滨师范大学青冈实验中学校2018-2019学年高二上学期开学考试化学试题(已下线)第6单元 常见的非金属元素(A卷 基础过关检测)-2021年高考化学一轮复习单元滚动双测卷(已下线)第三单元 物质的性质与转化(能力提升)-2020-2021学年高一化学必修第一册单元测试定心卷 (鲁科版2019)河南省汤阴县五一中学2019-2020学年高一下学期第四次月考化学试题浙江省杭州市富阳区第二中学2020-2021学年高一4月月考化学试题云南省楚雄中学2020-2021学年高一下学期4月月考化学试题广东省清远市2021-2022学年高一下学期期中调研考试化学试题贵州省六盘水市六枝特区2021-2022学年高一下学期期中教学质量检测化学试题安徽省淮北市第一中学2022-2023学年高一下学期第二次月考化学试题江西省丰城市第二中学2023-2024学年高一上学期11月期中考试化学试题
解题方法
10 . 部分含铁物质的分类与相应化合价的关系如图所示。
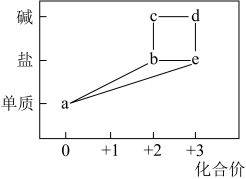
下列说法错误的是

下列说法错误的是
| A.a可与e反应生成b | B.c在空气中可转化为d |
| C.可用KSCN溶液鉴别b、e | D.可存在a→e→d→c→b→a的循环转化关系 |
您最近一年使用:0次
2021-07-12更新
|
1217次组卷
|
5卷引用:山东省日照市2020-2021学年高一下学期期末校际联合考试化学试题
山东省日照市2020-2021学年高一下学期期末校际联合考试化学试题(已下线)新人教必修1第3章第一节第3课时铁盐和亚铁盐(课中)(已下线)《新教材变化解读及考法剖析 》(人教版2019必修第一册)第三章(已下线)易错专题23 Fe2+和Fe3+的检验与转化-【突破易错·冲刺满分】2021-2022学年高一上学期化学期中期末易错专题(人教版2019)(已下线)第三章 铁 金属材料(B卷·能力提升练)-【单元测试】2022-2023学年高一化学分层训练AB卷(人教版2019必修第一册)



