名校
1 . 绿矾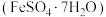 主要用于净水、照相制版及治疗缺铁性贫血等。工业上利用生活废铁(主要成分为
主要用于净水、照相制版及治疗缺铁性贫血等。工业上利用生活废铁(主要成分为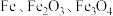 ,以及少量
,以及少量 等)制备绿矾的一种工艺流程如下:
等)制备绿矾的一种工艺流程如下:
(1)“焙烧”的目的是______ 。
(2)提高“酸溶”反应速率的措施是______ (任写一条)。“反应”时发生反应的离子方程式为______ 。
(3)隔绝空气的目的是______ ;一系列操作包括______ 、干燥。
(4)“酸溶”后,若溶液中 为
为 ,为了减少损失,常温下必须控制溶液的
,为了减少损失,常温下必须控制溶液的 小于
小于______  已知:
已知: 。
。
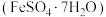 主要用于净水、照相制版及治疗缺铁性贫血等。工业上利用生活废铁(主要成分为
主要用于净水、照相制版及治疗缺铁性贫血等。工业上利用生活废铁(主要成分为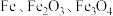 ,以及少量
,以及少量 等)制备绿矾的一种工艺流程如下:
等)制备绿矾的一种工艺流程如下: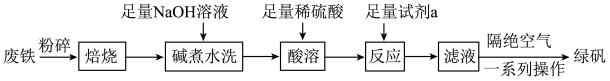
(1)“焙烧”的目的是
(2)提高“酸溶”反应速率的措施是
(3)隔绝空气的目的是
(4)“酸溶”后,若溶液中
 为
为 ,为了减少损失,常温下必须控制溶液的
,为了减少损失,常温下必须控制溶液的 小于
小于 已知:
已知: 。
。
您最近一年使用:0次
解题方法
2 . 根据实验目的,下列实验及现象操作、结论都正确的是
| 选项 | 实验目的 | 实验操作及现象 | 结论 |
| A | 制备Fe(OH)3胶体 | 向沸水中逐滴加入5~6滴饱和FeCl3溶液,持续加热,生成红褐色固体 | FeCl3与水反应产生Fe(OH)3胶体 |
| B | 验证Cl2的漂白性 | 将有色鲜花放入盛有干燥氯气的集气瓶中,盖上玻璃瓶,一段时间后有色鲜花褪色 | Cl2有漂白性 |
| C | 检验溶液中的Na+ | 用硫酸洗净后的铂丝蘸取少量溶液在酒精灯外焰上灼烧,产生黄色火焰 | 溶液中存在Na+ |
| D | 验证Fe3+的氧化性 | 在盛有2mLFeCl3的溶液中加入过量Fe粉,充分振荡后滴入几滴KSCN溶液,溶液未变红色 | Fe3+可以被Fe还原 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
3 . 某稀硫酸和稀硝酸混合溶液100 mL,逐渐加入铁粉,产生气体的量随铁粉加入量的变化如图所示,求原混合溶液 和
和 的浓度
的浓度___________ 。(需在答题纸上写出计算过程)

 和
和 的浓度
的浓度
您最近一年使用:0次
名校
4 . 某同学按图装置进行实验,最后可以使瓶中少量固体粉末溶解消失。下列物质组合不符合要求的是
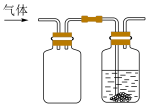

| 气体 | 液体 | 固体粉末 | |
| A |  |  | 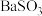 |
| B |  |  溶液 溶液 | Fe |
| C | HCl |  溶液 溶液 | Cu |
| D |  |  | AgCl |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-12-14更新
|
43次组卷
|
2卷引用:海南省海口市第一中学2023-2024学年高二上学期11月期中考试化学试题
名校
5 . 向盛有5mL0.005mol/LFeCl3溶液的试管中加入5mL0.015mol/LKSCN溶液,观察现象。将上述溶液平均分装在a、b、c三支试管中,向试管b中加入少量铁粉,向试管c中滴加vmLxmol/LKSCN溶液,观察试管b、c中溶液颜色的变化,并均与试管a对比。下列说法正确的是
| A.FeCl3溶液和KSCN溶液可以产生红色沉淀 |
| B.b试管中的现象说明:当其他条件不变时,增大生成物浓度平衡向逆反应方向移动 |
| C.为了证明其他条件不变时,增大反应物的浓度平衡向正反应方向移动,则x应该尽可能的大,而v应该尽可能的小 |
| D.若向试管a中加入4滴1mol/L的KCl溶液,溶液颜色会变深 |
您最近一年使用:0次
2023-11-09更新
|
142次组卷
|
2卷引用:湖南省长沙市长郡中学2023-2024学年高二上学期期中考试化学试题
解题方法
6 . 元素周期表中大多数元素是金属元素。小刀日常民用,大到国防军工,都能看到金属材料的身影。其中铁元素是最常见金属材料的组成元素。
(1)铁元素的相关信息如图所示,其相对原子质量是_______ 。

(2)有关铁的性质,说法正确的是_______。(选填编号)
(3)还原Fe粉可作脱氧剂,使用后为红棕色。将一包部分变质的脱氧剂用稀盐酸浸泡,浸泡过程中粉末表面会产生大量细小的无色气泡。补全溶液中可能发生的离子反应: Fe+2H+=Fe2++H2↑;_______ ;2Fe3++Fe=3Fe2+。
(4)若上述溶液充分反应后只含有Fe2+,欲检验Fe2+,不合理的操作是_______。(选填编号)
(1)铁元素的相关信息如图所示,其相对原子质量是

(2)有关铁的性质,说法正确的是_______。(选填编号)
| A.在空气中,加热Fe(OH)2可得FeO |
| B.一定条件下,Fe能与水蒸气反应生成H2 |
| C.常温下,Fe与浓H2SO4反应能产生SO2 |
| D.实验室用FeCl3溶液与NaOH溶液反应制备Fe(OH)3胶体 |
(4)若上述溶液充分反应后只含有Fe2+,欲检验Fe2+,不合理的操作是_______。(选填编号)
| A.加入氢氧化钠溶液观察现象 |
| B.先加入足量氯水,再加入KSCN溶液 |
| C.加入少量酸性KMnO4溶液观察现象 |
| D.先加入KSCN溶液,再滴加少量氯水观察现象 |
您最近一年使用:0次
7 . 下列关于元素及其化合物的性质说法不正确的是
A. 与 与 反应可生成C 反应可生成C |
B. 与 与 反应可生成 反应可生成 |
C.可通过化合反应生成 |
D.工业上用 和澄清石灰水反应来制备漂白粉 和澄清石灰水反应来制备漂白粉 |
您最近一年使用:0次
名校
8 . 下列实验事实可以用平衡移动原理解释的是
| A.合成氨工业中使用铁触媒作催化剂 | B.“NO2”球浸泡在热水中,颜色变深 |
| C.过量铁和稀硝酸反应,溶液变成浅绿色 | D.H2(g)+ I2 (g) 2HI(g),加压后颜色变深 2HI(g),加压后颜色变深 |
您最近一年使用:0次
名校
解题方法
9 . 黄铁矿烧渣(主要成分为Fe2O3、FeO、及少量FeS、SiO2等)是生产硫酸的工业废渣,其综合利用对环境保护具有现实意义。利用黄铁矿烧渣为原料制备高档颜料—铁红(Fe2O3)(主要成分为Fe2O3不考虑其他杂质),并以铁红为原料制备硫酸亚铁晶体(FeSO4·7H2O)的工艺:
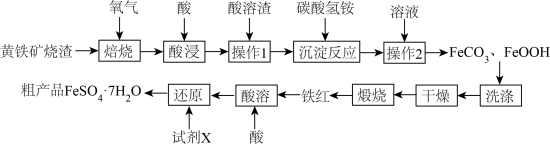
(1)焙烧的过程中采用如图所示的“多层逆流焙烧”,“多层逆流焙烧”的优点是_______ (任答两点)。

(2)“酸浸”时温度比较高,最适合的酸是_______ ,“酸溶渣”的成分是_______ 。
(3)“沉淀反应”中,生成FeCO3的离子方程式是_______ 。
(4)检验FeCO3是否洗涤干净的操作方法_______ 。
(5)从过滤后的滤液中得到产品,应进行的操作是_______ 、_______ 、过滤、洗涤、干燥。
(6)FeSO4·7H2O在医学上常用作补血剂。某课外小组通过以下实验方法测定某补血剂中亚铁离子的含量:
步骤I:取20片补血剂样品除去糖衣、研磨、溶解、过滤,将滤液配成250mL溶液。
步骤Ⅱ:取上述溶液25mL于锥形瓶中,加入少量稀硫酸酸化后,逐渐滴加0.0200 mol/L的KMnO4溶液,至恰好完全反应,记录消耗的KMnO4溶液的体积(假定药品中其他成分不与KMnO4反应,且 )。
)。
步骤Ⅲ:重复“步骤II”2-3次,平均消耗KMnO4溶液10.00mL。
①步骤I中配制溶液时需要的玻璃仪器除烧杯、量筒,玻璃棒外,还需要_______ 、_______ 。
②该补血剂中亚铁离子的含量为_______ mg/片。

(1)焙烧的过程中采用如图所示的“多层逆流焙烧”,“多层逆流焙烧”的优点是

(2)“酸浸”时温度比较高,最适合的酸是
(3)“沉淀反应”中,生成FeCO3的离子方程式是
(4)检验FeCO3是否洗涤干净的操作方法
(5)从过滤后的滤液中得到产品,应进行的操作是
(6)FeSO4·7H2O在医学上常用作补血剂。某课外小组通过以下实验方法测定某补血剂中亚铁离子的含量:
步骤I:取20片补血剂样品除去糖衣、研磨、溶解、过滤,将滤液配成250mL溶液。
步骤Ⅱ:取上述溶液25mL于锥形瓶中,加入少量稀硫酸酸化后,逐渐滴加0.0200 mol/L的KMnO4溶液,至恰好完全反应,记录消耗的KMnO4溶液的体积(假定药品中其他成分不与KMnO4反应,且
 )。
)。步骤Ⅲ:重复“步骤II”2-3次,平均消耗KMnO4溶液10.00mL。
①步骤I中配制溶液时需要的玻璃仪器除烧杯、量筒,玻璃棒外,还需要
②该补血剂中亚铁离子的含量为
您最近一年使用:0次
2022-11-13更新
|
217次组卷
|
2卷引用:浙江省杭州地区(含周边)重点中学2022-2023学年高二上学期期中考试化学试题
解题方法
10 . 把铁片放入下列溶液中,铁片溶解,溶液质量增加,且有气体放出的是
| A.稀盐酸 | B.AgNO3溶液 | C.CuSO4溶液 | D.Fe2(SO4)3溶液 |
您最近一年使用:0次
2022-06-18更新
|
380次组卷
|
3卷引用:浙江省杭州市北斗联盟2023-2024学年高二上学期期中联考化学试题



