名校
解题方法
1 . 现将有铜的印刷线路板浸入120mL氯化铁浓溶液中,有9.6g铜被腐蚀掉。取出印刷线路板,向溶液中加入8.4g铁粉,经充分反应,溶液中还存在4.8g不溶解的物质。(设溶液体积不变,且不考虑金属离子水解)。请回答下列问题:
(1)充分反应后,溶液中存在4.8g不溶物的成分为___________ (用化学式表示)。
(2)充分反应后溶液中一定不存在的金属离子为___________ 。
(3)比较 、
、 、
、 的氧化性大小:
的氧化性大小:___________ 。
(4)试计算最后溶液中 离子的物质的量浓度
离子的物质的量浓度___________ mol/L。
(1)充分反应后,溶液中存在4.8g不溶物的成分为
(2)充分反应后溶液中一定不存在的金属离子为
(3)比较
 、
、 、
、 的氧化性大小:
的氧化性大小:(4)试计算最后溶液中
 离子的物质的量浓度
离子的物质的量浓度
您最近一年使用:0次
2 . 为确定Fe和Fe2O3混合物样品的组成,称取该样品27.2g加入200mL盐酸中使其充分溶解,放出氢气的体积为2.24L(折算成标况),向反应后的溶液中加入KSCN颜色无明显变化,测得溶液中氢离子浓度为1.0mol/L(忽略溶液体积变化)。试计算:
(1)样品中铁的质量m(Fe)=___ 。
(2)盐酸的物质的量浓度c(HCl)=___ 。
(1)样品中铁的质量m(Fe)=
(2)盐酸的物质的量浓度c(HCl)=
您最近一年使用:0次
3 . 某同学利用如图所示的实验装置进行铁跟水蒸气反应的实验,并研究铁及其化合物的部分性质。

请回答下列问题:
(1)硬质试管中发生反应的化学方程式为___ 。
(2)一段时间后,取少量反应后的固体于试管中,加入过量盐酸,固体完全溶解,所得溶液B中存在的阳离子___ (填序号)。
a.一定有Fe2+、H+和Fe3+ b.一定有Fe2+、H+,可能有Fe3+
c.一定有Fe2+、Fe3+,可能有H+ d.一定有Fe3+、H+,可能有Fe2+
(3)该同学马上另取少量溶液B,使其跟NaOH溶液反应,可观察到生成白色沉淀,迅速变成灰绿色,最后变成红褐色的现象,请写出与上述现象相关的反应的化学方程式(并标出电子转移的方向和数目):___ 。
(4)实验室中含Fe2+的盐溶液现用现配的原因是___ ,故配制含Fe2+的盐溶液时应加入少量___ 。
(5)将一小块钠投入FeCl3溶液中,可观察到的现象除了“浮”、“熔”、“游”、“嘶”外,还有___ ,如何检验反应产物中是否含有铁单质___ ?(说明操作、现象、结论)
(6)另称取一定量的铁钉放入适量的浓硫酸中,加热,充分反应后收集气体。经测定气体中含有SO2、CO2和H2。
①铁与足量浓硫酸反应的化学方程式是___ 。
②气体中混有的CO2是___ 产物(填“氧化”或“还原”);干冰是其固态形式,可用于人工降雨、食品保鲜等,它属于___ 晶体(填“原子”、“离子”、“分子”或“金属”)。
③将672mL(STP)收集到的气体通入足量溴水中,发生反应:SO2+Br2+2H2O=2HBr+H2SO4,然后加入足量BaCl2溶液,经过滤、洗涤、干燥后得到固体4.66g。由此推知收集到的气体中SO2的体积分数是___ 。

请回答下列问题:
(1)硬质试管中发生反应的化学方程式为
(2)一段时间后,取少量反应后的固体于试管中,加入过量盐酸,固体完全溶解,所得溶液B中存在的阳离子
a.一定有Fe2+、H+和Fe3+ b.一定有Fe2+、H+,可能有Fe3+
c.一定有Fe2+、Fe3+,可能有H+ d.一定有Fe3+、H+,可能有Fe2+
(3)该同学马上另取少量溶液B,使其跟NaOH溶液反应,可观察到生成白色沉淀,迅速变成灰绿色,最后变成红褐色的现象,请写出与上述现象相关的反应的化学方程式(并标出电子转移的方向和数目):
(4)实验室中含Fe2+的盐溶液现用现配的原因是
(5)将一小块钠投入FeCl3溶液中,可观察到的现象除了“浮”、“熔”、“游”、“嘶”外,还有
(6)另称取一定量的铁钉放入适量的浓硫酸中,加热,充分反应后收集气体。经测定气体中含有SO2、CO2和H2。
①铁与足量浓硫酸反应的化学方程式是
②气体中混有的CO2是
③将672mL(STP)收集到的气体通入足量溴水中,发生反应:SO2+Br2+2H2O=2HBr+H2SO4,然后加入足量BaCl2溶液,经过滤、洗涤、干燥后得到固体4.66g。由此推知收集到的气体中SO2的体积分数是
您最近一年使用:0次
名校
4 . Ⅰ.A+B→X+Y+H2O(未配平,反应条件略去)是中学常见反应的化学方程式,其中A、B的物质的量之比为1:4.请回答:
(1)若Y是黄绿色气体,则该反应的离子方程式是______________ 。
(2)若A为非金属单质,构成它的原子核外最外层电子数是次外层电子数的2倍,B的溶液为某浓酸,则反应中氧化剂与还原剂的物质的量之比是______________ 。
(3)若A为金属单质,常温下A在B的浓溶液中“钝化”,且A可溶于X溶液中①A元素在周期表中的位置是第______________ 周期______________ 族,气体Y的化学式是______________ 。
②含amolX的溶液溶解了一定量A后,若溶液中两种金属阳离子的物质的量恰好相等,则被还原的X的物质的量为______________ mol。
(4)若A、B、X、Y均为化合物。A溶于水电离出的金属阳离子水解的生成物可净化水,向A溶液中加入硝酸酸化的AgNO3溶液,产生白色沉淀;B的焰色为黄色。则A与B按物质的量之比1:4恰好反应,所得溶液为无色时,该该反应的离子方程式是______________ 。
Ⅱ.用CH4催化还原氮氧化物可以消除氮氧化物的污染。已知:
①CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g)ΔH=-574kJ·mol-1
②CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g)ΔH=-1160kJ·mol-1
③H2O(g)=H2O(l)ΔH=-44.0kJ·mol-1
写出CH4(g)与NO2(g)反应生成N2(g)、CO2(g)和H2O(l)的热化学方程式______________ 。
(1)若Y是黄绿色气体,则该反应的离子方程式是
(2)若A为非金属单质,构成它的原子核外最外层电子数是次外层电子数的2倍,B的溶液为某浓酸,则反应中氧化剂与还原剂的物质的量之比是
(3)若A为金属单质,常温下A在B的浓溶液中“钝化”,且A可溶于X溶液中①A元素在周期表中的位置是第
②含amolX的溶液溶解了一定量A后,若溶液中两种金属阳离子的物质的量恰好相等,则被还原的X的物质的量为
(4)若A、B、X、Y均为化合物。A溶于水电离出的金属阳离子水解的生成物可净化水,向A溶液中加入硝酸酸化的AgNO3溶液,产生白色沉淀;B的焰色为黄色。则A与B按物质的量之比1:4恰好反应,所得溶液为无色时,该该反应的离子方程式是
Ⅱ.用CH4催化还原氮氧化物可以消除氮氧化物的污染。已知:
①CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g)ΔH=-574kJ·mol-1
②CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g)ΔH=-1160kJ·mol-1
③H2O(g)=H2O(l)ΔH=-44.0kJ·mol-1
写出CH4(g)与NO2(g)反应生成N2(g)、CO2(g)和H2O(l)的热化学方程式
您最近一年使用:0次
名校
5 . 将铁粉、铜粉、氧化铁、氧化铜溶于一定量的盐酸溶液中,充分反应,试判断下列情况溶液中存在的金属化合物。
(1)若铁粉有剩余,则溶液中一定有___________ (填溶质的化学式,下同)。
(2)若铜粉有剩余,则溶液中一定有___________ ,可能有___________ 。
(3)若溶液中有氯化铜,则溶液中一定还有___________ 。
(1)若铁粉有剩余,则溶液中一定有
(2)若铜粉有剩余,则溶液中一定有
(3)若溶液中有氯化铜,则溶液中一定还有
您最近一年使用:0次
名校
解题方法
6 . 将铁粉,铜粉,FeCl3溶液和CuCl2溶液混合于某溶液中充分反应,判断下列情况下,溶液中存在的金属离子和金属单质。
(1)若铁粉有剩余,则溶液中不可能有的离子是_______ ,铜单质______ (填“一定”或“可能”)存在.
(2)若氯化铁和氯化铜都有剩余.则容器中不可能有的单质是_______ , Fe2+_______ ,(填“一定”或“可能”)存在。
(3)若充分反应后,容器中没有固体,则反应的化学方程式有________________ 。
(1)若铁粉有剩余,则溶液中不可能有的离子是
(2)若氯化铁和氯化铜都有剩余.则容器中不可能有的单质是
(3)若充分反应后,容器中没有固体,则反应的化学方程式有
您最近一年使用:0次
解题方法
7 . 按要求填空
(1)“四种基本反应类型与氧化还原反应的关系”如图所示:

其中I为化合反应,IV是___________ 反应。请写出一个符合IV的化学反应方程式_______________________________________________________ 。
(2)鲜榨苹果汁是人们喜爱的饮料,由于此饮料中含Fe2+,现榨的苹果汁在空气中会由淡绿色(Fe2+)变为棕黄色(Fe3+)。这个变色过程中的Fe2+被_________ (填“氧化”或“还原”),若榨汁时加入适量的维生素C可有效防止这种现象的发生,这说明维生素C具有_______ 性。(填“氧化”或“还原”)
(3)电子工业常用30%的FeCl3溶液腐蚀敷在绝缘板上的铜箔来制造印刷电路板。写出FeCl3溶液与铜发生反应的离子方程式:_____________________________________ 。若向盛有氯化铁溶液的烧杯中同时加入铁粉和铜粉,反应结束后,下列结果不可能出现的是_________ 。
A.有铜无铁 B.有铁无铜 C.铁、铜都有 D.铁、铜都无
(1)“四种基本反应类型与氧化还原反应的关系”如图所示:

其中I为化合反应,IV是
(2)鲜榨苹果汁是人们喜爱的饮料,由于此饮料中含Fe2+,现榨的苹果汁在空气中会由淡绿色(Fe2+)变为棕黄色(Fe3+)。这个变色过程中的Fe2+被
(3)电子工业常用30%的FeCl3溶液腐蚀敷在绝缘板上的铜箔来制造印刷电路板。写出FeCl3溶液与铜发生反应的离子方程式:
A.有铜无铁 B.有铁无铜 C.铁、铜都有 D.铁、铜都无
您最近一年使用:0次
解题方法
8 . 将铁粉、铜粉、FeCl3溶液、FeCl2溶液和CuCl2溶液混合于某容器中充分反应(容器不参与反应),试判断下列情况溶液中存在的金属离子和金属单质。
(1)若铁粉有剩余,则容器不可能有__ 。
(2)若CuCl2有剩余,则容器中一定有__ ,可能有__ 。
(3)若FeCl3和CuCl2都有剩余,则容器中不可能有__ ,一定有__ 。
(4)FeCl3和Fe粉反应时,氧化产物与还原产物的物质的量之比为__ 。
(1)若铁粉有剩余,则容器不可能有
(2)若CuCl2有剩余,则容器中一定有
(3)若FeCl3和CuCl2都有剩余,则容器中不可能有
(4)FeCl3和Fe粉反应时,氧化产物与还原产物的物质的量之比为
您最近一年使用:0次
19-20高一·全国·课时练习
9 . 已知X为Fe2O3和CuO的混合物,且氧化性强弱顺序:Fe3+>Cu2+>H+>Fe2+。X样品可发生如图所示的转化关系:
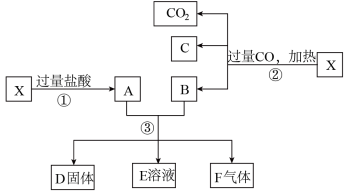
(1)写出步骤③可能发生反应的离子方程式:___ 。
(2)若溶液E中只有一种金属离子,则一定是____ ;若溶液E中含有两种金属离子,则一定是___ 。
(3)若D固体是纯净物,该固体是__ (填化学式)。

(1)写出步骤③可能发生反应的离子方程式:
(2)若溶液E中只有一种金属离子,则一定是
(3)若D固体是纯净物,该固体是
您最近一年使用:0次
2013·上海·一模
解题方法
10 . 向FeCl3溶液中加入铁粉和铜粉混合粉末,充分反应后,分析溶液中的溶质和可能残留固体不溶物的成分。请完成下列表格
| 序号 | 溶液中的盐 | 固体不溶物的成分 |
| ① | FeCl2、CuCl2、FeCl3 | |
| ② | 无 | |
| ③ | FeCl2、CuCl2 | |
| ④ | Cu | |
| ⑤ | Fe、Cu |
您最近一年使用:0次



